Pluton
| Pluton | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
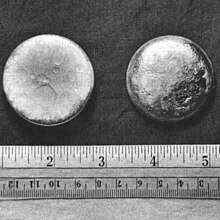 Peletki z plutonu. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pozycja w układzie okresowym | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Symbol | Mógłby | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nazwisko | Pluton | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liczba atomowa | 94 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupa | - | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kropka | 7- ty okres | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | Blok f | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rodzina elementów | aktynowiec | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroniczna Konfiguracja | [ Rn ] 5 f 6 7 s 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrony według poziomu energii | 2, 8, 18, 32, 24, 8, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomowe właściwości pierwiastka | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atomowa | 244,06 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Promień atomowy (obliczony) | 159 po południu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Promień kowalencyjny | 187 ± 1 po południu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stan utlenienia | 6, 5, 4, 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroujemności ( Paulinga ) | 1,28 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlenek | Amfoteryczny | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energie jonizacji | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 Re : 6,0260 eV | 2 E : 11,2 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Najbardziej stabilne izotopy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proste właściwości fizyczne ciała | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Państwo zwykłe | solidny | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa objętościowa | 19 816 kg · m -3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kryształowy system | Jednoskośny | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kolor | Srebrzysty biały matowienie na otwartej przestrzeni | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punkt fuzji |
640 ° C 640 ° ± 2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura wrzenia | 3228 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia termojądrowa | 2,84 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia parowania | 344 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Objętość molowa | 12,29 × 10 -6 m 3 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ciśnienie pary |
1 Pa (przy 1483 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prędkość dźwięku | 2260 m · s -1 do 20 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ogromne ciepło | 35,5 J · kg -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Przewodnictwo elektryczne | 685 x 10 6 S · m -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Przewodność cieplna | 6,74 W · m -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Różnorodny | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O ECHA | 100 028,288 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O WE | 231-117-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Środki ostrożności | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Pierwiastek promieniotwórczy o znacznej aktywności |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednostki SI i STP, chyba że zaznaczono inaczej. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Pluton jest pierwiastkiem o symbolu Pu i liczbę atomową 94. Jest metalu radioaktywnego transuranowych rodziny z aktynowcami . Ma postać skrystalizowanego ciała stałego, którego świeże powierzchnie są srebrzystoszare, ale w ciągu kilku minut, w obecności wilgoci, pokrywa się matową warstwą szarego koloru, czasami przechodzącą w oliwkową, składającą się z tlenków i wodorków ; wynikający z tego wzrost objętości może osiągnąć 70% bloku czystego plutonu, a tak utworzona substancja ma tendencję do rozpadu na proszek piroforyczny .
Pluton został po raz pierwszy wyprodukowany i izolowane na 14 grudnia 1940 roku na Uniwersytecie Kalifornijskim w Berkeley przez bombardowanie uranu 238 z deuteru . Ten nowy pierwiastek chemiczny , wywodzący się z układu okresowego pierwiastków po uranie i neptunie , został nazwany w odniesieniu do Plutona , który pochodzi od planet Uran i Neptun w Układzie Słonecznym . Jest to pierwiastek syntetyczny , wytwarzany sztucznie przez człowieka, ale odnotowano również obserwacje śladów naturalnego plutonu w rudach uranu . Jest radiotoksycznym metalem ciężkim, który ma tendencję do gromadzenia się w kościach i, w mniejszym stopniu, w wątrobie . Zwykle obserwujemy cztery stopnie utlenienia plutonu, od +3 do +6 (stan +7 jest rzadki), z wyraźnymi zabarwieniami. Strukturę elektronową czystego metalu określa pasmo 5f, które ma największą gęstość stanów na poziomie Fermiego ; Szczególnie wąskie, pasmo 5f ma tendencję do lokalizowania w nim elektronów, tak że czysty pluton w temperaturze pokojowej jest podobny do ciężkich materiałów fermionowych , o dużej pojemności cieplnej i oporności elektrycznej .
Znamy co najmniej sześć alotropów plutonu pod ciśnieniem atmosferycznym i jedną siódmą powyżej 60 MPa . Mają dobrze zdefiniowane i często nietypowe dla metalu właściwości. Tak więc α pluton, stabilny w temperaturze pokojowej, jest jednym z bardzo rzadkich metali, które krystalizują w układzie jednoskośnym ; jego właściwości fizyczne i strukturalne odnoszą się bardziej do minerałów niż do metali nieszlachetnych, podczas gdy jego właściwości mechaniczne przypominają właściwości żeliwa . Δ pluton, stabilną w temperaturze wyższej lub niskiej ułamek molowy w galu , krystalizuje się z drugiej strony w siatce płaskocentryczną sześcienny , o gęstości zmniejszyć prawie o 20% większy od pluton α; jest bardziej metaliczny, o właściwościach mechanicznych zbliżonych do aluminium , ale o ujemnym współczynniku rozszerzalności cieplnej (kurczy się przy ogrzewaniu). Pluton jest również jednym z nielicznych pierwiastków chemicznych, których ciecz w temperaturze topnienia jest gęstsza od ciała stałego . Istnienie wielu alotropów z sąsiednimi energiami wewnętrznymi sprawia, że kształtowanie plutonu jest szczególnie delikatne, do tego stopnia, że zamiast niego stosuje się stop plutonowo-galowy , który stabilizuje fazę δ w temperaturze pokojowej, co ułatwia obróbkę części w plutonie.
Pluton 239 i pluton 241 są rozszczepialne izotopy z neutronami termicznymi , które to środki mogą przyczyniać się do reakcję łańcuchową i mogą być stosowane w konstrukcji broni jądrowej i reaktorów jądrowych . Pluton 240 ma wskaźnik spontanicznego rozszczepienia bardzo wysokie, co wymaga, aby utrzymać szybkość poniżej 7% plutonu broni jakości. Pluton 238 ma okres półtrwania 88 lat i emituje cząstki alfa ; jest to źródło ciepła często wykorzystywane przez termoelektryczne generatory radioizotopów do zasilania energią elektryczną niektórych sond kosmicznych . Oddzielenie izotopów od plutonu jest trudne i zwykle są one produkowane specjalnie przez wyspecjalizowane reaktory. Produkcja wystarczającej ilości plutonu była jednym z celów Projektu Manhattan podczas II wojny światowej w celu opracowania pierwszych bomb atomowych. Pierwsza eksplozja atomowa, test Trinity , wykorzystywała ładunek plutonu, podobnie jak Fat Man , bombę atomową zrzuconą na Nagasaki ; Bomba Little Boy zrzucona trzy dni wcześniej na Hiroszimę miała rdzeń wzbogacony uranem .
Nazwisko
Swoją nazwę pluton zawdzięcza planecie Pluton , odkrytej po Uranie i Neptunie , przez analogię do pierwiastków uran i neptun bezpośrednio go poprzedzających w układzie okresowym pierwiastków.
Nieruchomości
- Pluton widziany przez krawędź placka solnego z wielocyklowego procesu bezpośredniej redukcji tlenków ( MCDOR ): dwutlenek plutonu PuO 2rozpuszcza się w chlorku wapnia CaCl 2stopiony w temperaturze 820 do 875 °C w tyglu z tlenku magnezu MgO w celu zredukowania tam do metalicznego plutonu.
- Promień metaliczny (w kolorze czarnym) aktynowców . Zaobserwowano, że metaliczny promień protaktynu , uranu , neptunu i plutonu jest znacznie mniejszy niż w przypadku innych aktynowców ( toru , ameryku , kiuru , berkelu itp.). Efekt ten można przypisać elektronów z tych 5f orbitali .
Fizyczny
Pluton jest metalem z rodziny z aktynowców z, jak w większości innych metali, jasnym srebrzystym wyglądzie, takie jak nikiel . Jednak w kontakcie z powietrzem szybko pokrywa się matową szarawą warstwą, której kolory mogą nawiązywać do żółci lub oliwkowej zieleni, przy czym ten ostatni odcień pochodzi z dwutlenku plutonu PuO 2..
Podobnie jak neptun i uran – iw mniejszym stopniu protaktyn – struktura elektronowa plutonu w normalnych warunkach temperatury i ciśnienia jest określana przez orbitale 5f, które są głównymi współtwórcami wiązań międzyatomowych. Odległości między atomami są zmniejszone w tych materiałach, które w związku z tym mają szczególnie wysoką gęstość : gęstość plutonu wynosi 19,816 g · cm -3 , ponad dwukrotnie więcej niż einsteinium ( 8,84 g · cm -3 ), który jednak ma wyższy atom masa . Jednak odległości międzyatomowe w krysztale wpływają na szerokość pasm elektronowych : im mniejsze te odległości, tym węższe pasma. Pasmo 5f jest matematycznie węższe niż pasma 6d i 7s, staje się tutaj wystarczająco wąskie, aby mieć tendencję do lokalizowania elektronów w krysztale, którego właściwości metaliczne są w konsekwencji znacznie degradowane. Z tego wynika cała złożoność plutonu: biorąc pod uwagę bardzo szczególną strukturę pasmową materiału, gdzie pasma 5f i 6d mają bardzo podobne poziomy energii, elektrony 5f plutonu znajdują się na granicy między stanem zlokalizowanym a stanem zdelokalizowanym w krysztale , dzięki czemu wystarczy niewielka zmiana energii wewnętrznej, aby przejść z jednej na drugą, co powoduje gwałtowne zmiany właściwości makroskopowych materiału.
W wyniku wpływu elektronów 5f kryształy lekkich aktynowców są mniej symetryczne niż metali zwykłych, ponieważ orbitale 5f są bardzo kierunkowe i ograniczają geometrię kryształów. Protaktyn krystalizuje w układzie kwadratowym , mniej symetrycznie niż w przypadku metali nieszlachetnych, podczas gdy uran i neptun krystalizuje w układzie rombowym , jeszcze mniej symetrycznie, a pluton krystalizuje w układzie jednoskośnym , najmniej symetrycznym ze wszystkich. Wynika z tego, że pluton w stanie standardowym jest mało plastyczny , mało plastyczny , mało plastyczny , a przeciwnie jest raczej twardy i kruchy; jego właściwości mechaniczne są często porównywane do właściwości żeliwa szarego .
Inną konsekwencją wpływu elektronów 5f, pluton w stanie standardowym ma niską przewodność elektryczną i niską przewodność cieplną , ale wysoką pojemność cieplną , podobną do ciężkich materiałów fermionowych . Ponadto jego przewodnictwo elektryczne ma tendencję do zmniejszania się, gdy materiał jest chłodzony, co jest przeciwieństwem zwykłego zachowania metali. Trend obserwuje się do 100 K , a następnie odwraca się dla świeżego plutonu; jednak rezystywność wzrasta z czasem z powodu uszkodzenia sieci krystalicznej z powodu radioaktywności.
| Metal |
Przewodność cieplna |
Rezystywność elektryczna |
Ściśliwość |
Younga sprężystości |
|---|---|---|---|---|
| pluton α | 4,2 W · m -1 · K -1 | 1,45 μΩ · m | 0,020 GPa -1 | 100 GPa |
| pluton δ ( Pu-Ga ) | 9,2 W · m -1 · K -1 | 1,00 μΩ · m | 0,033 GPa -1 | 42 GPa |
| Stal nierdzewna | 15 W · m -1 · K -1 | 0,7 μΩ · m | 0,0007 GPa -1 | 180 GPa |
| Aluminium | 222 W · m -1 · K -1 | 0,029 μΩ · m | 0,015 GPa -1 | 70 GPa |
Ogólnie rzecz biorąc, radioaktywność zaburza strukturę krystaliczną plutonu poprzez kumulowanie się defektów krystalicznych . Jednak samopromieniowanie może również nagrzać materiał dostatecznie, aby doprowadzić do wyżarzania , kompensując poprzedni efekt do temperatur powyżej 1000 K .
Znanych jest około dwudziestu izotopów plutonu . Pluton-244 ma okres półtrwania dłuższy, z 80,8 mln lat temu, a następnie plutonu 242 , z 373 300 lat, a pluton-239 , z 24 110 lat. Wszystkie inne izotopy plutonu mają okres półtrwania krótszy niż 7000 lat. Pluton ma również osiem izomerów jądrowych , których okres półtrwania jest zawsze krótszy niż jedna sekunda.
Znane izotopy plutonu mają masę atomową w zakresie od 228 do 247. Preferowanym sposobem rozpadu izotopów lżejszych niż pluton 244 jest samorzutne rozszczepienie i rozpad α , w wyniku którego powstaje głównie neptun i uran , a także szeroka gama produktów rozszczepienia. . Preferowanym sposobem rozpadu izotopów cięższych niż pluton 244 jest rozpad β , który zasadniczo wytwarza ameryk . Pluton-241 to izotop dominującą neptun serii rozpadu, co daje ameryk-241 przez p rozkładu.
Pluton-239 jest z uranu-233 i uranu-235 , jeden z trzech głównych rozszczepialnych izotopów wykorzystywane przez przemysł jądrowy lub do celów wojskowych. Pluton-241 jest również bardzo rozszczepialne, to znaczy może on podzielony pod wpływem działania neutronów termicznych uwalniającego więcej neutronów wystarczający do rozszczepiania innych atomów, a tym samym utrzymywać reakcję łańcuchową ; jest jednak znacznie bardziej radioaktywny niż pluton 239 i wytwarza, poprzez rozpad β , ameryku 241 , silnego emitera niepożądanych cząstek α w typowych zastosowaniach plutonu. Po poddaniu neutronów termicznych izotopy 239 PU i 241 PU ma prawdopodobieństwo około 3 / 4 pękania i około 1 / 4 dając 240 PU i 242 Pu odpowiednio, tak, że stopa 240 PU resztkowego plutonu PO reakcja jądrowa jest większa niż początkowego plutonu.
Zasadniczo mniej radioaktywny niż większość innych izotopów, jednak czysty pluton 239 ma współczynnik mnożenia k eff większy niż 1, co oznacza, że ten materiał może osiągnąć masę krytyczną, o ile wystarczająca ilość materiału zostanie zebrana w odpowiedniej objętości. Podczas rozszczepienia atomu ułamek energii wiązania jądrowego , który utrzymuje jądro atomowe razem , jest uwalniana w postaci energii elektromagnetycznej i energii kinetycznej , przy czym ta ostatnia jest szybko przekształcana w energię cieplną . Rozszczepienie jednego kilograma plutonu-239 może powodować eksplozję odpowiada 21 kt z TNT ( 88,000 GJ ). To właśnie ta energia jest wykorzystywana przez reaktory jądrowe i broń jądrową .
Obecność plutonu 240 w masie plutonu-239 ogranicza jego znaczenie militarne, ponieważ izotop ten ma szybkość samorzutnego rozszczepienia wyższą o ponad cztery rzędy wielkości od plutonu 239 - około 440 rozszczepienie · s -1 · G -1 lub więcej niż 1000 neutronów · s -1 · g -1 - co obniża właściwości wybuchowe materiału i zwiększa ryzyko niekontrolowanej eksplozji. Mówi się, że pluton jest klasy wojskowej (klasa do broni ), gdy zawiera mniej niż 7% plutonu 240 , a klasy paliwowej (klasa paliwowa ), gdy zawiera mniej niż 19%. Wysoka jakość pluton ( supergrade ), zawierająca mniej niż 4% plutonu 240 , używany, ze względu na jego dolnej radioaktywności dla broni jądrowej, które muszą być przechowywane w bezpośrednim sąsiedztwie załóg, w atomowych okrętów podwodnych wyrzutni z narzędzi i różnych typów okrętów wojennych dla przykład. Pluton-238 nie jest rozszczepialny, ale łatwo można fissioned napędzany przez szybkie neutrony i alfa radioaktywności .
Dwa główne zsyntetyzowane izotopy to pluton 238 i pluton 239 . Pluton-239 jest produkowany przez wychwyt neutronów i rozkładu z p o uran-238 :
W neutronów z rozszczepienia o uranu 235 są przejmowane przez jąder z uranu 238 , z wytworzeniem uranu 239 ; β rozpad przekształca neutronu do protonu do formy neptun 239 , przekształcany przez drugi rozpadu beta w plutonu 239 .
Pluton-238 jest produkowany przez bombardowanie uranu-238 z jonami o deuteru :
Radioaktywność
Oprócz plutonu 240 , który charakteryzuje się dużą szybkością samorzutnego rozszczepienia , i plutonu 241 , który rozpada się pod wpływem promieniotwórczości β , spontaniczny rozpad głównych izotopów plutonu odbywa się głównie na drodze promieniotwórczości α , czyli emisji cząstek α ( He 2+ ), które rekombinują z elektronami metalu tworząc hel , podczas gdy pluton ulega transmutacji w uran . Tak więc typowy 5 kg rdzeń broni jądrowej zawiera 12,5 × 10 24 atomów, co daje aktywność 11,5 × 10 12 Bq ( rozpadów na sekundę) emitujących cząstki α, co odpowiada całkowitej mocy 9 68 W .
| Izotop | Kropka
radioaktywny |
Aktywność masowa |
Tryb zaniku |
syn nuklidowy |
Raport połączenia |
Energia rozpadu |
|---|---|---|---|---|---|---|
| 238 Pu | 87,76 lat | 6,34 x 10 11 Bq · g-1 | Α promieniotwórczość | 234 U | 71,04% | 5,499 MeV |
| 28,84% | 5,457 MeV | |||||
| 239 Pu | 24 130 lat | 2,295 x 10 9 Bq · g-1 | Α promieniotwórczość | 235 jednostek | 73,30% | 5,156 MeV |
| 15,10% | 5,144 MeV | |||||
| 11,45% | 5,106 MeV | |||||
| 240 pu | 6567,5 lat | 8,40 x 10 9 Bq · g-1 | Α promieniotwórczość | 236 U | 72,90% | 5,168 MeV |
| 27,00% | 5.124 MeV Me | |||||
| 241 Pu | 14,29 lat | 3,81 × 10 12 Bq g-1 | Β promieniotwórczość | 241 rano | 99,99% | 20,81 keV |
Do radioizotopów plutonu uwalniają ciepło rozkładu zmiennej w zależności od rozpatrywanych izotopów. Wielkość ta jest zwykle podawana w watach na kilogram lub miliwatach na gram . Może osiągnąć znaczne wartości w dużych częściach plutonu (na przykład w głowicach nuklearnych ). Wszystkie izotopy plutonu emitują również słabe promienie γ .
| Izotop | Ciepło rozpadu | Spontaniczne rozszczepienie ( neutrony ) | Uwagi |
|---|---|---|---|
| 238 Pu | 560 W · kg -1 | 2600 g -1 · s -1 | Ciepło o bardzo dużym rozpadzie stosowane w radioizotopowych generatorach termoelektrycznych |
| 239 Pu | 1,9 W · kg -1 | 0,022 g -1 · s -1 | Główny izotop rozszczepialny plutonu. |
| 240 pu | 6,8 W · kg -1 | 910 g -1 · s -1 | Główne zanieczyszczenie plutonu 239 . Jakość plutonu jest ogólnie wyrażana jako procent 240 Pu. Szybkość spontanicznego rozszczepienia jest niekorzystna dla zastosowań wojskowych. |
| 241 Pu | 4,2 W · kg -1 | 0,049 g -1 · s -1 | Rozpada się do ameryku 241 . Jego akumulacja stwarza ryzyko napromieniowania przez stare kawałki plutonu. |
| 242 Pu | 0,1 W · kg -1 | 1700 g -1 · s -1 |
Alotropy
Istnieje sześć alotropów plutonu pod ciśnieniem atmosferycznym, a siódmy powyżej 60 MPa . Te alotropy mają energię wewnętrzną, która niewiele się zmienia, podczas gdy ich właściwości fizyczne zmieniają się dramatycznie. Gęstości czystego plutonu przy ciśnieniu atmosferycznym, to w ten sposób 19,86 g · cm -3 plutonu α w temperaturze pokojowej, ale tylko 15,92 g · cm -3 plutonu δ w 125 ° C , o gęstości 20% mniejsza, co odpowiada liniowej wydłużenia o ponad 7,6%. Pluton może więc gwałtownie reagować na zmiany ciśnienia, temperatury lub środowiska chemicznego, a przemianom fazowym mogą towarzyszyć znaczne i gwałtowne zmiany objętości.
| Faza | Kryształowy system |
Temperatura od przejścia fazowego |
Masa objętościowa |
|---|---|---|---|
| α | Pojedyncza klinika | - | 19,86 g · cm -3 |
| β | Monoklina z wyśrodkowanymi podstawami | 124,5 °C | 17,70 g · cm -3 |
| γ | Twarz wyśrodkowany rombowy | 214,8 °C | 17,14 g · cm -3 |
| δ | sześcienny skupiony na twarzy | 320,0 °C | 15,92 g · cm -3 |
| ' | Wyśrodkowany kwadratowy | 462,9 °C | 16,00 g · cm -3 |
| ε | Wyśrodkowany sześcienny | 482,6 °C | 16,51 g · cm -3 |
| Ciekły | ~ 640 °C | 16,65 g · cm -3 | |
- Układy krystaliczne czystego plutonu
-
Jednoskośny (α)
-
Wyśrodkowany na czworokąt (δ ')
Istnienie tak różnych alotropów dla tak podobnych energii wewnętrznych sprawia, że kształtowanie czystego plutonu jest szczególnie delikatne. Jego stan standardowy , faza α, jest jednoskośna , dzięki czemu czysty pluton w temperaturze pokojowej jest twardym i kruchym materiałem, takim jak żeliwo szare , które mało poddaje się obróbce i jest podatne na nagłe zmiany geometrii pod ciśnieniem. Z drugiej strony, faza δ jest sześcienna , podobnie jak wiele popularnych metali, takich jak aluminium i nikiel , i ma właściwości mechaniczne podobne do aluminium . Stabilna od 320,0 do 462,9 °C dla czystego plutonu, faza δ może być stabilizowana do temperatury pokojowej przez dodanie niewielkiej ilości galu , aluminium, ameryku , skandu lub ceru , które mogą być obrabiane i spawane z plutonu. Stopu pluton galu są często używane do tego celu, ponieważ sprawia, że możliwe jest przezwyciężenia niepożądanych przemian fazowych powodowania zakłóceń na skutek pęcznienia lub skurcze się w części. Krzemu The indu The cynku i cyrkonu umożliwić powstawanie δ fazy metastabilnej przez szybkie chłodzenie. Dodatek dużych ilości hafnu , holmu i talu umożliwia również zachowanie fazy δ do temperatury pokojowej. Neptunium jest jedynym elementem, który stabilizuje a fazą monokliniczną temperaturze wyższej.
Elastyczność fazy hemibursztynianu jest anizotropowy , który może zmieniać się o współczynnik sześciu do siedmiu, w zależności od kierunku.
W broniach rozszczepialnych fala uderzeniowa ściskająca jądro (powyżej kilkudziesięciu kilobarów) powoduje również przejście z fazy delta do formy alfa, wyraźnie gęstszej, co umożliwia łatwiejsze osiągnięcie krytyczności .
Stopy
Stopy pluton mogą być uzyskane poprzez dodanie metalu do stopionego plutonu. Jeśli dodany metal jest wystarczająco redukujący , pluton może być dostarczany w postaci tlenków lub halogenków . Pluton galu stopu i stopu pluton aluminium, które stabilizują fazę hemibursztynianu plutonu w temperaturze pokojowej, otrzymuje się przez dodanie pluton trifluorek puf 3ze stopionym galem lub aluminium , co ma tę zaletę, że unika się manipulowania metalicznym plutonem, który jest bardzo reaktywny.
- Pluton-gal Pu-Ga - Główny stop stosowany do formowania , obróbki skrawaniem i spawania elementów plutonu unikając problemów strukturalnych związanych z przemianami fazowymi α – . Jest używany głównie do realizacji nuklearnej broni implozyjnej.
- Pluton-aluminium Pu-Al - Alternatywa dla stopu plutonu-galu, ale ma tendencję do interakcji z cząsteczkami α poprzez emisję neutronów , co zmniejsza zainteresowanie wytwarzaniem broni jądrowej. Z drugiej strony może być wykorzystany do produkcji paliwa jądrowego .
- Pluton-gal-kobalt PuCoGa 5- nadprzewodnik niekonwencjonalny wykazujący nadprzewodnictwo poniżej 18,5 K , o rząd wielkości powyżej wyższego z systemów ciężkich fermionów i o wysokim prądzie krytycznym.
- Plutonium-Cerium Pu-Ce i Plutonium-Cerium-Cobalt Pu-Ce-Co - Może być stosowany jako paliwo jądrowe.
- Uran-pluton U-Pu - Zawierający około 15-30 procent atomowych plutonu stop ten może być stosowany jako paliwo jądrowe w reaktorach rozrodczych . Jest piroforyczny i bardzo wrażliwy na korozję, aż do zapalenia lub rozpadu w kontakcie z powietrzem, co wymaga łączenia z innymi składnikami. Dodatek aluminium, węgla czy miedzi nie zapewnia żadnej zauważalnej poprawy, natomiast cyrkon i żelazo poprawiają odporność na korozję, ale nie zapobiegają gniciu po kilku miesiącach ekspozycji na powietrze. Dodatek tytanu lub cyrkonu podnosi temperaturę topnienia stopu.
- Uran-pluton-cyrkon U-Pu-Zr - Może być stosowany jako paliwo jądrowe, szczególnie w reaktorach regenerujących. Tytan i cyrkon zwiększają odporność na korozję, zmniejszają palność oraz poprawiają ciągliwość, wytrzymałość, skrawalność i właściwości termiczne. Stop U-Pu-Mo uran-pluton-molibden ma najlepszą odporność na korozję, ale tytan i cyrkon są preferowane w stosunku do molibdenu ze względu na lepsze właściwości fizyczne.
- Tor-uran-pluton Th-U-Pu - Badany jako możliwe paliwo jądrowe do reaktorów reprodukcyjnych.
Chemia
Czysty pluton w temperaturze pokojowej ma srebrzyste powierzchnie, które matowieją w ciągu kilku minut w kontakcie z powietrzem. Wykazuje cztery typowe stany utlenienia w roztworze wodnym oraz rzadszą piątą:
- Pu (III), jako jon Pu 3+ (lawendowy niebieski)
- Pu (IV), jako jon Pu 4+ (żółto-brązowy)
- Pu (V), jako jon PuO 2+ (blady róż)
- Pu (VI), jako jon PuO 22+ (pomarańczowo-różowy)
- Pu (VII), w postaci jonu PuO 53− (zielony; ten siedmiowartościowy jon jest rzadki).
Kompleks z plutonem na formalnym stopniu utlenienia +2, [K (2.2.2- kryptand )] [Pu II Cp ″ 3 ], gdzie Cp ″ = C 5 H 3 (SiMe 3 ) 2, również został opublikowany.
Kolor roztworów jonów plutonu zależy zarówno od stopnia utlenienia, jak i charakteru anionu kwasowego . To właśnie ta ostatnia wpływa na stopień skompleksowania plutonu.
Metaliczny pluton otrzymuje się w reakcji tetrafluorku plutonu PuF 4z barem , wapniem lub litem w 1200 ° C . Jest atakowany przez kwasy , tlen i parę wodną , ale nie przez zasady . Łatwo rozpuszcza się w kwasie solnym HCl, jodowodorowym HI i kwasie nadchlorowym HClO 4koncentraty. Stopiony pluton musi być przechowywany pod próżnią lub w atmosferze obojętnej, aby uniknąć reakcji z powietrzem. W temperaturze 135 ° C metaliczny pluton zapala się na wolnym powietrzu i eksploduje w obecności tetrachlorometanu CCl 4.
Pluton reaguje z węglem, tworząc węgliki plutonu Pu 3 C 2, PuC 1-δ, Pu 2 C 3i PuC 2 ; reaguje z azotem N 2z wytworzeniem PUN azotki oraz z krzemem , tworząc Pusi 2 krzemku ; reaguje z halogenami X 2, gdzie X może oznaczać fluor , chlor , brom i jod , dając trójhalogenki PuX 3. Z fluorem, oprócz trifluorku plutonu PuF 3obserwujemy również tetrafluorek plutonu PuF 4a także sześciofluorek plutonu PuF 6. Ponadto powstają tlenohalogenki PuOCl, PuOBr i PuOI.
W tygle używane z plutonu musi być w stanie wytrzymać same właściwości redukujących ten metal. Odpowiednie mogą być metale ogniotrwałe, takie jak tantal i wolfram oraz tlenki , borki , węgliki , azotki i krzemki . Topienie w elektrycznym piecu łukowym może umożliwić wytwarzanie małych wlewków metalicznego plutonu bez konieczności stosowania tygla.
Korozja
Czysty pluton wystawiony na działanie wilgoci, zarówno w powietrzu, jak i w argonie , w ciągu kilku minut pokrywa się matową warstwą mieszaniny tlenków i wodorków , która rozpada się, tworząc drobny lotny pył, którego wdychanie może stanowić poważne zagrożenie dla zdrowia . To jest powód, dla którego pluton jest przechowywany w komorach rękawicowych, które zapobiegają rozproszeniu atmosferycznemu tego pyłu.
Dokładniej, pluton wystawiony na suche powietrze zostaje pokryty warstwą dwutlenku plutonu PuO 2co zapewnia znakomitą pasywację metalu, zmniejszając postęp utleniania w materiale do zaledwie 20 pm · h -1 . Z drugiej strony obecność wilgoci wprowadza wodorki PuH x, Z 1,9 <x <3 , która katalizuje się korozji przez tlen O 2, natomiast wilgotność przy braku tlenu wprowadza tlenki pośrednie, takie jak półtoratlenek Pu 2 O 3które sprzyjają korozji wodorowej. Wreszcie wilgoć w obecności tlenu prowadzi do utleniania dwutlenku PuO 2 .z wytworzeniem wyższego tlenku PuO 2 + x na warstwie dwutlenku, który w wilgotnym powietrzu wydaje się sprzyjać korozji metalu.
Proszki plutonu, jego wodorków i niektórych tlenków, np. Pu 2 O 3są piroforyczne , tj. mogą zapalić się samoistnie w kontakcie z powietrzem w temperaturze pokojowej, dlatego są obsługiwane w suchej obojętnej atmosferze azotu N 2lub argon Ar. Stały pluton zapala się dopiero powyżej 400 °C . Pu 2 O 3samorzutnie nagrzewa się i zamienia w dwutlenek plutonu PuO 2, który jest stabilny w suchym powietrzu, ale reaguje na gorąco z parą wodną . Reakcje w grze byłyby następujące:
3 PuO 2+ Pu → 2 Pu 2 O 3 2 Pu 2 O 3+ O 2→ 4 PuO 2.Pluton reaguje również z wodorem H 2do tworzenia wodorków PuH x, przy 1,9 <x <3 :
2P + x H 2→ 2 PuH x.Wartość x zależy od ciśnienia cząstkowego wodoru i temperatury reakcji. Te wodorki, które są skrystalizowanymi ciałami stałymi w układzie sześciennym zorientowanym na twarz, są szybko utleniane przez powietrze i dysocjują na swoje elementy składowe po podgrzaniu w dynamicznej próżni, tj. przy ciągłym pompowaniu uwalnianego wodoru.
Bezpieczeństwo
Różne rodzaje ryzyka muszą być rozpatrywane w odniesieniu do przenoszenia plutonu, który zależy ściśle od izotopów zaangażowanych . Wypadków krytyczności wystąpić podczas manipulowania błędów prowadzących do utworzenia masy krytycznej plutonu i są podatne na uszkodzenia . Przyczynę syndromu promieniowania ostry . Radiowej toksyczność i toksyczność reprodukcyjnego wystąpić w wyniku absorpcji plutonu w ciele prowadząc do napromieniowaniu tkanki z promieniowaniem jonizującym może powodować mutacje genetyczne i wywoływać raka .
Najpopularniejszymi izotopami plutonu są przede wszystkim emitery α , napromieniowujące cząstki α o mocy od 4,9 do 5,5 MeV, które są łatwo zatrzymywane przez dowolną substancję stałą, w szczególności naskórek . Przez pluton 241 Emitowane promienie beta , bardziej przenikania niż promieniowanie alfa, ale tylko 5,2 keV .
Z chemicznego punktu widzenia pluton jest palny i samozapalny , więc stwarza zagrożenie pożarowe. Z drugiej strony jego toksyczność chemiczna nie jest szczególnie znacząca.
Krytyczność
Akumulacja plutonu w objętości zbliżonej do masy krytycznej prawdopodobnie doprowadzi do zainicjowania reakcji jądrowej, w której emitowana jest śmiertelna ilość neutronów i promieni γ . Ryzyko jest tym większe w przypadku plutonu, ponieważ masa krytyczna plutonu 239 wynosi na ogół tylko jedną trzecią masy uranu 235 . To ryzyko zwiększa się w roztworze ze względu na zmniejszającego efektu z wodorem w wodzie , która thermalises się neutronów .
Kilka wypadków krytyczności udziałem pluton został zgłoszony do XX th wieku , prowadząc do śmierci niektórych osób dotkniętych. Tak było na przykład w Narodowym Laboratorium Los Alamos w dniu 21 sierpnia 1945 r. podczas błędu w obsłudze cegieł z węglika wolframu używanych jako reflektory neutronów wokół kuli plutonu klasy wojskowej, co spowodowało 25 dni później śmierć Harry'ego Daghliana Jr. . , a następnie Manhattan Project badacz , w wyniku zespołu ostrego promieniowania po dawce on odebrany, szacuje się na 5,1 Sv . Dziewięć miesięcy później Louis Slotin również zmarł w Los Alamos w podobnym wypadku, gdy manipulował reflektorami berylowymi wokół tej samej kuli plutonu, zwanej rdzeniem demona . Również w Los Alamos doszło do innego wypadku w accidentgrudzień 1958, co kosztowało życie technika laboratoryjnego Cecila Kelleya podczas operacji oczyszczania plutonu, w wyniku tworzenia się masy krytycznej w mieszalniku. Inne tego typu wypadki miały miejsce na całym świecie, czy to w Stanach Zjednoczonych , Związku Radzieckim , Japonii czy innych krajach.
Radiotoksyczność
Syntetyczny pierwiastek wyprodukowany specjalnie ze względu na swoją radioaktywność , pluton jest najbardziej znany ze swojej radiotoksyczności . Wynika to z trzech rodzajów promieniowania jonizującego : promieni α ( cząstki α ), promieni β ( elektrony ) i promieni γ ( fotonów energetycznych). Ostra lub długotrwała ekspozycja na to promieniowanie stanowi zagrożenie dla zdrowia, które może objawiać się w kontekście ostrego zespołu popromiennego z mutacjami genetycznymi i nowotworami . Ryzyko wzrasta wraz z pochłoniętą dawką , mierzoną w szarościach (Gy), a dokładniej w funkcji dawki równoważnej , mierzonej w siwertach (Sv), która waży fizjologiczny wpływ różnych rodzajów otrzymanego promieniowania według ich zdolności do spowodować uszkodzenie napromieniowanej tkanki . Ta waga jest wprowadzana przez współczynnik dawki, zwykle mierzony w mikrosiwertach na bekerel (µSv / Bq):
| Izotop | pluton 238 | pluton 239 | pluton 240 | pluton 241 | pluton 242 |
|---|---|---|---|---|---|
| Aktywność masowa | ~ 630 GBq · g -1 | ~ 2,3 GBq · g -1 | ~ 8,5 GBq · g -1 | ~ 3700 GBq · g -1 | ~ 0,15 GBq · g -1 |
| Współczynnik dawki | 0,23 Sv · Bq -1 | 0,25 Sv · Bq -1 | 0,25 Sv · Bq -1 | 0,0048 Sv · Bq -1 | 0,24 Sv · Bq -1 |
W ten sposób promienie γ przechodzą przez wszystkie tkanki i wpływają na cały organizm, podczas gdy promienie β są mniej penetrujące, a promienie α nie przechodzą przez naskórek, ale są znacznie bardziej energetyczne (kilka megaelektronowoltów wobec kilku kiloelektronowoltów dla promieni β i γ) . Tak więc cząstki α są niebezpieczne, gdy są emitowane nawet w tkankach przez zaabsorbowany pluton. Głównym zagrożeniem jest wdychanie cząstek zawierających pluton, zwłaszcza w postaci dwutlenku plutonu PuO 2, który tworzy się szybko w kontakcie z powietrzem i który ma tendencję do rozpadu na drobny pył w obecności wilgoci. W ten sposób wykazano zwiększoną zachorowalność na raka płuc u pracowników sektora jądrowego. Ryzyko raka płuca wzrasta, gdy równoważna dawka wziewnego plutonu osiąga 400 mSv . Z drugiej strony, spożycie pochłania tylko 0,04% PuO 2spożyte. Zagrożenia dotyczą również kości, w których gromadzi się pluton, a także wątroby, w której jest skoncentrowany.
Nie wszystkie izotopy plutonu wykazują ten sam poziom radiotoksyczności. Pluton o jakości wojskowej, składający się w ponad 92% z plutonu 239 , wykazuje zatem dość umiarkowaną radiotoksyczność, ze względu na swoją masową aktywność mniejszą niż plutonu 240, a zwłaszcza plutonu 238 . Pluton-241 wykazuje aktywność tysiąc razy większa, emitując beta promienie , które są bardziej penetrujące niż promieniowanie alfa , aczkolwiek tysiąc razy mniej energii.
| Izotop | pluton 238 | pluton 239 | pluton 240 | pluton 241 | pluton 242 |
|---|---|---|---|---|---|
| Α promieniowanie | 5,5 MeV | 5,1 MeV | 5,2 MeV | < 1 keV | 4,9 MeV |
| Β promieniowanie | 11 keV | 6,7 keV | 11 keV | 5,2 keV | 8,7 keV |
| Γ promieniowanie | 1,8 keV | < 1 keV | 1,7 keV | < 1 keV | 1,4 keV |
Największą radiotoksyczność wykazuje pluton-238 , natomiast pluton-241 , którego stężenie w plutonie wzrasta z czasem, szybko produkt ameryku-241 , który emituje energię promieniowania γ, może znacząco narażać środowisko na promieniowanie.
Dawka śmiertelna spowodowana ostrym zespołem napromieniowania obserwowana w doświadczeniach in vivo jest rzędu 400 do 4000 µg kg- 1 w pojedynczej dawce, chroniczne zanieczyszczenie ma bardziej rozproszone efekty. Szacuje się zatem, że ilość rzędu dziesięciu miligramów powoduje śmierć osoby, która jednorazowo wdychała tlenki plutonu. Rzeczywiście, testy przeprowadzone na pawianach i psach prowadzą do oszacowania śmiertelności ludzi na 50% po 30 dniach przy 9 mg , po roku przy 0,9 mg i po 1000 dniach przy 0,4 mg .
Pojawienie się guzów płucnych wykazano u psów i szczurów po inhalacji słabo rozpuszczalnych związków, takich jak tlenki plutonu: wykazana zależność dawka-efekt obejmuje próg dla pojawienia się guzów dla dawki w płucach około 1 Gy . Ten próg pojawiania się guzów odpowiadałby u ludzi złogu w płucach około 200 kBq lub 87 μg ) 239 PuO 2 ..
Palność
Pluton stanowi zagrożenie pożarowe, zwłaszcza gdy jest w postaci drobno rozdrobnionego proszku. W obecności wilgoci tworzy na swojej powierzchni wodorki, które są piroforyczne i mogą się zapalić w temperaturze pokojowej. Ryzyko jest realne i zmaterializowało się w 1969 r. w wyniku dużego pożaru plutonu w krajowym laboratorium Rocky Flats . Wzrost objętości wynikający z utlenienia plutonu może osiągnąć 70% i rozbić zbiorniki. Radioaktywność tego palnego metalu stanowi dodatkowe zagrożenie.
Tlenek magnezu MgO prawdopodobnie najskuteczniejszym substancja gaszenia ognia plutonu: stygnięcia metalu, służących jako radiator podczas przycinania dostarczać tlen spalania . Aby zapobiec ryzyku pożaru, zaleca się obsługę plutonu w obojętnej, suchej atmosferze.
Toksykologia
Pluton wykazuje toksyczność metali ciężkich w taki sam sposób, jak na przykład uran , ale jest mniej udokumentowany niż ten drugi, a badania nie stawiają toksyczności chemicznej jako głównego zagrożenia związanego z plutonem. Kilka populacji narażonych na pył plutonowy było ściśle monitorowanych w celu oceny wpływu skażenia plutonem na ich zdrowie, takich jak ludzie mieszkający w pobliżu miejsc eksperymentów jądrowych w atmosferze, gdy byli upoważnieni, ludzie pracujący w instalacjach jądrowych, osoby, które przeżyły bombardowanie atomowe Nagasaki nawet pacjentom „w terminalnej fazie” śmiertelnych chorób, którym wstrzykiwano pluton w latach 1945-1946 w celu obserwowania jego metabolizmu w organizmie człowieka . Badania te nie wykazują toksyczności zwykle szczególnie wysokiej dla plutonu, ze słynnymi przykładami przypadków, takich jak przypadek Alberta Stevensa , cytowanego przez Bernarda Cohena (w) , który dożył późnego wieku po zastrzykach z plutonu. Kilkudziesięciu badaczy z Narodowego Laboratorium Los Alamos również wdychało znaczne ilości pyłu plutonu w latach 40. bez rozwoju raka płuc.
Pewna antynuklearna retoryka twierdzi, że „spożycie nawet jednej milionowej grama jest śmiertelne”, czego nie potwierdza istniejąca literatura. Dane epidemiologiczne członków „klubu UPPU ”, to znaczy 26 osób, które pracowały w narodowym laboratorium Los Alamos nad plutonem i które spożyły go do tego stopnia, że były obserwowane w moczu, pokazują na przykładzie śmiertelność i zachorowalność na raka niższa od średniej.
Twierdzenie, że „wystarczyłoby tylko kilkaset gramów plutonu równomiernie rozłożonego na ziemi, aby wymazać całe ludzkie życie” również nie jest zgodne z dostępnymi danymi. Szacuje się, że rozproszenie masy rzędu jednego kilograma na obszarze kilkuset kilometrów kwadratowych (czyli w promieniu około 10 km ) prowadzi do skażenia poniżej jednej setnej mikrograma na metr kwadratowy , więc kilkaset gramów równomiernie rozłożonych na powierzchni Ziemi byłoby znacznie poniżej jakiejkolwiek wykrywalnej ilości.
Konieczne jest również, aby odróżnić radiotoksyczności z plutonu 238 , co jest szczególnie wysoka, od tego plutonu 239 używanych przez przemysł jądrowy, którego wojska i spontaniczny radioaktywność jest znacznie mniej. Te dwa izotopy są produkowane w bardzo różnych ilościach, przez oddzielne obwody i do niepowiązanych zastosowań: pluton 238 jest produkowany w ilości kilku kilogramów głównie jako pokładowe źródło energii dla radioizotopowego generatora termoelektrycznego , podczas gdy pluton-239 jest produkowany w tempie kilku ton, aby wykorzystać jego naturę rozszczepialnego izotopu w reaktorach jądrowych lub broni jądrowej.
Toksydynamika
U ludzi wchłonięty pluton jest transportowany przez transferyny i gromadzony we krwi przez ferrytynę, ostatecznie gromadząc się głównie w kościach , także w wątrobie oraz, w mniejszym stopniu, w płucach . Pozostaje w ludzkim ciele z biologicznym okresem półtrwania około 50 lat. Powszechnym sposobem ograniczenia skutków jest wstrzyknięcie kompleksu kwasu dietylenotriaminopentaoctowego ( DTPA , czasami zwanego „kwasem pentetowym”) z wapniem lub cynkiem w ciągu 24 godzin od zanieczyszczenia, co ogranicza wiązanie plutonu, a także ameryku i kurium . Można również stosować inne chelatory , takie jak enterobaktyna i deferoksamina , niektóre o lepszej skuteczności niż DTPA, takie jak 3,4,3-LIHOPO lub DFO-HOPO (deferoksamina-hydroksypirydynon).
Szacuje się, że u ludzi 10% plutonu, który przekroczył barierę jelitową lub płucną, opuszcza organizm (w moczu i kale). Pozostała część po przejściu przez krew jest utrwalana w połowie w wątrobie, a w połowie w szkielecie , gdzie pozostaje przez bardzo długi czas, a częściowo na całe życie (amerykański DOE szacuje, że okres półtrwania w narządzie wynosi odpowiednio 20 i 50 lat). dla wątroby i kości, według uproszczonych modeli, które nie uwzględniają redystrybucji pośrednich (w przypadku złamań i/lub menopauzy (por. odwapnienie ) oraz podczas normalnego recyklingu kości itp.). poziom nagromadzony w wątrobie i szkielecie zależy również od wieku osobnika (absorpcja w wątrobie wzrasta wraz z wiekiem) i w rzeczywistości pluton jest najpierw utrwalany na powierzchni korowej i beleczkowej kości, a następnie ulega powolnej redystrybucji. objętość mineralna kości.
Aplikacje
Wojskowy
Pluton-239 jest rozszczepialny izotop kluczem do realizacji broni jądrowej ze względu na jego względnej łatwości wdrożenia i stosunkowo wysokiej dostępności. Możliwe jest zmniejszenie masy krytycznej niezbędnej do wybuchu poprzez otoczenie rdzenia plutonowego reflektorami neutronowymi, które pełnią podwójną rolę polegającą na zwiększeniu przepływu neutronów termicznych w rdzeniu i opóźnieniu rozszerzalności cieplnej tych ostatnich, w celu przedłużenia łańcucha reakcji i zwiększyć siłę wybuchu jądrowego .
Masa 10 kg z plutonu 239 , bez odbłyśnika jest na ogół wystarczające do osiągnięcia krytycznego; tę masę można zmniejszyć o połowę dzięki zoptymalizowanemu projektowi. To około jednej trzeciej masy krytycznej uranu 235 .
Bomba Fat Man spadła na Nagasaki przez Stany Zjednoczone 9 sierpnia 1945 stosując obciążenie 6,4 kg od stopu plutonu-galu 239 Pu - 240 Pu - Ga 96: 1: 3 wokół źródła neutronów He inicjacja Be - 210 Po wszystkim otoczona soczewek wybuchowych prasując plutonu znacznie zwiększa jego gęstość, a tym samym siła wybuchu, które osiągnęły równoważnik 20000 t w TNT . Teoretycznie możliwe jest zmniejszenie masy plutonu wymaganej w broni jądrowej w celu osiągnięcia krytyczności do mniej niż 4 kg przy wystarczająco dopracowanej konstrukcji.
Cywile
Zużytego paliwa jądrowego z reaktorów wodnych konwencjonalnych zawiera mieszaninę izotopów 238 Pu , 239 Pu , 240 Pu i 242 Pu . Ta mieszanina nie jest wystarczająco wzbogacona w pluton 239 , aby umożliwić produkcję broni jądrowej , ale może być przetworzona na paliwo MOX . W liczba neutronów niezamierzonym podczas reakcji jądrowej zwiększa ilość plutonu 240 i plutonu 242 podczas pluton naświetlano w reaktorze neutronów termicznych tak, że po pierwszym cyklu, pluton mogą być stosowane więcej niż szybko reaktorów neutronów . Jeśli takie reaktory nie są dostępne, co zwykle ma miejsce, nadmiar plutonu jest zwykle usuwany, tworząc długożyciowe odpady promieniotwórcze . Chęć zmniejszenia ilości takich odpadów i ich odzysku skłoniła do stworzenia większej liczby reaktorów na neutrony prędkie.
Najpopularniejszy proces chemiczny, znany jako PUREX , umożliwia ponowne przetwarzanie zużytego paliwa jądrowego poprzez ekstrakcję zawartego w nim plutonu i uranu w celu wytworzenia mieszaniny tlenków zwanej MOX , zasadniczo dwutlenku uranu UO 2i dwutlenek plutonu PuO 2, który może być ponownie użyty w reaktorach jądrowych. Do tej mieszaniny można dodać pluton klasy wojskowej, aby zwiększyć jej wydajność energetyczną. MOX może być stosowany w reaktorach na lekką wodę i zawiera około 60 kg na tonę paliwa; po czterech latach użytkowania zużywa się trzy czwarte plutonu. Te reaktory hodowca mają na celu optymalizację wykorzystania neutronów wytwarzanych podczas reakcji jądrowej stosując je wytworzyć, z " płodnych węgla , więcej materiału rozszczepialnego one zużywają.
MOX jest używany od lat 80 - tych , zwłaszcza w Europie . Stany Zjednoczone i Rosja podpisały wwrzesień 2000, porozumienie o zarządzaniu i przetwarzaniu plutonu ( PMDA ), na mocy którego zamierzają wycofać 34 tony plutonu przeznaczonego do celów wojskowych; amerykański Departament Energii planuje się recyklingowi tę masę plutonu w MOX przed końcem 2019 roku.
MOX zwiększa całkowitą efektywność energetyczną. Pręt paliwowy jądrowy jest ponownie przetwarzany po trzech latach użytkowania w celu wydobycia odpadów, które następnie stanowią około 3% całkowitej masy tych prętów. Izotopy uranu i plutonu wytworzone podczas tych trzech lat pracy pozostają w pręcie paliwowym, który wraca do reaktora do wykorzystania. Obecność galu do 1% wagowego w plutonie klasy wojskowej może zakłócać długotrwałe użytkowanie tego materiału w reaktorze na lekką wodę.
Największe deklarowane zakłady recyklingu plutonu to jednostki B205 (en) i THORP (en) w Sellafield w Wielkiej Brytanii ; zakład przerobu w La Hague , w Francji ; elektrownia jądrowa Rokkasho w Japonii ; oraz kompleks nuklearny Majak w Rosji ; istnieją inne strony deklarowane jako mniejsze, na przykład w Indiach i Pakistanie .
Przestrzeń
Pluton-238 ma okres półtrwania o 87.74 lat. Emituje dużą ilość energii cieplnej, której towarzyszą słabe strumienie neutronów i fotonów energii gamma . Jeden kilogram tego izotopu może wytworzyć moc cieplną około 570 W . Emituje głównie wysokoenergetyczne cząstki α, które są słabo penetrujące, dlatego wymaga jedynie osłony przed światłem. Wystarczy kartka papieru, aby zatrzymać promienie α.
Te cechy sprawiają, że ten izotop plutonu jest szczególnie interesującym źródłem ciepła do zastosowań pokładowych, które muszą działać bez możliwości bezpośredniej konserwacji przez całe życie człowieka. Był więc wykorzystywany jako źródło ciepła w generatorach termicznych radioizotopów ( RTG ) i grzejnikach radioizotopowych ( RHU ), takich jak sondy Cassini , Voyager , Galileo i New Horizons oraz łazik Curiosity on Mars Science Laboratory .
Bliźniacze sondy Voyager zostały wystrzelone w 1977 roku, każda ze źródłem plutonu uwalniającym 500 W mocy . Ponad 30 lat później te źródła energii nadal uwalniały moc 300 W, umożliwiając ograniczone działanie sond. Starsza wersja tej technologii zasilała pięć pakietów Apollo Lunar Surface Experiments, począwszy od Apollo 12 w 1969 roku.
Pluton 238 został również z powodzeniem wykorzystany do zasilania rozruszników serca, aby uniknąć powtarzających się operacji w celu zastąpienia źródła zasilania. Od tego czasu pluton-238 został w dużej mierze zastąpiony przez baterie litowe , ale w 2003 roku nadal pozostawał w Stanach Zjednoczonych wśród 50-100 pacjentów wyposażonych w pluton-238 zasilany rozrusznikami serca .
bezpieczeństwo
Ponieważ pluton może być wykorzystywany do celów wojskowych lub terrorystycznych, jest przedmiotem wielu międzynarodowych tekstów i konwencji mających na celu zapobieganie jego rozprzestrzenianiu się . Pluton poddany recyklingowi ze zużytego paliwa jądrowego stwarza ograniczone ryzyko proliferacji ze względu na wysokie zanieczyszczenie nierozszczepialnymi izotopami, takimi jak pluton 240 i pluton 242 , których unieszkodliwienie jest niewykonalne.
Reaktor działający z bardzo niskim stopniem wypalenia wytwarza niewiele z tych niechcianych izotopów, a zatem pozostawia materiał jądrowy potencjalnie użyteczny do celów wojskowych. Uważa się, że pluton klasy wojskowej zawiera co najmniej 92% plutonu 239 , ale technicznie możliwe jest zdetonowanie bomby jądrowej małej mocy z plutonu zawierającego tylko 85% plutonu 239 . Pluton wytwarzany w reaktorze na wodę lekką o normalnej szybkości spalania zazwyczaj zawiera mniej niż 60% plutonu 239 , 10% rozszczepialnego plutonu 241 i do 30% niepożądanych izotopów plutonu 240 i 242 . Nie wiadomo, czy możliwe jest zdetonowanie urządzenia jądrowego wykonanego z takiego materiału, jednak takie urządzenie mogłoby prawdopodobnie rozprzestrzenić materiał radioaktywny na dużym obszarze.
Międzynarodowa Agencja Energii Atomowej klasyfikuje zatem wszystkie izotopy plutonu, czy są one rozszczepialny lub nie, jako materiał bezpośrednio użytkowej do celów jądrowych, to znaczy jako materiał jądrowy, który może być stosowany do produkcji materiałów wybuchowych jądrowych bez transmutacji lub dodatkowego wzbogacenia . We Francji, pluton jest materiał jądrowy, którego zatrzymanie jest uregulowane w rozdziale III tego kodeksu Obrony .
Pochodzenie
Pluton jest pierwiastkiem chemicznym bardzo rzadkim w przyrodzie i prawie wyłącznie produkowanym przez ludzi od 1940 roku do dnia dzisiejszego. Jednakże od 4 do 30 kilogramy z plutonu 239 będzie wytwarzany w każdym roku na ziemi przez alfa radioaktywności z uranu lżejsze elementy, a także pod wpływem promieniowania kosmicznego . Jest to drugi z odkrytych transuranów .
Izotop 238 Pu został wyprodukowany w 1940 roku przez bombardowanie docelową uranu przez deuter w cyklotronie w Berkeley . Podczas Projektu Manhattan , pluton 239 miał kryptonim 49 , tym „4” jest ostatnią cyfrę 94 (liczba atomowa) i „9” ostatnią cyfrę 239, masę atomową izotopu używany. O bombie , 239 Pu .
Nie ma już plutonu w wykrywalnych ilościach sięgających pierwotnej nukleosyntezy . Jednak starsze publikacje donoszą o obserwacjach naturalnego plutonu 244 . Ślady plutonu-239 znajdujemy również w naturalnych rudach uranu (podobnie jak w neptunie ), gdzie powstaje on w wyniku napromieniowania uranu przez bardzo niską prędkość neutronów powstałych w wyniku spontanicznego rozpadu uranu.
Został wyprodukowany masowo (i nadal występuje w śladowych ilościach) jako 239 Pu w szczególnych strukturach geologicznych , gdzie uran był naturalnie skoncentrowany w procesach geologicznych około 2 miliardów lat temu, osiągając krytyczność wystarczającą do wygenerowania naturalnej reakcji jądrowej . Tempo jego powstawania w rudzie uranu zostało zatem przyspieszone przez reakcje jądrowe, które były możliwe w wyniku naturalnej awarii krytycznej . Tak jest w przypadku naturalnego reaktora jądrowego w Okle .
Produkcja
pluton 238
W elektrowniach jądrowych pluton 238 powstaje obok plutonu 239 , w łańcuchu transformacji rozpoczynającym się od rozszczepialnego uranu 235 .
- Uran 235, który wychwytuje neutron termiczny, może się stabilizować emitując promieniowanie γ w 16% przypadków. Następnie tworzy atom 236 U , stosunkowo stabilny (okres półtrwania 23 miliony lat).
- Drugie wychwytywanie neutronów przekształca je w 237 U (dla przypomnienia, jądra 238 U mogą również ulec reakcji (n, 2n), która przekształca je w 237 U poprzez utratę neutronu). Uran 237 jest niestabilny z okresem półtrwania 6,75 dnia i jest przekształcany przez emisję β w stosunkowo stabilny neptun 237 (okres półtrwania 2,2 miliona lat).
- Trzecie wychwytywanie neutronów przekształca jądro w neptun 238, niestabilny z okresem półtrwania wynoszącym 2,1 dnia, który przekształca się w pluton 238 przez emisję β .
Pluton 238, z okresem półtrwania 86,41 lat, jest bardzo silnym emiterem promieniowania α . Ze względu na wysoką aktywność masową alfa i gamma jest wykorzystywany jako źródło neutronów (w wyniku „reakcji alfa” z elementami lekkimi), jako źródło ciepła oraz jako źródło energii elektrycznej ( poprzez zamianę ciepła na energię elektryczną). ). Zastosowania 238 Pu do wytwarzania energii elektrycznej ograniczają się do zastosowań kosmicznych, a w przeszłości do niektórych rozruszników serca.
Pluton 238 wytwarza się z napromieniowania neutronem neptunu 237, niewielkiego aktynowca odzyskanego podczas ponownego przetwarzania lub z napromieniowania ameryku, w reaktorze. W obu przypadkach, w celu wyekstrahowania plutonu 238 z celów, poddaje się je obróbce chemicznej obejmującej rozpuszczanie azotu.
Istnieje tylko około 700 g / t, w neptun 237 w paliwie reaktora wodę lekką spędzony 3 lata, i musi być selektywnie ekstrakcji.
pluton 239
Napromieniowanie uranu 238 w reaktorach jądrowych generuje pluton 239 przez wychwytywanie neutronów . Po pierwsze, atom uranu 238 wychwytuje neutron i przejściowo przekształca się w uran 239 . Ta reakcja wychwytywania jest łatwiejsza w przypadku neutronów prędkich niż neutronów termicznych, ale występuje w obu przypadkach.
Utworzony uran 239 jest bardzo niestabilny. Przekształca się szybko (z okresem półtrwania 23,5 minuty) w neptun pod wpływem radioaktywności β:
Neptun 239 jest niestabilny, a to z kolei przechodzi P- próchnicy (z okresem półtrwania 2,36 dni), który zamienia się w pluton-239 względnie stabilny (okres półtrwania od 24000 lat).
Pluton 239 jest rozszczepialny , a zatem może przyczynić się do reakcji łańcuchowej w reaktorze . Dlatego też, dla bilansu energetycznego reaktora jądrowego , potencjał energetyczny uranu obecnego w reaktorze obejmuje nie tylko ten początkowo obecny uran 235, ale również ten płodny uran 238, który zostanie przetransmutowany w plutonie.
Poddany działaniu strumienia neutronów w reaktorze, pluton 239 może również wychwytywać neutron bez ulegania rozszczepieniu. Ponieważ paliwo podlega coraz dłuższym okresom napromieniania, w ten sposób gromadzą się wyższe izotopy w wyniku absorpcji neutronów przez pluton-239 i jego produkty. Tworzą się w ten sposób izotopy 240 Pu, 241 Pu, 242 Pu, aż do nietrwałego 243 Pu, który rozpada się na ameryk243 .
Izotop będący przedmiotem zainteresowania ze względu na jego rozszczepialny charakter to 239 Pu , stosunkowo stabilny w skali człowieka (24 000 lat).
Szybkość produkcji izotopu zależy od dostępności jego prekursora, który musiał mieć czas na akumulację.
W nowym paliwie 239 Pu tworzy się zatem liniowo w funkcji czasu, proporcja 240 Pu wzrasta zgodnie z kwadratem czasu (w t 2 ), a 241 Pu zgodnie z sześciennym prawem czasu (w t 3 ) i tak dalej.
Tak więc, gdy do produkcji „plutonu wojskowego” wykorzystywany jest konkretny reaktor, paliwo używane do produkcji plutonu, jak również tarcze i ewentualnie osłona, są wydobywane po krótkim postoju (kilka tygodni). reaktora, aby zapewnić, że pluton 239 jest tak czysty, jak to możliwe.
Z drugiej strony, w przypadku zastosowań cywilnych, krótkie napromieniowanie nie pobiera całej energii, którą może wytworzyć paliwo. Paliwo jest więc usuwane z reaktorów wytwórczych dopiero po znacznie dłuższym pobycie (3 lub 4 lata).
W pierwszym przybliżeniu, reaktor daje zazwyczaj 0,8 atomów 239 Pu dla każdego rozszczepienia 235 U albo jeden gram plutonu na dzień na M W mocy cieplnej (reaktorów wodnych wytwarzają mniej niż grafit gazu). Na przykład we Francji reaktory jądrowe produkują rocznie około 11 ton plutonu.
pluton 240
240 Pu jest po prostu żyzna i ma radioaktywność „tylko” cztery razy wyższy niż 239 Pu (z półtrwania 6500 lat).
pluton 241
241 Pu jest rozszczepialny ale wysoce radioaktywny (okres półtrwania 14,29 lat).
Ponadto rozpada się wytwarzając ameryk 241 absorbujący neutrony , który poprzez możliwą akumulację zmniejsza skuteczność wojskowych lub cywilnych urządzeń jądrowych.
pluton 242
242 Pu ma okres znacznie dłuższy niż w poprzednich latach (373,000). Nie jest rozszczepialny w neutronach termicznych. Jego przekrój jest znacznie mniejszy niż innych izotopów; sukcesywny recykling plutonu w reaktorze ma zatem tendencję do gromadzenia plutonu w tej bardzo niepłodnej postaci.
pluton 243
243 PU niestabilny (okres półtrwania wynosi mniej niż 5 godzin), i rozpada się ameryk 243 .
pluton 244
Pluton-244 , najbardziej stabilnym izotopem z okresem półtrwania wynoszącym 80 milionów lat, nie tworzy się w reaktorach nuklearnych. Rzeczywiście, kolejne wychwyty neutronów, począwszy od 239 uranu, prowadzą do 243 Pu, z bardzo niskim okresem półtrwania (rzędu pięciu godzin). Nawet w reaktorach „wysokich strumieni” 243 Pu zmienia się szybko do 243 Am, bez czasu na wychwycenie dodatkowego neutronu w celu utworzenia 244 Pu.
Z drugiej strony, większe strumienie neutronów umożliwiają to tworzenie. Jest syntetyzowany podczas wybuchów jądrowych lub w gwiezdnej nukleosyntezie podczas wybuchu supernowej . Tak więc w 1952 roku wybuch pierwszej amerykańskiej bomby termojądrowej (test Ivy Mike'a ) wytworzył dwa jeszcze nieznane pierwiastki promieniotwórcze : pluton 244 ( 244 Pu) i pluton 246 ( 246 Pu). Te śladowe ilości od 244 Pu w środowisku na ogół przypisać atmosferycznych badań jądrowych, a także pozostałości 244 istotną PU.
Po blisko 70 latach stale rosnącej światowej produkcji, deklarowane zapasy plutonu osiągnęły na koniec 2013 roku łącznie 500 ton, z czego 52% pochodzenia cywilnego i 48% pochodzenia wojskowego. Zadeklarowane zapasy są dystrybuowane głównie między 5 krajów:
- Rosja : 178 ton lub 35,6%
- Wielka Brytania : 107,2 tony lub 21,4%
- Stany Zjednoczone : 88,3 tony lub 17,7%
- Francja : 66,2 tony lub 13,2%
- Japonia : 47,1 tony lub 9,4%
- Reszta świata: 13 ton lub 3%
Uwagi
- W temperaturze przejścia fazowego.
- odpowiednia Gęstość podana jako 0 ° C .
- Jon PuO 2+ jest niestabilny w roztworze i rozpada się na Pu 4+ i PuO 22+ ; Pu 4+ następnie utlenia PuO 2+ pozostałość w PuO 22+ stając się sobą Pu 3+ . Roztwór PuO 2+ dlatego z czasem staje się mieszaniną PuO 22+ i Pu 3+ . Jon UO 2+ jest niestabilny z tego samego powodu.
- W języku angielskim UPPU mówi Ci sikasz Pu , co oznacza „ odlewasz pluton”.
- Skład izotopowy plutonu w zużytym paliwie jądrowym jest rzędu 58% z 239 Pu , 24% z 240 Pu , 11% z 241 Pu , 5% z 242 Pu i 2% z 238 Pu .
- Poważny wyciek plutonu i uranu miał miejsce 19 kwietnia 2005 r. w zakładzie THORP (w) po przerwie w spawaniu w zbiornikach regeneracyjnych. Utracono 200 kg plutonu, a 83 000 l materiału radioaktywnego pochodziło ze zbiornika żelbetowego przeznaczonego do zbierania wszelkich strat. Ten wyciek nastąpił po pęknięciu rury, które nie zostało wykryte, ponieważ technicy przez kilka miesięcy ignorowali wskaźniki ostrzegawcze na ten temat, które wskazywały na utratę masy w zbiorniku, co oznaczało nieszczelność. Obawiając się krytycznego wypadku , władze bezpieczeństwa tymczasowo zamknęły jedną z dwóch bliźniaczych instalacji.
- Stany Zjednoczone zdetonowały w ten sposób urządzenie jądrowe w 1962 r. ze zużytego paliwa z brytyjskiego reaktora Magnox , najprawdopodobniej elektrowni jądrowej Chapelcross , typu Calder Hall ; skład izotopowy tego plutonu nie został podany do wiadomości publicznej, ale z pewnością nie przekracza 85% plutonu 239 .
Uwagi i referencje
- (w) Beatriz Cordero Verónica Gómez, Ana E. Platero-Prats, Marc Revés Jorge Echeverría, Eduard Cremades, Flavia i Santiago Barragan Alvarez , „ Kowalentne promienie ponownie ” , Dalton Transactions ,2008, s. 2832 - 2838 ( DOI 10.1039 / b801115j )
- (w) David R. Lide, CRC Handbook of Chemistry and Physics , CRC,2009, 89 th ed. , s. 10-203
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 th ed. , 2804 s. , Oprawa twarda ( ISBN 978-1-420-09084-0 )
- arkusz IFA GESTIS
- Daniel Calais i André Chesné, „ Plutonium ” na stronie universalis.fr (konsultacja 8 czerwca 2021 r . ) .
- (w) David L. Clark, Gordon Jarvinen, Cynthia Kowalczyk, Jim Rubin i Mary Ann Stroud, „ Przetwarzanie kwasu azotowego ” [PDF] , Actinide Research Quarterly – 3. kwartał 2008 r. w Actinide Research Quarterly (ARQ) na stronie Los Alamos Laboratorium Krajowe , Instytut Badań Transaktynowych Seaborg,październik 2008(dostęp 7 sierpnia 2017 r. ) ,s. 10
-
(w) David L. Clark, Gordon Jarvinen, Cynthia Kowalczyk, Jim Rubin i Mary Ann Stroud, „ Przetwarzanie kwasu azotowego ” [PDF] , Actinide Research Quarterly – 3. kwartał 2008 r. w Actinide Research Quarterly (ARQ) na stronie Los Alamos Laboratorium Krajowe , Instytut Badań Transaktynowych Seaborg,
październik 2008(dostęp 5 sierpnia 2017 r. ) ,s. 6:
" Podczas gdy dwutlenek plutonu jest zwykle oliwkowozielony, próbki mogą mieć różne kolory. Powszechnie uważa się, że kolor jest funkcją czystości chemicznej, stechiometrii, wielkości cząstek i sposobu przygotowania, chociaż kolor wynikający z danej metody przygotowania nie zawsze jest powtarzalny. "
- (i) A. Boring Michael James L. Smith , „ pluton skróconego materii Physics - badanie teorii i eksperymentu ” , Los Alamos, Science , n O 26, 2000, s. 90-127 ( czytaj online )
- (i) Siegfried S. Hecker , „ plutonu i jego stopów - z atomami do mikrostruktury ” , Los Alamos, Science , n O 26, 2000, s. 290-335 ( czytaj online )
- (w) Siegfried S. Hecker, i Michael F. Stevensa , " mechaniczne zachowanie plutonu i jego stopy " , Los Alamos Science , n O 26, 2000, s. 336-355 ( czytaj online )
- (en) William N. Miner Fred W. Schonfeld "pluton" Encyklopedia pierwiastków , 1968, Clifford A. Hampel, Reinhold Book Corporation, New York, pp. 540–546
- (w) Siegfried S. Hecker , " pluton, element w sprzeczności ze sobą " , Los Alamos, Science , n O 26, 2000, s. 16-23 ( czytaj online )
- (w) Siegfried S. Hecker i Joseph C. Martz , " starzenie plutonu i jego stopy " , Los Alamos, Science , n O 26, 2000, s. 238-243 ( czytaj online )
- (w) Dana C. Christensen , " The Future Role of Technology plutonu " , Los Alamos, Science , n O 23, 1995, s. 168-173 ( czytaj online )
- (w) „ Wykres nuklidów ” na Narodowym Centrum Danych Jądrowych (dostęp 6 sierpnia 2017 r . ) .
- (i) David L. Heiserman "Element 94: pluton" Badając pierwiastków i ich związków , 1992 Tab Books, New York (Nowy Jork), str. 337–340 . ( ISBN 0-8306-3018-X ) .
- (w) Isaac Asimov, Reaktory jądrowe , Understanding Physics 1988, Barnes & Noble Publishing, Nowy Jork. ( ISBN 0-88029-251-2 ) .
- (w) Samuel Glasstone i Leslie M. Redman, „ Wprowadzenie do broni jądrowej ” [PDF] na web.archive.org , Komisja Energii Atomowej, Czerwiec 1972(dostęp 7 sierpnia 2017 r . ) .
- (w) FG Gosling (1999). Projekt Manhattan: Making the Atomic Bomb " Archive copy" (wersja archiwum internetowego z 24 lutego 2009 ) [PDF] , 1999, Departament Energii Stanów Zjednoczonych, Oak Ridge. ( ISBN 0-7881-7880-6 )
- (w) „ Pluton: 50 lat ” [PDF] na web.archive.org , Departament Energii USA, 1996(dostęp 7 sierpnia 2017 r . ) .
- (w) JW Kennedy, GT Seaborg, E. Segre i AC Wahl , " Właściwości 94 (239) " , Physical Review , tom. 70, Bez kości 7-8, Październik 1946, s. 555-556 ( DOI 10.1103 / PhysRev.70.555 , Bibcode 1946PhRv... 70..555K , czytaj online )
- (w) Louis A. Turner , „ Energia atomowa z U- 238 ” , „ Physical Review” , tom. 69 Bez kości 7-8, Kwiecień 1946, s. 366-366 ( DOI 10.1103/PhysRev.69.366 , Bibcode 1946PhRv... 69..366T , czytaj online )
- (w) David L. Heiserman , Exploring Chemical Elements and Their Compounds , Nowy Jork (NY), TAB Books 1992, 1 st ed. , 376 s. ( ISBN 978-0-8306-3018-9 , LCCN 91017687 ) , „Element 94: pluton” , s. 337–340
- (w) Richard Rhodes , The Making of the Atomic Bomb , New York, Simon & Schuster , 1986, 1 st ed. , 886 s. , kieszeń ( ISBN 978-0-671-65719-2 , LCCN 86015445 ) , s. 659–660 Leona Marshall: „Kiedy bierzesz sztabkę do ręki, czujesz, że jest gorąca jak żywy królik”.
- K. Beaugelin-Seiller, D. Boust, P. Germain, S. Roussel-Debet i C. Colle, „ Plutonium and environment ” [PDF] , Radionuclide sheet , http://www.irsn.fr/ , Institut ochrona radiologiczna i bezpieczeństwo jądrowe , 1 st wrzesień 2004(dostęp 13 sierpnia 2017 r . ) .
- (w) " Czy pluton klasy reaktorowej może produkować broń jądrową? » , http://www.cnfc.or.jp/ , Council for Nuclear Fuel Cycle Institute for Energy Economics Japan, maj 2001(dostęp 7 sierpnia 2017 r . ) .
- (w) „ Plutonium Radioactive ” [html] , National Institutes of Health (dostęp 5 sierpnia 2017 ) .
- (w) „ Przejścia faz kryształów plutonu ” , GlobalSecurity.org
- (w) Kenton James Moody, Ian D. Hutcheon i Patrick M. Grant, Nuclear forensic analysis , 2005, CRC Press, s. 169 . ( ISBN 0-8493-1513-1 )
- (w) David G. Kolman i Lisa P. Colletti , „ Zachowanie korozyjne w środowisku wodnym plutonu, metalu i stopów wystawionych na działanie roztworów wodnych azotanu i chlorku galu ” , Journal of the Electrochemical Society , tom. 155 n O 12, 7 października 2008, C565-C570 ( DOI 10.1149/1.2976352 , przeczytaj online )
- (w) DG Hurst, AG Ward, Canadian Research Reactors [PDF] , 1956, Atomic Energy of Canada Limited, Ottawa.
- (en) AE Kay, pluton 1965 , 1965, Taylor & Francis.
- (w) Gerard L. Hofman, RG Pahl, EC Lahm i DL Porter , „ Pęcznienie paliwa U-Pu-Zr ” , Transakcje metalurgiczne A , tom. 21 N O 2 Luty 1990, s. 517-528 ( DOI 10.1007/BF02671924 , Bibcode 1990MTA.... 21..517H , czytaj online )
- (w) RG Pahl, DL Porter EC Lahm i GL Hoffman , „ Badania eksperymentalne sworzni paliwowych reaktora prędkiego U-Pu-Zr w eksperymentalnym reaktorze wtórnym II ” , Metallurgical Transactions A , tom. 21, n o 7, lipiec 1990, s. 1863-1870 ( DOI 10.1007/BF02647233 , Bibcode 1990MTA.... 21.1863 P , przeczytaj online )
- (w), David L. Clark , " Chemical złożoności plutonu " , Los Alamos Science , n O 26, 2000, s. 364-381 ( czytaj online )
- (w) David R. Lide, Handbook of Chemistry and Physics , 2006, CRC Press, Taylor & Francis Grupa 87 th Edition, Boca Raton. ( ISBN 0-8493-0487-3 )
- (w) William J. Crooks, „ Moduł szkoleniowy inżynierii bezpieczeństwa o krytyczności jądrowej 10 – Bezpieczeństwo krytyczne w operacjach przetwarzania materiałów, część 1 ” [PDF] 2002.
- (w) Cory J. Windorff Guo P. Chen, Justin N. Cross, William J. Evans, Filipp Furche, Andrew J. Gaunt, Michael T. Janicke, Stosh A. Kozimor i Brian L. Scott , „ Identyfikacja Formalny stan utlenienia plutonu +2: synteza i charakterystyka {Pu II [C 5 H 3 (SiMe 3 ) 2 ] 3 } - ”, Journal of the American Chemical Society ,tom. 139n O 1122 marca 2017 r., s. 3970-3973 ( PMID 28235179 , DOI 10.1021/jacs.7b00706 , czytaj online )
- (w) George Matlack, Primer Plutonium: An Introduction to Its Plutonium Chemistry and Radioactivity , Los Alamos National Laboratory, styczeń 2003.
- (w) Mary Eagleson, Concise Encyclopedia Chemistry 1994, Walter de Gruyter, Berlin, s. 840 . ( ISBN 978-3-11-011451-5 ) .
- (en) John Emsley, (2001). „Plutonium”, Nature's Building Blocks: An A–Z Guide to the Elements , 2001, Oxford University Press, Oxford (Wielka Brytania). ( ISBN 0-19-850340-7 ) .
- (w), John M. Haschke, Thomas H. Allena i Luis A. Morales , " Surface i korozja plutonu Chemistry " , Los Alamos Science , n O 26, 2000, s. 252-273 ( czytaj online )
- (en) „ Plutonium ” , Primer on Spontaneous Heating and Pyrophoricity , na web.archive.org , US Department of Energy, Washington, DC 20585, grudzień 1994(dostęp 8 sierpnia 2017 r . ) .
- (w) Kevin N. Roark, „ Wydano odroczenie wypadków krytycznych ”, krajowe laboratorium w Los Alamos, 8 października 2008 r.
- (w) Jon Hunner, Wymyślanie Los Alamos , 2004 ( ISBN 978-0-8061-3891-6 ) .
- (w) „ Raemer Schreiber ” — Biografie sztabowe, Los Alamos 16 listopada 2008 r . .
- (w) William R. Stratton, „ Przegląd wypadków krytycznych ” [PDF] , Los Alamos National Laboratory , 26 września 1967(dostęp 16 sierpnia 2017 r . ) .
- (w) John Peterson, Margaret MacDonell, Lynne Haroun i Fred Monette, „ Radiologiczna i chemiczna broszura informacyjna w celu wsparcia analizy ryzyka dla zdrowia w obszarach skażonych ” [PDF] w sprawie radioterapii w nagłych wypadkach medycznych , Argonne National Laboratory Environmental Science Division, Marzec 2007(dostęp 14 sierpnia 2017 r . ) .
- Ch. O. Bacri, „ Zarządzanie odpadami jądrowymi ” [PDF] , Od fizyki do detektora , na http://www.in2p3.fr , IN2P3 , listopad 2010(dostęp 14 sierpnia 2017 r. ) ,s. 17.
- Arkusz informacyjny FAS
- (w) Reuben Rainisch, „ Wpływ zawartości Americium-241 na terminy związane ze źródłem promieniowania plutonu ” [PDF] , doroczne spotkanie American Nuclear Society 1999 i temat osadzone w Bostonie, Październik 1999(dostęp 17 sierpnia 2017 r . ) .
- (w) William Moss i Roger Eckhardt , „ Zastrzyk z ludzkim plutonem ” , Los Alamos Science , tom. 23, 1995, s. 177-233 ( czytaj online )
- Guillaume Phan Francois Rebière Jean-Michel Deligne Jean-René Jourdain " plutonu: Aspekty Santé " [PDF] , arkusz radionuklidu na http://centredoc.ecole-eme.fr/opac/ de Szkoła Rzemiosł środowiska ( Francja ) , IRSN , 2007(dostęp 15.08.2017 ) ,s. 5.
- Arkusz radiotoksykologiczny dotyczący plutonu , CEA, grudzień 2005.
- (w) David Albright i Kevin O'Neill, „ The Lessons of Nuclear Secrecy at Rocky Flats ” na https://web.archive.org/ , Institute for Science and International Security, 1999(dostęp 17 sierpnia 2017 r . ) .
- (w) Bernard L. Cohen , „ Zagrożenia związane z zatruciem plutonem ” , Fizyka Zdrowia , tom. 32 N O 5, maj 1977, s. 359-379 ( PMID 881333 , DOI 10.1097/00004032-197705000-00003 , czytaj online )
- (en) Bernard L. Cohen, „ Mit o zatruciu plutonem ” , na web.archive.org , 1985(dostęp 13 sierpnia 2017 r . ) .
- (w) „ Profil toksykologiczny dla plutonu ” na portalu substancji toksycznych ATSDR , Agencja ds. Substancji Toksycznych i Rejestru Chorób, 2010(dostęp 18 sierpnia 2017 r . ) .
- (w) GL Voelz , „ Czego dowiedzieliśmy się o plutonie z danych ludzkich ” , Fizyka Zdrowia , tom. 29 N O 4, Październik 1975, s. 551-561 ( PMID 1205858 , DOI 10.1097/00004032-197510000-00011 , czytaj online )
- promieniotwórczość naturalna i sztuczna , swobodny elektron, 12/2002
- Energia jądrowa: jak się wydostać? , Sieć „Sortir du nuclear”, 2007.
- Biuletyn z kwietnia 2011 r. EELV Midi-Pyrénées.
- Fleur Australe , Geraldine Danon, Flammarion-Arthaud, 2012.
- przestrzeni kosmicznej jądrowego „nowa granica”? , Sortir du jądrowy n o 56 - Winter 2012-2013
- Coś jest nie tak ... nie-d'in Le blog de Gdalia Roulin, Mediapart, 4 lipca 2015 r.
- (w) " Profil toksykologiczny plutonu " [PDF] , Portal substancji toksycznych na ATSDR - Pluton , Agencja ds. Rejestru Substancji Toksycznych i Chorób (ATSDR) i Agencja Ochrony Środowiska USA (EPA) listopad 2010(dostęp 18 sierpnia 2017 r . ) .
- (w) Jeremy Bernstein, pluton: historia najbardziej niebezpiecznego pierwiastka na świecie , 2007, Joseph Henry Press, Waszyngton, DC ( ISBN 978-0-309-10296-4 )
- Misja Ciekawostki: Atomówki w kosmosie , Karl Grossman.
- Obserwacja plutonu: Śledzenie zapasów plutonu , Raporty ISIS, czerwiec 2004 r.
- (en) GA Turner i DM Taylor , " Wiązanie białek surowicy z plutonem in vitro " , Radiation Research , tom. 36, n o 1, Październik 1968, s. 22-30 ( PMID 17387923 , DOI 10.2307/3572534 , JSTOR 3572534 , czytaj online )
- (w) AR Chipperfield i DM Taylor , „ Wiązanie plutonu z glikoproteinami in vitro ” , Radiation Research , tom. 43 N O 2 sierpień 1970, s. 393-402 ( PMID 5465552 , DOI 10.2307 / 3573043 , JSTOR 3573043 , czytaj online )
- (w) Mark P. Jensen, Drew Gorman-Lewis, Baikuntha Aryal, Tatjana Paunesku Stefan Vogt, Paul G. Rickert, Soenke Seifert, Barry Lai, Gayle E. Woloschak i L. Soderholm , „ Uzależniona od żelaza i transferyna – pośredniczy szlak wychwytu komórkowego dla plutonu ” , Nature Chemical Biology , tom. 7 N O 8, 26 czerwca 2011, s. 560-565 ( PMID 21706034 , PMCID 3462652 , DOI 10.1038/nchembio.594 , czytaj online )
- (w) John R. Cooper i Helen S. Gowing , „ Wiązanie ameryku i kurium z białkami surowicy ludzkiej ” , International Journal of Radiation Biology and Related Studies in Physics, Chemistry and Medicine , tom. 40 N O 5, listopad 1981, s. 569-572 ( PMID 6975262 , DOI 10.1080/09553008114551541 , czytaj online )
- (w) David M. Taylor i George J. Kontoghiorghes , „ Mobilizacja plutonu i żelaza z transferyny i ferrytyny przez chelatory hydroksypirydonu ” , Inorganica Chimica Acta , tom. 125 n O 3, Listopad 1986, s. L35-L38 ( DOI 10.1016/S0020-1693 (00) 84710-6 , czytaj online )
- (w) David M. Taylor, Arnulf Seidel, Felicitas Planas-Bohne, Ute Schuppler, Margarethe Neu-Müller i Rainer E. Wirth , „ Badania biochemiczne interakcji plutonu, neptunu i protaktynu z białkami krwi i wątroby ” , Nieorganica Chimica Acta , obj. 140, 15 grudnia 1987 r, s. 361-363 ( DOI 10.1016 / S0020-1693 (00) 81124-X )
- (w) FW Bruenger, BJ Stover i W. Stevens , „ 239 Pu ( IV ): jego subkomórkowa dystrybucja i związek z ferrytyną w wątrobie psa ” , Health Physics , tom. 21 N O 5, Listopad 1971, s. 679-687 ( PMID 5112182 , DOI 10.1097/00004032-197111000-00009 , czytaj online )
- (w) G. Boocock, CJ Danpure, DS i DM Taylor Popplewell , „ Podkomórkowe rozmieszczenie plutonu w wątrobie szczura ” , Radiation Research , tom. 42 N O 2 maj 1970, s. 381-396 ( PMID 4315168 , DOI 10.2307/3572805 , JSTOR 3572805 , czytaj online )
- (w) NP Singh i Wrenn MDE SA Ibrahim , „ Stężenia plutonu w tkankach ludzkich: porównanie z torem ” , Fizyka Zdrowia , tom. 44, n o Suppl. 1, 1983, s. 469-476 ( PMID 6862922 , DOI 10.1097/00004032-198306001-00045 , czytaj online )
- (w) „ Załącznik D. Przegląd podstaw fizyki promieniowania, chemii i biologii ” [PDF] , Portal substancji toksycznych na ATSDR - pluton , Agencja ds. Rejestru Substancji Toksycznych i Chorób (ATSDR) i Agencja Ochrony Środowiska USA (EPA) , listopad 2010(dostęp 18 sierpnia 2017 ) , D-4.
- (w) K. Konzen i R. Brey , „ Rozwój biokinetycznego modelu plutonu-DTPA ” , Fizyka Zdrowia , tom. 108 N O 6, czerwiec 2015, s. 565-573 ( PMID 25905517 , DOI 10.1097/HP.0000000000000283 , czytaj online )
- (w) Pan Alex Brown, Alena i Artem V. Paulenova Gelis , „ Wodne kompleksowanie toru ( IV ), uranu ( IV ), neptunu ( IV ), plutonu ( III / IV ) i ceru ( III / IV ) z DTPA ” , Chemia nieorganiczna , tom. 51 N O 14 16 lipca 2012, s. 7741-7748 ( PMID 22738207 , DOI 10.1021/ic300757k , czytaj online )
- (w) F.Ménétrier, L.Grappin, P.Raynaud, C.Courtay, R.Wood, S.Joussineau, V.List, GN Stradling, DM Taylor, Ph.Berard , MA Morcillo i J.Rencova , " Postępowanie w przypadku przypadkowego spożycia plutonu i ameryku: Wskazówki przewodnie ” , Promieniowanie stosowane i izotopy , tom. 62, n o 6, czerwiec 2005, s. 829-846 ( PMID 15799861 , DOI 10.1016 / j.apradiso.2005.01.005 , czytaj online )
- (w) G Sérandour Tsapis N., C. Gervelas G. Grillon, Mr. Fréchou, JR Deverre H. Bénech E. Fattal, P. Fritsch i JL Poncy , „ odcieleśnienie plutonu przez podanie dopłucne suchego proszku Ca-DTPA : badanie na szczurach po skażeniu płuc różnymi formami plutonu ” , Dosimetry ochrony przed promieniowaniem , tom. 127, n kość 1-4 listopad 2007, s. 472-476 ( PMID 17562654 , DOI 10.1093/rpd/ncm300 , czytaj online )
- (w) David M. Taylor, Susan A. Neil Hodgson i Stradling , „ Leczenie ludzkiego zanieczyszczenia plutonem i amerykiem: czy podawane doustnie złoto Ca-Zn-DTPA byłoby skuteczne? » , Dozymetria ochrony przed promieniowaniem , tom. 127, n kość 1-4 listopad 2007, s. 469-471 ( PMID 17556346 , DOI 10.1093/rpd/ncm299 , czytaj online )
- (w) Pihong Zhao, Vadim V. Romanovsky, Donald W. Whisenhunt Jr. Darleane C. Hoffman, Thomas R. Mohs, Jide Xu i Kenneth N. Raymond , „ ekstrakcja plutonu za pomocą żywic chelatujących hydroksypirydynon i katecholamid ” , Ekstrakcja rozpuszczalnikiem i Wymiana jonowa , obj. 17 N O 5, 1999, s. 1327-1353 ( DOI 10.1080/07366299908934651 , przeczytaj online )
- (w) V. Volf, R. Burgada, KN Raymond i PW Durbin , „ Wczesna terapia chelatacyjna wstrzykniętych Pu-238 i Am-241 u szczurów: Porównanie 3,4,3-LIHOPO, DFO-HOPO, DTPA -DX, DTPA i DFOA ” , International Journal of Radiation Biology , tom. 63, n o 6, Czerwiec 1993, s. 785-793 ( PMID 8100266 , DOI 10.1080/09553009314552191 , czytaj online )
- (w) A. Blanchard, KR Yates, JF Zino, D. Biswas, DE Carlson, H. i D. Hoang Heemstra, „ Zaktualizowane szacunki masy krytycznej dla plutonu-238 ” na https://www.osti.gov / , US Department of Energy: Office of Scientific & Technical Information (dostęp 19 sierpnia 2017 r . ) .
- (w) John Malik, „ Uzyski wybuchów jądrowych w Hiroszimie i Nagasaki ” [PDF] na https://fas.org/ , Los Alamos National Laboratory , wrzesień 1985(dostęp 19 sierpnia 2017 r . ) .
- (en) CE Till, YI Chang, Plentiful Energy: The Story of the Integral Fast Reactor, Complex History of a Simple Reactor Technology, z naciskiem na jej naukowe podstawy dla niespecjalistów , 2011, Charles E. Till i Yoon Il Chang, s. 254-256 . ( ISBN 978-1-4663-8460-6 )
- (w) (w) „ Przechowywanie plutonu w rejonie rzeki Savannah Departamentu Energii: pierwszy raport roczny dla kongresu ” [PDF] na https://www.dnfsb.gov , Rada Bezpieczeństwa Obiektów Obronnych Obiektów Jądrowych,2004(dostęp 20 sierpnia 2017 r. ) , A-1.
- (w) Theodore M. Besmann , „ Zachowanie termochemiczne broni zawierającej gal , paliwo z mieszanką tlenkowo -wodną z reaktora lekkiego (LWR) ” , Journal of the American Ceramic Society , tom. 81 N O 12, grudzień 1998, s. 3071-3076 ( DOI 10.1111 / j.1151-2916.1998.tb02740.x , czytaj online )
- (w) „ zamknięty wyciek radioaktywny Huge Thorp jądrowa elektrownia ” na https://www.theguardian.com , The Guardian , 9 maja 2005(dostęp 20 sierpnia 2017 r . ) .
- (w) „ Od źródeł ciepła do źródeł serca Los Alamos made material for pluton-powered pumper ” na http://www.lanl.gov , Los Alamos National Laboratory (dostęp 20 sierpnia 2017 ) .
- (w) „ Dlaczego misja Cassini nie może używać tablic słonecznych ” na https://web.archive.org , Jet Propulsion Laboratory , Listopad 1996(dostęp 20 sierpnia 2017 r . ) .
- (w) „ Voyager Spacecraft ” na https://www.jpl.nasa.gov , Jet Propulsion Laboratory (dostęp 20 sierpnia 2017 ) .
- (w) Venkateswara Sarma Mallela, V. Ilankumaran i N. Srinivasa Rao , „ Trendy w bateriach rozruszników serca ” , Indian Pacing and Electrophysiology Journal , tom. 4, n O 4, październik-grudzień 2004, s. 201-212 ( PMID 16943934 , PMCID 1502062 , czytaj online )
- (w) „ Plutonium Powered Pacemaker (1974) ” , na http://www.orau.org , Oak Ridge Associated Universities (w) , 10 maja 2011(dostęp 20 sierpnia 2017 r . ) .
- (w) „ Plutonium ” , na http://www.world-nuclear.org/ , World Nuclear Association (dostęp 20 sierpnia 2017 ) .
- „ Kodeks obrony ” , na https://www.legifrance.gouv.fr (dostęp 19 sierpnia 2017 r . ) .
- Henri Métivier , „ Pluton - Mythes et Réalités ” (dostęp 23 grudnia 2014 )
- Produkcja plutonu , Federacja Naukowców Amerykańskich.
- (w) EF Hammel, „ Poskromienie” 49” – Big Science w krótkim czasie. Wspomnienia Edwarda F. Hammla ” , Los Alamos Science, t. 26, Iss. 1, 2000 (dostęp 24 maja 2008 ) . Konwencja ta została rozszerzona na wszystkie aktynowce , w równaniach opisujących dynamikę ich populacji w reaktorach. Tak więc izotop 235 uranu (92) otrzymuje w równaniach indeks 25 i tak dalej.
- (w) DC Hoffmana, FP Lawrence, JL Mewherter i FM Rourke , " Wykrywanie plutonu-244 w przyrodzie " , Nature , vol. 234 n O 5.325 19 listopada 1971, s. 132-134 ( DOI 10.1038/234132a0 , Bibcode 1971Natur.234.132H , czytaj online )
- Raport bojowy 1997/1998 do Senatu.
- (w) " Alternatives to MOX - Direct-disposable options for stockpils of plutonu " na http://fissilematerials.org ,kwiecień 2015(dostęp 23 kwietnia 2015 )
Zobacz również
Bibliografia
- ( fr ) David R. Lide i in. , Handbook of Chemistry and Physics , Boca Raton (FL), CRC Press, Taylor & Francis Group,2006, 87 th ed. , 2608 s. ( ISBN 0-8493-0487-3 )
- Sandrine Matton; Pomiary in vitro i in vivo parametrów rozpuszczania mieszanych tlenków uranu i plutonu w środowisku biologicznym (pomiary in vitro i in vivo parametrów rozpuszczania mieszanych tlenków uranu i plutonu w środowisku biologicznym); Praca dyplomowa Sandrine Matton (promotor Michel Genet), obroniona na Uniwersytecie Paryskim 11 Orsay ( Inist CNRS )
- IEER, energii i bezpieczeństwo n O 3 Podsumowanie: Stosowanie plutonu wojskowej jako paliwa do reaktora; Wpływ plutonu na zdrowie; MOX we Francji i Belgii; Sytuacja i perspektywy produkcji paliwa MOX w Rosji; Transmutacja nie jest alternatywą dla pochówku; Transformacja plutonu w czasie] Energie-Sécurité n O 3, 1997 (PDF skanowania)
Powiązane artykuły
Linki zewnętrzne
- (pl) „ Dane techniczne dla plutonu ” (dostęp 19 kwietnia 2019 r. ) , ze znanymi danymi dla każdego izotopu na podstronach
- (fr) Eksperymenty na ludziach z plutonem w Stanach Zjednoczonych (Los Alamos Science, 23, 1995)
- (en) pluton , przez „Światowe Stowarzyszenie Jądrowe”
- (fr) „ Izotopy plutonu i ich potomkowie w cywilnej energetyce jądrowej ” (konsultacja 23 grudnia 2014 r. ) , raport do Akademii Nauk Robert Dautray - Paryż -maj 2005 - Wydania Tec & Doc Lavoisier.
- (pl) Pluton, Mythes et Réalités – styczeń 2010 – EDP Sciences.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | Hej | |||||||||||||||||||||||||||||||
| 2 | Li | Być | b | VS | NIE | O | fa | Urodzony | |||||||||||||||||||||||||
| 3 | nie dotyczy | Mg | Glin | tak | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | To | Sc | Ti | V | Cr | Mn | Fe | Współ | Lub | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Tak | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Płyta CD | W | Sn | Sb | ty | ja | Xe | |||||||||||||||
| 6 | Cs | Ba | To | Pr | Nd | Po południu | Sm | Miał | Bóg | Tb | Dy | Ho | Er | Tm | Yb | Czytać | Hf | Twój | W | Re | Kość | Ir | Pt | W | Hg | Tl | Pb | Bi | Po | W | Rn | ||
| 7 | Fr | Ra | Ac | Cz | Rocznie | U | Np | Mógłby | Jestem | Cm | Bk | cf | Jest | Fm | Md | Nie | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
|
Metale alkaliczne |
Ziemia alkaliczna |
Lantanowce |
Metale przejściowe |
Słabe metale |
metalem loids |
Długoterminowe metale |
geny halo |
Gazy szlachetne |
Przedmioty niesklasyfikowane |
| aktynowce | |||||||||
| Superaktynowce | |||||||||
![{\ displaystyle \ mathrm {^ {238} _ {\ 92} U \ + \ _ {0} ^ {1} n \ \ longrightarrow \ _ {\ 92} ^ {239} U \ {\ xrightarrow [{23,5 \ min}] {\ beta ^ {-}}} \ _ {\ 93} ^ {239} Np \ {\ xrightarrow [{2,3565 \ d}] {\ beta ^ {-}}} \ _ {\ 94} ^ {239} Pu}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ca14d0d7115d4a0e1c82696e40c9ef5bd86d1b5a)
![{\ displaystyle {\ początek {wyrównany} ^ {238} _ {92} \ matematyka {U} + \, _ {1} ^ {2} \ matematyka {D} \ longrightarrow \; & ^ {238} _ {93 } \ mathrm {Np} +2 \; _ {0} ^ {1} \ mathrm {n} \\ & ^ {238} _ {93} \ mathrm {Np} \; {\ xrightarrow [{2 {,} 117 \; \ mathrm {j}}] {\ beta ^ {-}}} \; _ {94} ^ {238} \ mathrm {Pu} \ koniec {wyrównany}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/90b3f48cb5d6e7864949a39ca0de084e89f9cdc5)


