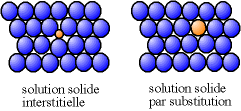Stop
Stopu jest połączenie metalowego elementu z jednym lub więcej metali w wyniku fuzji.
Właściwości mechaniczne czystych metali są w większości stosunkowo niskie. Fakt dodania kolejnych elementów umożliwia „utwardzanie” metalu przy jednoczesnym zwiększeniu jego właściwości mechanicznych. Oprócz wzmocnień mechanicznych generowanych przez odkształcenia, takich jak umocnienie przez zgniot , istnieje utwardzanie chemiczne przez dodanie pierwiastków w roztworze stałym lub przez wytrącanie twardniejących faz wtórnych, takich jak węgliki . Te dodatki umożliwiają również modyfikację właściwości chemicznych, takich jak odporność na korozję , lub poprawę innych właściwości, na przykład płynności .
W stopie główny pierwiastek metaliczny, to znaczy stanowiący najważniejszą część mieszaniny, nazywany jest „metalem podstawowym” lub „zasadą”. Elementy dodane celowo nazywane są „elementami stopowymi” lub „elementami dodatkowymi”, a elementy niepożądane nazywane są „zanieczyszczeniami”.
Pierwiastkami stopowymi są najczęściej metale, ale mogą to być również inne pierwiastki chemiczne takie jak węgiel w stali lub żeliwie , krzem w aluminium itp.
Gdy pierwiastek stopowy nie jest metalem, jego zawartość na ogół pozostaje niska (maksymalnie kilka % masy). Tak więc w stali stężenie węgla jest mniejsze niż 2% masowych (mniej niż 7% masowych w przypadku żeliwa), podczas gdy możliwe jest wykonanie stopu miedziowo - cynkowego (potocznie nazywanego mosiądzem ) o zawartości 50% każdy z elementów.
Historia
Istnieją również tak - zwane stopy naturalne, na przykład elektron , stopu rodzimej złota i srebra użytego w prehistorii i starożytności : Warna , Azji Mniejszej , Ur , Egipcie , między innymi. Na III th century BC. AD , w dziele O kamieniach , filozof Teofrast wyjaśnia, że tytuł stopu określany jest w collybos , drachmach lub półdrachmach – a nawet ziarnach jęczmienia .
Stop binarny
Stop binarny jednofazowy
Jednorodny stop składa się z pojedynczej jednorodnej fazy stałej. Aby uzyskać jednorodny stop, musi istnieć całkowita mieszalność między pierwiastkami stopowymi. Istnieją dwie możliwości:
- Te dwa pierwiastki stopowe są rozpuszczalne w sobie, niezależnie od ich odpowiednich proporcji.
- Stężenie pierwiastka stopowego jest poniżej granicy rozpuszczalności.
W Humowskich reguł-Rothery wskazuje warunki do uzyskania jednorodnego stopu z całkowitą rozpuszczalność w stanie stałym.
| Element | Promień atomowy |
Struktura krystaliczna |
|---|---|---|
| Bizmut | 160 po południu | Rhomboedral |
| Antymon | 145 po południu | Rhomboedral |
Bizmutu i antymonu są całkowicie rozpuszczalne jeden w drugim. Tworzą zatem roztwór stały niezależnie od składu chemicznego i temperatury (pod warunkiem, że pozostają w stanie stałym, to znaczy poniżej temperatury solidusu ). Uzyskany diagram fazowy jest w tym przypadku, gdy schemat jednej linii.
Inne pary metali charakteryzują się dobrą mieszalnością, umożliwiającą uzyskanie jednorodnych roztworów stałych w określonych temperaturach: miedź - nikiel , miedź- pallad , srebro - złoto , srebro-pallad, molibden - wanad , molibden- wolfram itp.
Niektóre stopy dwuskładnikowe wykazują małą wadę rozpuszczalności w niskich temperaturach. Na diagramie fazowym pojawia się sektor, w którym współistnieją dwie fazy, pierwsza składa się z roztworu stałego nasyconego B w A i odwrotnie, druga faza składa się z roztworu stałego nasyconego A w B. Tak jest na przykład w przypadku układ miedziowo-niklowy, który poniżej 322 °C przedstawia strefę dwufazową.
Stop binarny wielofazowy
Innym typem diagramu fazowego stosunkowo powszechnym w stopach binarnych jest diagram fazowy eutektyczny. Ten typ diagramu fazowego wykazuje szereg ważnych cech, na które należy zwrócić uwagę. Przede wszystkim na schemacie widoczne są trzy obszary jednofazowe: α, β i ciecz. Na rysunku po lewej, faza α jest roztworem stałym bogatym w miedź, która zawiera srebro jako substancję rozpuszczoną i ma strukturę komórkową CFC ( face-centered Cuba ). Faza β (roztwór stały) również charakteryzuje się strukturą CFC, ale dla której miedź jest substancją rozpuszczoną.
Zatem rozpuszczalność dodawanego pierwiastka w każdej z tych faz stałych jest ograniczona. Innymi słowy, stężenie srebra, które może rozpuszczać się w miedzi (dla fazy α) bez modyfikowania jej struktury krystalograficznej jest ograniczone. Z tego samego powodu dodatek miedzi do srebra (faza β) jest ograniczony. Granica rozpuszczalności fazy α odpowiada linii podziału oznaczonej „CBA”.
Dla temperatur poniżej 779 °C ( 1434 °F ) linię odpowiadającą granicy rozpuszczalności ciała stałego, która oddziela obszar fazy α i obszar współistnienia faz α + β nazywamy linią solvus. Granicą oddzielającą fazę α i obszar α+L jest linia solidus (AB), natomiast linią oddzielającą region α+L i domenę ciekłą jest linia likwidus (AE). Dla bogatej w srebro części diagramu fazowego istnieją również trzy linie: solvus (HG), solidus (GF) i likwidus (EF). Pozioma linia BEG, która jest równoległa do osi odciętej, rozciąga się pomiędzy odpowiednimi maksimami rozpuszczalności faz α i β. Nazywa się to łożyskiem eutektycznym i może być również traktowane jako linia solidus, reprezentująca najniższą temperaturę, w której faza ciekła może istnieć w równowadze termodynamicznej dla dowolnego stopu miedzi i srebra.
Istnieją również trzy regiony dwufazowe występujące w układzie miedź-srebro. W miarę dodawania srebra do miedzi temperatura, w której stopy stają się całkowicie płynne, zmniejsza się wzdłuż linii likwidus (linia AE); w ten sposób temperatura topnienia miedzi jest obniżona przez dodanie srebra. Ta sama zasada obowiązuje w przypadku stopów, w których przeważającym związkiem jest srebro: wprowadzenie miedzi obniża całkowitą temperaturę topnienia wzdłuż linii likwidus FE. Te linie likwidus odpowiadają punktowi E na wykresie fazowym, przez który przechodzi również pozioma linia izotermiczna BEG. Punkt E jest punktem eutektycznym, oznaczonym składem EC i temperaturą TE; dla układu miedź-srebro wartości CE i TE wynoszą odpowiednio 71,9% wag. Ag i 779 °C ( 1434 °F ).
W stopie o składzie „CE” zachodzi ważna reakcja, która jednak podczas przechodzenia przez TE zmienia temperaturę. Podczas chłodzenia faza ciekła przekształca się w dwie fazy stałe (α i β) w temperaturze TE, reakcja odwrotna zachodzi podczas ogrzewania. Nazywa się to reakcją eutektyczną (eutektyczna oznacza, że łatwo się topi), a CE i TE reprezentują odpowiednio skład eutektyczny i temperaturę. Często pozioma linia solidusowa w TE nazywana jest izotermą eutektyczną. Reakcja eutektyczna po schłodzeniu jest podobna do krzepnięcia czystych składników, ponieważ reakcja przebiega w stałej temperaturze lub izometrycznie przy TE. Jednak stałym produktem krzepnięcia eutektyki są zawsze dwie fazy stałe, podczas gdy dla pojedynczego składnika powstaje tylko jedna faza. Z powodu tej reakcji eutektycznej, diagramy fazowe podobne do tych na diagramie Ag-Cu są określane jako diagramy fazowe eutektyczne.
Konstruując binarne diagramy fazowe, ważne jest, aby zrozumieć, że jedna lub co najwyżej dwie fazy mogą być w równowadze w regionie fazowym. W przypadku układu eutektycznego trzy fazy (α, β i L) mogą być w równowadze, ale tylko w punktach wzdłuż linii eutektycznej.
Istnieją tysiące możliwych kombinacji diagramów fazowych z wieloma fazami. Niektóre z głównych cech diagramów fazowych obejmują punkty kongruentne, w których faza stała bezpośrednio zamienia się w ciecz. Istnieje również punkt peritektoidalny, dla którego faza stała po podgrzaniu zamienia się w dwie fazy stałe różne od początkowej fazy stałej. I odwrotnie, jeśli transformacja zachodzi podczas chłodzenia, mówimy o punkcie eutektoidalnym.
Złożonym diagramem fazowym o dużym znaczeniu technologicznym jest układ żelazo-węgiel zawierający mniej niż 7% węgla.
Oś X takiego wykresu odpowiada zmieniającemu się stężeniu mieszaniny. Ponieważ mieszaniny są na ogół dalekie od osłabienia, a ich gęstość w funkcji temperatury jest na ogół nieznana, korzystnym pomiarem jest stężenie molowe. Odradza się stosowanie schematu opartego na objętości pomiaru jako molarności.
Struktura
Jednorodny stop
Pierwiastek addycyjny, który tworzy roztwór stały z metalem nieszlachetnym, może znajdować się albo pomiędzy atomami pierwiastka większościowego (mówimy o „wstawieniu”), albo w miejsce atomów metalu większościowego (mówimy wtedy o „podstawieniu”). ").
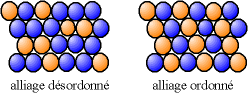
Zastąpienie może prowadzić albo do nieuporządkowanego stopu , w którym różne atomy zajmują losowe pozycje, albo do uporządkowanego stopu , w którym atomy o różnej naturze następują regularnie na przemian.
Stop heterogeniczny
Gdy zawartość pierwiastków stopowych wzrasta, mogą powstać dwie fazy: faza zawierająca niewiele pierwiastków stopowych oraz faza o wysokiej zawartości pierwiastków stopowych. Krystalitów wysokiej klasy są nazywane „rzucili”.
Te osady są często zamawiane stopów, zwany „międzymetalicznych”. Powstałe w ten sposób związki międzymetaliczne są czasem później badane jako czyste stopy, jak nowy materiał, i staramy się wytwarzać je jako takie, a nie jako wydzielenia.
Przykłady
Główne stopy
Stopy żelaza- żeliwo : żelazo + węgiel (ponad 1,7% i do 4% masy węgla)
- stal : żelazo + węgiel (mniej niż 2,1% masy węgla) (+ możliwe śladowe ilości niklu , chromu , molibdenu w niewielkim procencie (<4%))
- stal nierdzewna : żelazo + węgiel + nikiel + chrom, a czasami molibden, wanad
- brąz : miedź + cyna ; „ mosiądz ” to stara nazwa brązu
- mosiądz : miedź + cynk
- miliard : miedź + srebro ; używany głównie do bicia monet o niskiej wartości value
Nazywa się je również stopami lekkimi ze względu na gęstość aluminium w porównaniu z innymi metalami.
Więcej informacji można znaleźć w dwóch artykułach poniżej:
Mniej znane stopy
- stop ołowiowo-cynowy : do lutowania
- elektrum : złoto + srebro
- amalgamat : rtęć + inny metal, na przykład złoto lub miedź; termin oznacza również mieszaninę metali stosowaną do pielęgnacji zębów („wypełnianie”)
- srebro niklowe : miedź + cynk + nikiel
- monel (nazwa handlowa): nikiel + miedź
- reguluje : cyna lub ołów + antymon
- ruolz : nikiel + srebro + miedź
- tumbaga : stop złota i miedzi używany przez cywilizacje prekolumbijskie Ameryki Południowej i Mezoameryki .
- znalu : cynk + aluminium + magnez + miedź i inne " ZL " ( główne składniki : cynk i aluminium )
- virenium : miedź + cynk + nikiel
Stopy do konkretnych zastosowań
- ferrotityny : żelazo + 25 do 70% Ti + 4 do 10% aluminium
- TA6V: tytan + 6% aluminium + 4% wanadu, szeroko stosowany w przemyśle lotniczym
- MCrAl: metal + chrom + aluminium + czasami itr (MCrAlY), stopy znane z dobrej wytrzymałości mechanicznej i odporności na korozję w wysokich temperaturach
- FeCrAl: żelazo + chrom + aluminium
- NiCrAl: nikiel + chrom + aluminium
- superstopy na bazie niklu (np. inconele ): dobra wytrzymałość mechaniczna i odporność na korozję w wysokich temperaturach
-
międzymetaliczny : stopy uporządkowane z zachowaniem dokładnej stechiometrii (ale odchylenia od stechiometrii są tolerowane)
- NiAl β: 50% nikiel + 50% aluminium
- FeAl B2: 50% żelaza + 50% aluminium
- TiAl: 50% tytan + 50% aluminium
- Stopy o niskich współczynnikach rozszerzalności (stworzone przez Charlesa Édouarda Guillaume )
- FeNiCo stop 54% żelazo + 29% nikiel + 17% kobalt przeznaczony do uszczelniania szkło/metal lub ceramika/metal
Bibliografia
- Henri Godfroid , Metalurgia dla mechaniki: Ogólne właściwości stopów, ich obróbka cieplna , Paryż, La Chapelle-Montligeon, Impr. de Montligeon, płk. "Wydawnictwo Mechaniczne",1950( przedruk 1959), In-8 ° (240 × 160), 378 s., ryc., pl. 2000 fr. [DL 4455] ( BNF Wskazówki n O FRBNF32174558 ) ( BNF Wskazówki n O FRBNF32174559 )
- W starożytnej grece Περὶ Λίθων .
- w starożytnej grece κολλυβος .
- Frag. 46, wyd. Wimmer: retuszuje, precyzja jest tutaj o staterze z Cyzikosu .
- (w) William Callister , Podstawy materiałoznawstwa i inżynierii: etekst interaktywny , New York, Wiley ,2001( 1 st ed. 5), 524 , str. ( ISBN 978-0-471-39551-5 , OCLC 761975075 ) , s. 292-295.
Uwagi
- Zwykłe francuskie oznaczenie TA6V jest oparte na starej normie NF A 02-004, która została teraz anulowana, jej oznaczenie chemiczne to Ti Al 6 V.
Zobacz również
Różne stopy
- Magnes AlNiCo
- mosiądz
- stop aluminium do kutego
- stop aluminium dla odlewni
- stop miedzi
- stop Devarda
- Stop Heuslera
- stopu tytanu
- amorficzny stop metali metal
- stop złota i miedzi
- stop ołowiu z cyną
- stop plutonowo-galowy
- Alumel
- Pieniądze z Wielkiej Brytanii
- Srebro szterlingowe
- arsenek galu i glinu
- miliard (stop)
- brytyjczyk
- brąz (stop miedzi i cyny)
- brąz berylowy
- brąz koryncki
- brąz fosforowy
- chromel
- konstantan
- cunife
- miedzioaluminium
- cupronickel
- duraluminium
- elektron
- elektronika
- cyna
- Fernico
- stop żelaza
- żeliwo (metalurgia)
- galinstan
- Hastelloy
- inwar
- Kanthal
- kovar
- mosiądz
- ledbitis
- nowe srebro
- magnal
- drewno metal
- Moldamax , stop miedziowo-berylowy
- monel
- Nichrom
- nikiel
- Nikiel Raneya
- Nigusil
- Niresist
- Nitinol
- białe złoto
- Nordyckie złoto (czasami nazywane „stopem nordyckim”)
- orichalcum
- partinium
- Peraluman
- permalloy
- krzemień
- ołów typograficzny
- plotka
- Reynolds 531 , stop manganowo-molibdenowy
- ruolz
- shakudō
- stellit (stop)
- Titanal
- tumbaga
- Zamak
- zikral