Hel
| Hel | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Nadciekłe ciekły hel ( T ≤ 2 K ). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pozycja w układzie okresowym | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Symbol | Hej | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nazwisko | Hel | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liczba atomowa | 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupa | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kropka | 1 e okres | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | Bloki | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rodzina elementów | gaz szlachetny | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroniczna Konfiguracja | 1 s 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrony według poziomu energii | 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomowe właściwości pierwiastka | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atomowa | 4.002602 ± 0.000002 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Promień atomowy (obliczony) | 128 wieczorem ( 31 wieczorem ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Promień kowalencyjny | 28 wieczorem | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Promień Van der Waalsa | 140 po południu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stan utlenienia | 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlenek | nieznany | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energie jonizacji | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 Re : 24,587387 eV | 2 E : 54,417760 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Najbardziej stabilne izotopy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proste właściwości fizyczne ciała | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Państwo zwykłe | Gaz | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
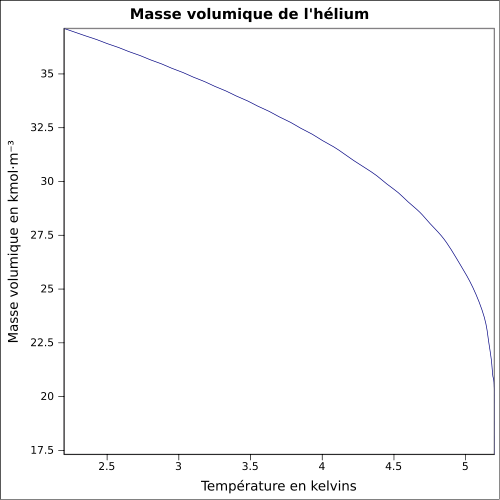
| Masa objętościowa |
0,1786 g · L- 1 ( 0 ° C , 1 atm ) ; 0,125 kg · L -1 (ciecz, -268,93 ° C ) równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kryształowy system | Kompaktowy sześciokątny | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kolor | Bezbarwny | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punkt fuzji | 0,95 K ( 26 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura wrzenia | -268,93 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia termojądrowa | 5,23 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia parowania | 0,08 kJ · mol -1 ( 1 atm , -268,93 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura krytyczna | -267,96 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ciśnienie krytyczne | 2,26 atm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Objętość molowa | 22,414 × 10 -3 m 3 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ciśnienie pary |
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prędkość dźwięku | 972 m · s -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ogromne ciepło | Cp 20,79 J · mol -1 · K -1
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Przewodność cieplna | 152,0 mW · m -1 · K -1 ( 26,85 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Różnorodny | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O ECHA | 100 028 334 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O WE | 231-168-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Środki ostrożności | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Ostrzeżenie H280 i P410 + P403 H280 : Zawiera gaz pod ciśnieniem; ogrzanie grozi wybuchem P410 + P403 : Chronić przed światłem słonecznym. Przechowywać w dobrze wentylowanym pomieszczeniu. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 W, A : Temperatura krytyczna sprężonego gazu = -267,9 ° C Ujawnienie przy 1,0% zgodnie z kryteriami klasyfikacji classification |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1046 : SPRĘŻONY HEL Klasa: 2.2 Nalepka: 2.2 :Gazyniepalne, nietoksyczne (odpowiada grupom oznaczonym literą A lub dużą literą O);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednostki SI i STP, chyba że zaznaczono inaczej. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hel jest pierwiastek chemiczny o liczbie atomowej 2 He symbolem. Jest to gaz szlachetny (lub szlachetny ), praktycznie obojętny , pierwszy z rodziny gazów szlachetnych w układzie okresowym pierwiastków . Jego temperatura wrzenia jest najniższa wśród znanych ciał i istnieje tylko w postaci stałej, gdy jest poddawana ciśnieniu przekraczającemu 25 atmosfer .
Hel ma dwa stabilne izotopy : hel 4 ( 4 He), najbardziej rozpowszechniony, oraz hel 3 ( 3 He). Te dwa izotopy, w przeciwieństwie do większości pierwiastków chemicznych, różnią się znacznie właściwościami, ponieważ ważny jest stosunek ich mas atomowych. Z drugiej strony efekty kwantowe, czułe przy niskich energiach, nadają im bardzo różne właściwości. Ten artykuł dotyczy głównie helu 4 ( 4 He). Artykuł Helium 3 zestawia specyficzne właściwości izotopu 3 He.
Słowo hel został zbudowany od greckiego Helios ( Ἥλιος / Helios , „THE Sun ” ), ten element po zaobserwowano po raz pierwszy w widmie słonecznym dniu18 sierpnia 1868podczas całkowitego zaćmienia Słońca przez astronoma Julesa Janssena .
Hel jest po wodorze pierwiastkiem najobficiej występującym we Wszechświecie . Większość tego helu została wytworzona podczas pierwotnej nukleosyntezy, ale produkują ją inne procesy, w szczególności radioaktywność α ( patrz podrozdział Obfitość naturalna ). Na Ziemi , według szacunków z Biura Gospodarki Przestrzennej w Stanach Zjednoczonych w 2006 roku, helu Zasoby łącznie 52 mld metrów sześciennych.
Hel ma różne zastosowania przy silnym wzroście, podczas gdy produkcja przemysłowa spadła z powodów ekonomicznych: jego niedobór staje się niepokojący. Jednak w 2016 roku z ekonomicznego punktu widzenia rynek helu jest spokojny i ostatnio przeszedł od niedoboru do nadwyżki.
Znanych jest osiem izotopów helu. Hel 3 (dwa protony i jednego neutronu) i helowo-4 (dwóch protonów i dwóch neutronów) są stałe, a inne są bardzo niestabilne, praktycznie pewne, istnieje tylko podczas treningu. W atmosferze ziemskiej, jest tylko jeden hel-3 atom na każdy milion hel-4 atomów . W przeciwieństwie do większości pierwiastków, obfitość izotopowa helu jest bardzo zróżnicowana w zależności od jego pochodzenia, ze względu na różne procesy powstawania. Najobficiej występujący izotop, hel 4 , jest wytwarzany na Ziemi przez radioaktywność α ciężkich pierwiastków: wytwarzane tam cząstki α są w pełni zjonizowanymi jądrami helu 4 . Hel-4 jest rdzeń niezwykłej trwałości, ponieważ jego nukleony są rozmieszczone w całych warstwach .
W całym Wszechświecie większość obecnego helu powstała (w ogromnych ilościach, około 25% całej materii) podczas pierwotnej nukleosyntezy . Prawie cała reszta helu wytwarzanego we Wszechświecie jest (lub była) podczas gwiezdnej nukleosyntezy.
Hel-3 jest obecny na Ziemi jedynie w śladowych ilościach; większość pochodzi z uformowania się Ziemi, choć trochę jeszcze na nią spada, uwięziona w międzygwiezdnym pyle . Ślady są nadal produkowane przez P radioaktywność w tryt . Skały w skorupie ziemskiej mają stosunków izotopowych różne aż do 10-krotnie , a wskaźniki te mogą być wykorzystane do określenia pochodzenia skał i składu ziemskiego płaszcza . Hel-3 jest w większej ilości w gwiazdy, jednak jest wytwarzany w czasie syntezy jądrowej , gwiazdy nie uwalniają niewiele (jak deuter i litu lub bor ), ponieważ n pojawia się tylko w pośrednim łańcucha prowadzi do helu 4 : jest jest „skonsumowany”, ponieważ jest produkowany w gwiazdach. W efekcie w ośrodku międzygwiazdowym stosunek izotopów jest około 100 razy wyższy niż na Ziemi. Materiały pozaplanetarne, takie jak regolit z Księżyca czy asteroidy, zawierają ślady helu 3 z wiatru słonecznego . Powierzchnia Księżyca zawiera koncentrację rzędu 10-8 . Wielu autorów, począwszy od Geralda Kulcińskiego w 1986 roku, zaproponowało zbadanie Księżyca, wydobycie helu-3 z regolitu i wykorzystanie go do generowania energii poprzez fuzję jądrową.
Hel-4 może być chłodzony do około 1 K przez odparowanie. Hel-3 , który ma niższą temperaturę wrzenia, oziębia się do temperatury 0,2 K w taki sam sposób. Mieszaniny równych części helu 3 i 4 oddzielne, poniżej 0,8 K , ponieważ nie mieszają się już ze względu na ich różnice (atom helu 4 jest bozonem, a atom helu 3 jest fermionem , mają dwie różne statystyki kwantowe) . Do lodówki rozcieńczania używać tej właściwości, aby osiągnąć pewne millikelvins.
Inne izotopy helu mogą być wytwarzane w reakcjach jądrowych , które są niestabilne i szybko rozpadają się na inne jądra. Izotopem o najkrótszym okresie półtrwania jest hel 2 (2 protony, bez neutronów: diproton , który rozpada się na dwa protony w czasie 3 × 10 −27 s ). Hel 5 i hel 7 zaniku przez emisję neutronu z okresem półtrwania 7,6 x 10 -23 sekund i 2,9 x 10 -21 sekund odpowiednio. Hel 6 i hel 8 rozpadają się przez p radioaktywności z okresem półtrwania 0,8 s i 0,119 S , odpowiednio. Do izotopów 6 i 8 posiadają luźną strukturę w którym neutrony krążące daleko od centrum, to jest nazywany halogen jądrowego .
Pojedynczy korpus helowy
Hel to bezbarwny, bezwonny i nietoksyczny gaz. Jest praktycznie obojętny chemicznie, monoatomowy w każdych okolicznościach. W szerokim zakresie temperatur i ciśnień zachowuje się eksperymentalnie jak gaz doskonały, co czyni go uprzywilejowaną substancją do eksperymentowania teorii fizykochemicznych. Dwa stabilne izotopy helu są jedynymi związkami chemicznymi, które nie posiadają punktu potrójnego .
Gaz
Przewodność cieplna gazowego helu jest większa niż wszystkich gazów z wyjątkiem wodoru, a jego ciepło właściwe jest wyjątkowo wysokie. Jego współczynnik Joule'a-Thomsona jest ujemny w temperaturze pokojowej, co oznacza, że w przeciwieństwie do większości gazów nagrzewa się, gdy może się swobodnie relaksować. Temperatura inwersji Joule'a-Thomsona wynosi około 40 K lub -233,15 ° C przy ciśnieniu 1 atm . Po schłodzeniu poniżej tej temperatury, hel można upłynnić przez ochłodzenie ze względu na jego rozszerzanie.
Hel jest również najmniej rozpuszczalnym w wodzie gazem ze wszystkich znanych gazów. Ze względu na małe rozmiary atomów, jego szybkość dyfuzji przez ciała stałe jest trzykrotnie większa niż powietrza i około 65% szybkości dyfuzji wodoru.
Współczynnik załamania helu jest bliższy jedności niż jakiegokolwiek innego gazu. Prędkość dźwięku w helu jest większa niż w jakimkolwiek innym gazie z wyjątkiem wodoru.
W przeciwieństwie do plazmy gaz jest doskonałym izolatorem elektrycznym.
Osocze
Większość pozaziemskiego helu znajduje się w stanie plazmy , którego właściwości znacznie różnią się od właściwości helu atomowego. W plazmie elektrony helu nie są związane z jądrem, co prowadzi do bardzo wysokiego przewodnictwa elektrycznego, nawet przy częściowej jonizacji. Naładowane cząstki są bardzo wrażliwe na pola elektryczne i magnetyczne. Na przykład w wietrze słonecznym zjonizowany hel i wodór oddziałują z magnetosferą Ziemi , powodując zjawisko prądów Birkelanda i zorzy polarnej .
Podobnie jak inne gazy szlachetne, hel ma metastabilne poziomy energii, które pozwalają mu pozostać podekscytowanym w wyładowaniu elektrycznym, którego napięcie jest poniżej jego potencjału jonizacyjnego. Pozwala to na jego zastosowanie w lampach wyładowczych .
Ciekły
W przeciwieństwie do innych pierwiastków, hel pozostaje płynny do zera absolutnego przy ciśnieniu poniżej 25 atm . Jest to bezpośrednia konsekwencja mechaniki kwantowej: dokładniej energia atomów w stanie podstawowym układu jest zbyt wysoka, aby umożliwić zestalenie (patrz podrozdział #Solidne ).
Poniżej punktu wrzenia w 4,22 K i powyżej elementu lambda do 2.176 8 K The hel-4 występuje w postaci bezbarwnej cieczy normalnej zwanej hel I . Podobnie jak inne ciecze kriogeniczne , wrze po podgrzaniu i kurczy się, gdy obniża się jego temperatura. Hel I ma współczynnik załamania zbliżone do gazu: 1,026; co sprawia, że jego powierzchnia jest tak trudna do zobaczenia, że często używamy pacy styropianowej, aby zobaczyć jej poziom. Bezbarwny ciecz ma bardzo niską lepkość i gęstość od 0,125 = 1/8 , który wynosi tylko jedną czwartą wartości przewidywanej przez fizyczne klasycznych . Aby wyjaśnić tę właściwość, należy odwołać się do mechaniki kwantowej i dlatego ciekły hel w jego różnych postaciach nazywany jest płynem kwantowym , co oznacza, że efekty mechaniki kwantowej, zwykle czułej tylko w skali mikroskopowej, ujawniają się w skali makroskopowej, ponieważ hel atom 4 jest bozonem . Jest to interpretowane jako konsekwencja faktu, że temperatura wrzenia jest tak bliska zeru bezwzględnego, że przypadkowe ruchy termiczne nie mogą już maskować właściwości atomowych.
Nadciekły
Ciekły hel poniżej punktu lambda zaczyna wykazywać dość nietypowe właściwości, w stanie zwanym helem II .
Na przejściu od helu I do helu II w punkcie lambda hel rozszerza się. Wraz ze spadkiem temperatury hel II nadal rozszerza się, aż do około 1 K , gdzie zaczyna się ponownie kurczyć, jak większość ciał.
Helu II może przepływać przez naczynia włosowate 10 -7 10 -8 m bez lepkości mierzalny. Jednak gdy mierzymy lepkość między dwoma obracającymi się względem siebie dyskami, stwierdzamy lepkość porównywalną z gazowym helem. Obecna teoria wyjaśnia ten fakt za pomocą dwóch płynów modelu z László Tisza (w) dla helu II . W tym modelu ciekły hel, poniżej punktu lambda, składa się z mieszaniny atomów helu w stanie podstawowym i atomów w stanach wzbudzonych, które zachowują się bardziej jak zwykły płyn.
Ilustracją tej teorii jest efekt fontanny . W tym eksperymencie pionowa rurka, mająca małą dyszę na górnym końcu, jest zanurzona na swoim dolnym końcu w kąpieli z helem II . Jest tam blokowany przez spiekaną tarczę , przez którą może krążyć tylko płyn bez lepkości. Jeśli podgrzejemy rurkę, np. zapalając ją, zamienimy część nadciekłą w zwykły płyn. Aby przywrócić równowagę obu płynów w kąpieli, przez spiekany korek przeniknie nadciek, a w celu zachowania objętości część zawartości tuby zostanie wyrzucona przez górną dyszę, tworząc strumień, który może być przerwać przez zaprzestanie ogrzewania.
Przewodność cieplna o helu II jest większa niż w przypadku jakiegokolwiek innego znanego ciała. Zapobiega to wrzeniu helu II , ponieważ każde doprowadzone ciepło natychmiast wędruje na powierzchnię, gdzie po prostu odparowuje w gaz. Ta przewodność jest milion razy większa niż helu I i kilkaset razy większa niż miedzi. Wynika to z faktu, że przewodzenie ciepła odbywa się w wyjątkowym mechanizmie kwantowym. Większość materiałów, które są dobrymi przewodnikami ciepła, ma pasmo walencyjne wolnych elektronów, które służą do przewodzenia ciepła. Helium II ma taką taśmę jeszcze dobrze przewodzi ciepło. Na przepływ ciepła równania podobne do przestrzega równań falowych dla rozchodzenia się dźwięku w powietrzu. Po wprowadzeniu ciepła przemieszcza się z prędkością 20 m s -1 w 1,8 K w helu II . Fale te nazywane są drugim dźwiękiem .
W przeciwieństwie do zwykłych cieczy, hel II pełza po powierzchniach, najwyraźniej nawet wbrew grawitacji . Ucieknie z niezamkniętego pojemnika, czołgając się na boki, chyba że napotka mniej zimne miejsce, w którym wyparuje. Bez względu na powierzchnię porusza się w warstwie około 30 nm . Film ten nazywa się filmem Rollina , ku pamięci fizyka, który go scharakteryzował, Bernarda V. Rollina. W wyniku tego efektu i zdolności helu II do szybkiego przechodzenia przez małe otwory trudno jest ograniczyć ciekły hel. Jeśli naczynie nie jest sprytnie skonstruowane, hel II będzie wspinał się po ścianach i przechodził przez zawory, aż dotrze do cieplejszego obszaru, w którym wyparuje. Fale rozchodzące się wzdłuż filmu Rollinsa podlegają tym samym równaniom, co fale w płytkiej wodzie, ale siłą przywracającą jest siła van der Waalsa, a nie grawitacja. Fale te znane są jako trzeci dźwięk .
Solidny
Hel krzepnie dopiero pod wpływem silnych ciśnień. Powstałe praktycznie niewidoczne i bezbarwne ciało stałe jest wysoce ściśliwe; kompresja laboratoryjna może zmniejszyć jej objętość o ponad 30%. Z sześciennego modułu sprężystości rzędu 5 x 10 7 Pa jest pięćdziesiąt razy bardziej ściśliwe niż woda. W normalnych warunkach ciśnienia, w przeciwieństwie do innych pierwiastków, hel nie krzepnie i pozostaje płynny do zera absolutnego . Hel stałej wymaga minimalnego ciśnienia około 26 atm . Często trudno jest odróżnić hel stały od ciekłego, ponieważ ich współczynniki załamania światła są prawie identyczne. Ciało stałe ma wysokie ciepło utajone (ciepło topnienia) i heksagonalną strukturę krystaliczną, taką jak woda.
Właściwości chemiczne
Jak wszystkie gazy szlachetne , hel ma pełną warstwę walencyjną, co oznacza bardzo niską reaktywność chemiczną. Ponieważ nie ma zdolnych do reagowania podwarstw, jest (wraz z neonem ) najmniej reaktywnym ze wszystkich ciał prostych .
Hel może jednak tworzyć nietrwałe związki ( ekscymery ) z wolframem, jodem, fluorem, siarką i fosforem w fazie plazmy , przez wyładowanie lub w inny sposób. W ten sposób powstały He Ne , Hg He 10 , W He 2 oraz jony molekularne He 2 + , He 2 ++ , HeH + , He D + . Technika ta umożliwiła również produkcję obojętnej cząsteczki He 2 , która ma większą liczbę układów pasm oraz HgHe , której kohezja wydaje się zależeć wyłącznie od sił polaryzacyjnych . Teoretycznie możliwe są również inne składniki, takie jak fluorowodorek helu (HHe F ). W 2013 roku helidek litu LiHe powstał w stanie gazowym metodą ablacji laserowej w bardzo niskiej temperaturze ( 1 do 5 K ).
Pierwsze sprawdzone związki stabilne hel endohedral kompleksy fulerenów , jak He @ C 60 , w której atom hel jest uwięziony w klatce C 60 fulerenu . Od tego czasu wykazano, że przy bardzo wysokim ciśnieniu (powyżej 113 GPa ) możliwe jest utworzenie trwałego związku helu i sodu Na 2 He . Takie molekuły można również znaleźć w wysokociśnieniowych olbrzymach, takich jak Jowisz i Saturn .
Z wnętrza Ziemi wyłania się (w lawach i gazach wulkanicznych ) hel bogaty w hel 3 , który uważa się za pierwotny (tj. nabyty podczas formowania się Ziemi , prawie 4,6 miliarda lat temu ). Gdyby był w stanie gazowym lub rozpuszczony w minerałach dolnego płaszcza, miałby wystarczająco dużo czasu na prawie całkowite odgazowanie, biorąc pod uwagę jego lotność i temperatury wewnątrz Ziemi. Dlatego musi być przechowywany jako trwały minerał w warunkach dolnego płaszcza , ale żadne nie są znane. Obliczenie 2018 entalpii swobodnej tysiąca hipotetycznych lecz możliwych helu związków przewidzieć jedną (i tylko jedną), wolny związek o entalpii wystarczająco małe do pułapki helu w płaszczu zamiast opuszczeniu. Wolne, dwutlenek żelaza i hel FeO 2 On.
Właściwości biologiczne
Hel, neutralny w normalnych warunkach, jest nietoksyczny, nie odgrywa żadnej roli biologicznej i występuje w śladowych ilościach w ludzkiej krwi. Jeśli wdychana jest wystarczająca ilość tlenu, aby usunąć tlen niezbędny do normalnego oddychania , możliwe staje się uduszenie .
Inhalacja
| Plik audio | |
| Tekst czytany helem | |
| Jeśli to konieczne, użyj klawisza poprzedniej strony przeglądarki na końcu rozprawy . (en) Hel to bezbarwny, bezwonny, bez smaku, nietoksyczny, obojętny jednoatomowy pierwiastek chemiczny, który stoi na czele szeregu gazów szlachetnych w układzie okresowym i którego liczba atomowa wynosi 2. Jego temperatury wrzenia i topnienia są najniższe wśród pierwiastków i istnieje tylko jako gaz, z wyjątkiem ekstremalnych warunków . | |
| Trudności w korzystaniu z tych mediów? | |
|---|---|
Głos osoby, która wdychała hel, chwilowo zmienia ton w kierunku wysokich harmonicznych – hel jest trzykrotnie mniej gęsty niż powietrze, dlatego prędkość dźwięku staje się wyższa – a podstawowa częstotliwość d 'wnęki wypełnionej gazem jest proporcjonalna do prędkości dźwięku, inhalacja hel odpowiadają wzrostu w częstotliwości rezonansowych w urządzeniu fonacyjny które modulują częstotliwości podstawowej danych przez struny głosowe . Odwrotny efekt, obniżenie barwy, można uzyskać poprzez wdychanie gęstszego gazu, takiego jak sześciofluorek siarki .
Wdychanie czystego helu w małych dawkach jest zwykle bezpieczne, ponieważ jest to gaz obojętny . Jednak stosowanie helu sprzedawanego w handlu, takiego jak ten używany do nadmuchiwania balonów, może być niebezpieczne ze względu na wiele zanieczyszczeń, które może zawierać, ślady innych gazów lub aerozole oleju smarowego.
Wdychanie nadmiaru helu może być niebezpieczne, ponieważ hel jest po prostu środkiem duszącym , który zastępuje tlen niezbędny do normalnego oddychania. Oddychanie czystym helem powoduje uduszenie w ciągu kilku minut. Wdychanie helu bezpośrednio z butli pod ciśnieniem jest niezwykle niebezpieczne ze względu na wysoki przepływ, który może powodować uraz ciśnieniowy, który rozdziera tkankę płuc i może być śmiertelny. Jednak ten wypadek jest dość rzadki, ponieważ w Stanach Zjednoczonych były tylko dwa zgony w latach 2000-2004.
Pod wysokim ciśnieniem (powyżej 20 atm lub 2 MPa ) mieszanina helu i tlenu dwutlenkowego ( helioksu ) może prowadzić do syndromu nerwowego wysokiego ciśnienia , który jest rodzajem efektu przeciwdziałającego znieczuleniu. Dodając trochę azotu do mieszanki, można uniknąć problemu. Niemniej jednak, w nurkowaniu podwodnym, syndromowi nerwowemu wysokiego ciśnienia można przeciwdziałać jedynie przez dodanie wodoru , przy czym dodanie azotu jest wysoce narkotyczne, gdy tylko całkowite ciśnienie osiągnie 5 barów.
Zastosowanie terapeutyczne
Hel podaje się w mieszaninach zawierających minimum 20% tlenu ditlenku pacjentom z niedrożnością górnych lub dolnych dróg oddechowych. Niska lepkość helu pozwala więc na ograniczenie pracy oddechowej.
bezpieczeństwo
Środki bezpieczeństwa dla helu kriogenicznego są podobne do tych wymaganych dla ciekłego azotu ; jego wyjątkowo niska temperatura może powodować zimne oparzenia .
Wdychanie dużej ilości za jednym razem powoduje lekkie uduszenie , co prowadzi do krótkiej, ale niebezpiecznej utraty przytomności . Istnieją również przypadki zatorowości mózgu lub poważnych problemów z płucami u osób, które wdychają hel pod ciśnieniem.
Ponadto, szybkość rozszerzania się pomiędzy fazą ciekłą a fazą gazową jest taka, że może powodować wybuchy w przypadku gwałtownego parowania, jeśli nie jest zainstalowane urządzenie ograniczające ciśnienie.
Zbiorniki gazowego helu o temperaturze 5 - 10 K również powinny być traktowane tak, jakby zawierały ciekły hel, ze względu na dużą i szybką rozszerzalność cieplną, która ma miejsce, gdy hel poniżej 10 K jest wprowadzany w temperaturze pokojowej.
Zastosowania
Pomimo wysokiej ceny, hel ma wiele zastosowań wymagających niektórych jego unikalnych właściwości, takich jak niska temperatura wrzenia , niska gęstość , niska rozpuszczalność , wysoka przewodność cieplna, czy też jego chemicznie i biologicznie obojętny charakter . Występuje w handlu w postaci ciekłej lub gazowej. W postaci płynnej można spotkać małe zbiorniki zwane dewarami , które mogą pomieścić do 1000 l helu, lub duże zbiorniki ISO o pojemnościach nominalnych do 40 000 l . W postaci gazowej małe ilości helu dostarczane są w butlach wysokociśnieniowych o pojemności do 8,5 m 3 w standardzie, natomiast duże ilości dostarczane są w cysternach ciśnieniowych, które mogą mieć pojemność do 5000 m 3 w standardzie.
Przemysłowy
Ze względu na swoją obojętność, wysoką przewodność cieplną , jego przezroczystość dla neutronów i ponieważ nie tworzy izotopów radioaktywnych w reaktorach, hel jest używany jako płyn przenoszący ciepło w niektórych reaktorach jądrowych chłodzonych gazem cieplnym .
Hel jest wykorzystywany jako atmosfera ochronna podczas wzrostu krzemu monokrystalicznego do produkcji układów scalonych i światłowodów , do produkcji tytanu i cyrkonu oraz w chromatografii gazowej , ponieważ jest obojętny.
Ze względu na swoją bezwładność chemiczną, idealne właściwości termodynamiczne i kaloryczne , dużą prędkość dźwięku i duży współczynnik Laplace'a , jest również przydatny w naddźwiękowych tunelach aerodynamicznych lub w instalacjach badających zjawiska przejściowe.
Te same właściwości pozwalają na stosowanie go w uszczelnionych dyskach twardych w celu zwiększenia ich pojemności. Ponieważ żadne uszczelnienie nie jest doskonałe, dyski te mają detektor, który sygnalizuje utratę helu, która z czasem jest niebezpieczna dla dysku.
Hel zmieszany z cięższym gazem, takim jak ksenon, jest przydatny w chłodnictwie termoakustycznym , ze względu na duży stosunek pojemności cieplnych i niską liczbę Prandtla . Bezwładność chemiczna helu ma korzyści dla środowiska w porównaniu z innymi systemami chłodniczymi, które przyczyniają się do powstania dziury ozonowej lub globalnego ocieplenia .
Ponieważ dyfunduje przez ciała stałe trzy razy szybciej niż powietrze, hel jest używany do wykrywania nieszczelności w urządzeniach o bardzo wysokiej próżni lub zbiornikach wysokociśnieniowych.
Jest również stosowany z produktami spożywczymi (dodatek do żywności dopuszczony przez Unię Europejską pod numerem referencyjnym E939 ) w celu umożliwienia kontroli szczelności opakowania (patrz lista dodatków do żywności ).
Naukowcy
Zastosowanie helu zmniejsza efekty zniekształceń spowodowanych zmianami temperatury w przestrzeni między soczewkami niektórych teleskopów lub okularów , ze względu na wyjątkowo niski współczynnik załamania światła . Metodę tę stosuje się zwłaszcza w teleskopach słonecznych, które podlegają znacznym wahaniom temperatury, ale dla których obudowa podtrzymująca różnicę ciśnień między atmosferą a próżnią byłaby zbyt ciężka.
Wiek skał i minerałów zawierających uran i tor można oszacować, mierząc zawartość helu w procesie zwanym datowaniem helowym .
Ciekły hel jest również używany do chłodzenia niektórych metali do ekstremalnie niskich temperatur wymaganych dla nadprzewodnictwa , na przykład magnesów nadprzewodzących stosowanych w szczególności w detektorach MRI . LHC w CERN wykorzystuje 120 t ciekłego helu, aby utrzymać temperaturę magnesów 1,9 K . Ogólnie rzecz biorąc, w kriogenice stosuje się niskotemperaturowy hel .
Komercyjne i rekreacyjne
Mieszaniny helu, takie jak trimiks , helioks i hel, ze względu na niską rozpuszczalność w tkance nerwowej , są używane do nurkowania głębokiego w celu zmniejszenia skutków narkozy azotowej . Na głębokościach większych niż 150 m do mieszaniny helu z tlenem dodawane są niewielkie ilości wodoru, aby przeciwdziałać syndromowi nerwowemu wysokiego ciśnienia .
Na tych głębokościach niska gęstość helu znacznie zmniejsza wysiłek oddechowy.
Do laserów He-Ne mają różne zastosowania, zwłaszcza czytniki kodów kreskowych .
Sterowce, balony i rakiety
Ponieważ hel jest lżejszy od powietrza, może być używany do nadmuchiwania sterowców i balonów swobodnych lub na uwięzi. Chociaż wodór ma około 7% większą nośność, hel ma tę zaletę, że jest niepalny (a nawet opóźniający palenie).
Eksploracja atmosfery, w szczególności dla meteorologii, odbywa się za pomocą balonów, w większości napompowanych helem.
W technologii rakietowej hel jest wykorzystywany jako czynnik wyporowy do zarządzania paliwem i utleniaczem w zbiornikach mikrograwitacyjnych poprzez zwiększanie ciśnienia oraz do zapewnienia mieszanki wodoru i tlenu, która zasila dysze napędowe. Służy również do usuwania tych substancji z urządzeń naziemnych przed startem oraz do wstępnego schładzania ciekłego wodoru z pojazdów kosmicznych . Na przykład rakieta Saturn V zużyła do startu około 370 000 m 3 helu.
Zasoby helu i oczyszczanie
Naturalna obfitość
Hel jest drugim po wodorze najobficiej występującym pierwiastkiem w znanym Wszechświecie i stanowi 23% jego masy barionowej . Ogromna większość helu powstała w wyniku pierwotnej nukleosyntezy w ciągu kilku minut po Wielkim Wybuchu . Dlatego pomiar jej liczebności pomaga ustalić pewne parametry modeli kosmologicznych. Przez większość istnienia gwiazd powstaje w wyniku syntezy jądrowej wodoru. Pod koniec życia gwiazdy wykorzystują hel jako surowiec do tworzenia cięższych pierwiastków w znacznie szybszych, nawet wybuchowych procesach. Ostatecznie hel we Wszechświecie pochodzi tylko z bardzo małej części gwiazd.
W atmosferze ziemskiej stężenie helu wynosi 5,2 × 10-6 objętości. To niskie stężenie jest dość stałe w czasie, ze względu na równowagę między ciągłą produkcją helu w skałach a ucieczką w kosmos przez różne mechanizmy . W ziemskiej heterosferze , część górnych warstw atmosfery, hel i inne lekkie gazy są najliczniejszymi składnikami.
Prawie cały hel na Ziemi pochodzi z radioaktywności alfa . Występuje głównie w związkach uranu i toru , m.in. blendy smolistej , karnotycie i monazycie , ponieważ emitują cząstki α , będące jądrami zjonizowanego helu He 2+ , które natychmiast neutralizują elektronami. Szacuje się, że w litosferze produkuje się rocznie 3000 t helu . W skorupie ziemskiej stężenie helu wynosi 8 × 10-6 objętości. W wodzie morskiej jest to tylko 4 × 10 -12 . Niewielkie ilości znajdują się również w wodzie mineralnej , gazach wulkanicznych i żelazie meteorytowym . Ponieważ hel jest uwięziony jak gaz ziemny przez nieprzepuszczalne warstwy skalne, najwyższe stężenia helu występują w polach gazu ziemnego, z których pozyskuje się większość komercyjnego helu. Jego stężenie objętościowe w stosunku do gazu ziemnego waha się od kilku części na milion do 7% stężenia zidentyfikowanego w hrabstwie San Juan w stanie Nowy Meksyk .
W 2016 roku firma o nazwie „Helium” poinformowała, że zidentyfikowała w Tanzanii trzy możliwe ogromne złoża tego pierwiastka , na tyle duże – według niej – by zaopatrywać świat na kilkadziesiąt lat, i z tego powodu poszukuje 40 mln dolarów inwestycji, aby spróbować odwiertów w Tanzanii w 2017 roku. Niektórzy eksperci uważają jednak, że eksploatacja tego złoża przez długi czas nie byłaby opłacalna, ponieważ według nich rynek światowy wszedł ostatnio w okres nadprodukcji ze względu na bardziej ekonomiczne użytkowanie i największy rynek w Stanach Zjednoczonych , Katarze i Rosji .
Ekstrakcja i oczyszczanie
W przypadku zastosowania na dużą skalę hel jest pozyskiwany przez destylację frakcyjną z gazu ziemnego, który może zawierać do 7%. Ponieważ hel ma niższą temperaturę wrzenia niż jakiekolwiek inne ciało, niska temperatura i wysokie ciśnienie są wykorzystywane do skraplania prawie wszystkich innych gazów (głównie azotu i metanu ). Powstały surowy hel jest następnie oczyszczany przez wystawienie na coraz niższe temperatury, co wytrąca praktycznie cały azot i inne pozostałe gazy z mieszaniny gazów. Na koniec węgiel aktywny jest używany do końcowego etapu oczyszczania, aby w ten sposób otrzymać hel o jakości 99,995%. Głównym zanieczyszczeniem helu klasy A jest neon . Aby zakończyć oczyszczanie, większość wyprodukowanego helu jest upłynniana w procesie kriogenicznym. Skraplanie jest konieczne w przypadku zastosowań wykorzystujących ciekły hel, a ponadto umożliwia dostawcom helu obniżenie kosztów transportu na odległość, ponieważ większe zbiorniki ciekłego helu mają pojemność co najmniej pięć razy większą niż większe przyczepy przewożące butle z helem pod ciśnieniem a .
W 2005 roku około 160 milionów metrów sześciennych helu wydobyto z gazu ziemnego lub wydobyto ze złóż, z czego około 83% ze Stanów Zjednoczonych , 11% z Algierii, a resztę głównie z Rosji i Polski . W Stanach Zjednoczonych większość helu wydobywa się z gazu ziemnego w Hugoton i sąsiednich złóż w Kansas, Oklahomie i Teksasie.
Inną metodą produkcji i oczyszczania helu jest dyfuzja surowego gazu ziemnego przez półprzepuszczalne membrany lub inne bariery.
Możliwe jest zsyntetyzowanie helu przez bombardowanie litu lub boru protonami o wysokiej energii, ale nie jest to ekonomicznie opłacalna metoda produkcji.
Historia
Odkrycie
Pierwsze oznaki obecności helu obserwuje się na 18 sierpnia 1868Jako jasnożółtego paskiem przy długości fali z 587.49 nm w widmie w chromosferze na słońcu . Linia ta została wykryta przez francuskiego astronoma Julesa Janssena podczas całkowitego zaćmienia w Guntur (Indie) . Początkowo uważa się, że ta linia to sód . 20 październikatego samego roku angielski astronom Norman Lockyer zaobserwował żółtą linię w widmie słonecznym, którą nazwał linią Fraunhofera D 3 , ze względu na jej bliskość do dobrze znanych linii D 1 i D 2 sodu. Dochodzi do wniosku, że jest to spowodowane przez nieznany na Ziemi pierwiastek Słońca. Lockyer i angielski chemik Edward Frankland nazwali ten pierwiastek od greckiego słowa oznaczającego Słońce, ἥλιος ( helios ).
W 1882 roku Luigi Palmieri po raz pierwszy zdołał zademonstrować obecność helu na Ziemi poprzez analizę spektralną lawy z Wezuwiusza .
26 marca 1895 rBrytyjski chemik Sir William Ramsay izoluje hel na Ziemi, traktując kleveit (odmiana mieszanki smolistej , zawierającej co najmniej 10% metali ziem rzadkich ) kwasami mineralnymi. Ramsay szukał argon , ale po oddzieleniu azotu i tlenu z gazu, uwolniony od kwasu siarkowego , zauważył, że jasnożółty linii w spektroskopu będącym jednocześnie z D linii 3 obserwowane w widmie słonecznym.
Próbki te zostały zidentyfikowane jako hel przez Lockyera i brytyjskiego fizyka Williama Crookesa . Niezależnie od tego, w tym samym roku jest on wyizolowany z kleweita przez chemików Pera Theodora Cleve'a i Abrahama Langleta (w) w Uppsali , którzy zgromadzili wystarczającą ilość gazu, aby móc dokładnie określić jego masę atomową .
Hel został również wyizolowany przez amerykańskiego geochemika Williama Francisa Hillebranda , kilka lat przed odkryciem Ramsaya, zauważając niezwykłe linie spektralne podczas badania próbki uninitu. Ale Hillebrand przypisuje te linie azotowi. Jego list gratulacyjny do Ramsaya przedstawia interesujący przypadek odkrycia i bliskiego odkrycia w nauce.
W 1907 r. Ernest Rutherford i Thomas Royds wykazali, że cząstki α są jądrami helu, pozwalając cząstkom na wejście przez cienkie szklane okienko w rurce, z której się ewakuowały, a następnie tworząc wyładowanie w rurce, aby zbadać widmo nowego gazu w to. W 1908 roku hel został po raz pierwszy skroplony przez holenderskiego fizyka Heike Kamerlingha Onnesa , poprzez schłodzenie gazu poniżej 1 K . Próbuje go zestalić przez dalsze obniżenie temperatury, ale mu się to nie udaje, ponieważ hel nie ma punktu potrójnego . Jest to uczeń Onnesa, Willem Hendrik Keesom , któremu w 1926 roku udaje się zestalić pod ciśnieniem 1 cm 3 helu.
W 1938 r. sowiecki fizyk Piotr Leonidowicz Kapitsa odkrył, że hel-4 w temperaturach bliskich zeru absolutnego prawie nie ma lepkości, co nazywa się obecnie nadciekłością. W 1972 roku to samo zjawisko zaobserwowano w helu 3 , ale w temperaturze znacznie bliższej zera absolutnego, przez amerykańskich fizyków Douglasa D. Osheroffa , Davida M. Lee i Roberta C. Richardsona . Zjawisko w helu 3 jest interpretowane jako tworzenie się par atomów, które są fermionami , w bozony , analogicznie do par elektronów Coopera na podstawie nadprzewodnictwa .
Produkcja i zastosowania
Po odwiertach naftowych w 1903 r. w Dexter w stanie Kansas wytworzony strumień gazu był niepalny. Erasmus Haworth (w) , geolog stanu Kansas, zebrał próbki wytworzonego gazu i przywiózł je na University of Kansas , Lawrence . Z pomocą chemików Hamiltona Cady (en) i Davida McFarlanda ustalono, że gaz, objętościowo, zawiera 72% podtlenku azotu, 15% metanu (procent palny tylko przy większej ilości tlenu) i 12% niezidentyfikowanego gazu. Dalsza analiza pokazuje Cady i McFarland, że 1,84% próbki gazu to hel. Pokazuje to, że pomimo globalnego niedoboru na Ziemi, hel jest skoncentrowany w dużych ilościach pod Wielkimi Równinami Amerykańskimi i dostępny do produkcji jako produkt uboczny eksploatacji gazu ziemnego. Największe rezerwy helu znajdują się na polu Hugoton oraz na sąsiednich polach w południowo-zachodnim Kansas z rozszerzeniami do Teksasu i Oklahomy.
Dzięki temu Stany Zjednoczone stały się wiodącym światowym producentem helu. Zgodnie z sugestią Sir Richarda Threlfalla (w) Marynarka Wojenna Stanów Zjednoczonych dotuje trzy małe eksperymentalne zakłady produkcyjne helu podczas I wojny światowej . Celem jest zaopatrzenie balonów na uwięzi w ten niepalny gaz, lżejszy od powietrza. W ramach tego programu wytwarza się łącznie 5700 m 3 92% helu, chociaż wcześniej w sumie wyprodukowano mniej niż 100 litrów . Część tego gazu jest używany do pierwszego na świecie wypełniony helem sterowiec US Navy C-7, otwarty na jego dziewiczego rejsu z Hampton Roads w Wirginii do Bolling Field w Waszyngtonie na1 st grudzień 1921.
Chociaż proces skraplania gazu w niskich temperaturach nie został opracowany wystarczająco wcześnie, aby odegrać znaczącą rolę podczas I wojny światowej, produkcja będzie kontynuowana. Hel służy przede wszystkim do nadmuchiwania balonów . Takie zastosowanie zwiększy zapotrzebowanie podczas II wojny światowej , podobnie jak zapotrzebowanie na spawanie łukowe .
Spektrometr masowy hel jest również niezbędna do Manhattan projektu bomby atomowej.
Rząd Stanów Zjednoczonych utworzony w 1925 roku Narodowy Hel Reserve w Amarillo , Teksas , w celu dostarczania Aerostaty, personel wojskowy w czasie wojny, i cywilów w czasie pokoju. Ze względu na embargo wojskowe Stanów Zjednoczonych na Niemcy, dostawy helu były tam ograniczone, a Hindenburg musiał być napompowany wodorem, z katastrofalnymi konsekwencjami, jakie nastąpiły po jego spaleniu. Zużycie helu po II wojnie światowej spadło, ale w latach 50. zwiększono rezerwę, aby zapewnić dostawy ciekłego helu do startów rakiet podczas wyścigu kosmicznego i zimnej wojny . W 1965 roku zużycie helu w Stanach Zjednoczonych przekroczyło ośmiokrotnie maksimum, jakie osiągnęło w czasie wojny.
Po poprawkach do ustawy o helu z 1960 r. (Prawo publiczne 86-777 ), Biuro Kopalń Stanów Zjednoczonych założyło pięć prywatnych fabryk do wydobywania helu z gazu ziemnego. W ramach tego programu ochrony helu Biuro buduje rurociąg o długości 684 km z Bushton w stanie Kansas do Cliffside, w pobliżu częściowo wyeksploatowanego pola Amarillo. Dostarczona w ten sposób mieszanina helowo-dwuazotowa jest wstrzykiwana i przechowywana do momentu, w którym jest potrzebna, po czym jest ekstrahowana i oczyszczana.
W 1995 roku zebrano miliard metrów sześciennych gazu, ale rezerwa ma 1,4 miliarda dolarów długu, co skłoniło Kongres Stanów Zjednoczonych w 1996 roku do stopniowego zaprzestania działalności. Wynikający Helium Prywatyzacja Act of 1996 (Public Law 104-273) kieruje się Departament Zasobów Wewnętrznych Stanów Zjednoczonych , aby rozpocząć opróżniania rezerwy w 2005 r.
Hel wyprodukowany w latach 1930-1945 miał czystość około 98,3% (~ 2% azotu), co było idealne dla aerostatów. W 1945 roku wyprodukowano niewielką ilość 99,9% helu do wykorzystania w spawaniu łukowym. Już w 1949 roku dostępne były ilości handlowe 99,995% helu klasy A.
Przez kilka lat Stany Zjednoczone wyprodukowały ponad 90% dostępnego na rynku helu na świecie, a pozostałe zakłady wydobywcze w Kanadzie, Polsce, Rosji i innych krajach. W tym tempie, zgodnie z badaniem (sierpień 2010), rezerwy Stanów Zjednoczonych skończą się przed 2040 r. (prawie 1/3 światowego zapotrzebowania pokrywają Stany Zjednoczone, których globalne moce produkcyjne wynoszą ok. 142 mln m sześc. (w 2010 r.) przy zużyciu 180 mln m sześc. i że hel wydaje się "niezbędny do większości jego zastosowań" ).
W połowie -1990s nowa fabryka rozpoczęła produkcję w Arzew , Algieria . Przy 1,7 × 107 m 3 rocznie może pokryć całe europejskie zapotrzebowanie, czyli około 16% światowej produkcji. Tymczasem, pobór w Stanach Zjednoczonych przekroczyła 15000 t w roku 2000. W latach 2004-2006, dwie inne rośliny zbudowany jedna Ras Laffan ( Katar ) wytwarzanie 9,2 ton ciekłego helu w ciągu dnia, to znaczy 1,88 x 10 7 m 3 rocznie a drugi w Skikda (Algieria). Algieria szybko stała się drugim co do wielkości producentem helu. W tym okresie wzrosło zużycie i koszty produkcji helu. W latach 2002-2007 ceny helu podwoiły się, a tylko w 2008 r. główni dostawcy podnieśli ceny o około 50% . Wiąże się to z bardzo niską produkcją i zużyciem helu, co utrudnia ich dorównanie, ponieważ niewielu producentów chce inwestować w ten „ rynek niszowy ”.
Robert Richardson ( Nagroda Nobla w dziedzinie fizyki ) w 2010 r. zaalarmował społeczność międzynarodową o ryzyku niedoboru, argumentując za wzrostem cen, aby odzwierciedlić niedobór tego pierwiastka i mniej go marnować .
Firma 45-8 Energy z siedzibą w Metz złożyła w październiku 2019 roku wyłączne pozwolenie na poszukiwania helu w południowo-zachodniej części departamentu Nièvre we Francji. Odpowiedź prefektury spodziewana jest we wrześniu 2020 r.
Uwagi i referencje
- (fr) Ten artykuł jest częściowo lub w całości zaczerpnięty z anglojęzycznego artykułu Wikipedii zatytułowanego " Helium " ( zobacz listę autorów ) .
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 th ed. , 2804 s. , Oprawa twarda ( ISBN 978-1-420-09084-0 )
- (w) Beatriz Cordero Verónica Gómez, Ana E. Platero-Prats, Marc Revés Jorge Echeverría, Eduard Cremades, Flavia i Santiago Barragan Alvarez , „ Kowalentne promienie ponownie ” , Dalton Transactions ,2008, s. 2832 - 2838 ( DOI 10.1039 / b801115j )
- „Ionization Energies of Atoms and Atomic Ions” w CRC Handbook of Chemistry and Physics, wydanie 91 (wersja internetowa 2011), red. WM Haynes, CRC Press / Taylor and Francis, Boca Raton, FL., P. 10-203
- (en) Robert H. Perry i Donald W. Green , Perry's Chemical Engineers' Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 pkt. ( ISBN 0-07-049841-5 ) , s. 2-50
- „Hel” w Banku Danych o Substancjach Niebezpiecznych , dostęp 1 maja 2010
- Baza danych Chemical Abstracts zapytana przez SciFinder Web 15 grudnia 2009 r. ( wyniki wyszukiwania )
- Arkusz Sigma-Aldrich związku Hel ≥99,995% , konsultowany 17 sierpnia 2018 r.
- „ Hel ” w bazie produktów chemicznych Reptox z CSST (Quebec organizacji odpowiedzialnej za bezpieczeństwo i higienę pracy), dostęp 25 kwietnia 2009
- Paul Depovere, Układ okresowy pierwiastków. Podstawowy cud Wszechświata , De Boeck Supérieur ,2002, s. 103.
-
(en) Eric Hand, „ Masywne pola helu znalezione w strefie ryftowej Tanzanii ” , Science , tom. 353 n O 6295,8 lipca 2016, s. 109-110 ( DOI 10.1126 / science.353.6295.109 , czytanie online
 , dostęp 11 lipca 2016 ).
, dostęp 11 lipca 2016 ).
- Audrey Chauvet, „ Światowe rezerwy helu spadają ” , na www.20minutes.fr ,30 sierpnia 2010(dostęp 22 czerwca 2019 ) .
- (en) John Emsley , Nature's building blocks: an AZ guide to the elements , Oxford New York, Oxford University Press ,2001, 538 pkt. ( ISBN 978-0-19-850340-8 i 978-0-198-50341-5 , OCLC 248877093 , czytaj online ) , s. 175–179.
-
(w) Achim Weiss, „ Elementy przeszłości: Nukleosynteza i obserwacja Wielkiego Wybuchu ” , Instytut Fizyki Grawitacyjnej im. Maxa Plancka (dostęp 23 czerwca 2009 ) ;.
(en) A. Coc i in. , „ Zaktualizowana Nukleosynteza Wielkiego Wybuchu skonfrontowana z obserwacjami WMAP i obfitością elementów świetlnych ” , The Astrophysical Journal , tom. 600,2004, s. 544 ( DOI 10.1086/380121 ). -
(w) Don L. Anderson, GR Foulger Anders Meibom, „ Podstawy helu ” , MantlePlumes.org MantlePlumes.org,
2006(dostęp 20 lipca 2008 ) .
Tylko
streszczenie. Przedmiot oferowany do sprzedaży. - (w) Aaron Novick , „ Półokres życia trytu ” , „ Physical Review” , tom. 72, 1947, s. 972 ( DOI 10.1103 / PhysRev.72.972.2 , przeczytaj online )Dostęp ograniczony dla subskrybentów PROLA.
- (w) GN Zastenker i E. Salerno, F. Buehler, P. Bochsler, M. Bassi, YN Agafonov, NA Eismont, VV Khrapchenkov, H. Busemann , „ Skład izotopowy i obfitość międzygwiazdowego neutralnego helu na podstawie pomiarów bezpośrednich ” , Astrofizyka , tom. 45 N O 2kwiecień 2002, s. 131–142 ( DOI 10.1023/A: 1016057812964 , przeczytaj online ) Tylko streszczenie . Przedmiot oferowany do sprzedaży.
- (w) „ Lunar Mining of Helium-3 ” , Instytut Technologii Fuzji Uniwersytetu Wisconsin-Madison, 2007(dostęp 9 lipca 2008 r . ) .
- (en) EN Slyuta AM Abdrakhimov EM Galimov, " Oszacowanie prawdopodobnych rezerw helu-3 w regolicie księżycowym w Lunar and Planetary Science XXXVIII " [PDF] ,2007(dostęp 23 czerwca 2009 ) .
- (w) Eric R. Hedman , „ Fascynująca godzina z Geraldem Kulcińskim ” , The Space Review ,16 stycznia 2006( przeczytaj online ).
- (w) Peter Häussinger1 Reinhard Glatthaar2 Wilhelm Rhode3 Helmut Kick4 Christian Benkmann5 Josef Weber6 Hans-Jörg Wunschel7 Viktor Stenke8 Edith Leicht9 Hermann Stenger10, Noble gas , Wiley-VCH Verlag GmbH & Co , et al. „ Encyklopedia Chemii Przemysłowej Ullmanna ”,15 marca 2001( prezentacja online ).
- (i) LW Brandt (Clifford A. Hampel, red.) Encyclopedia of pierwiastków , Reinhold Book Corporation , Nowy Jork, 1968, rozdz. "Hel" , s. 256–268 .
- (w) Ray F. Weiss , „ Rozpuszczalność helu i neonu w wodzie i wodzie morskiej ” , J. Chem. inż. Dane , obj. 16 N O 21971, s. 235–241 ( DOI 10.1021 / je60049a019 )Pierwsza strona.
- (w) Jack A. Stone i Alois Stejskal , „ Wykorzystywanie helu jako wzorca refrakcji ” , Metrologia , tom. 41,2004, s. 189-197 ( DOI 10.1088/0026-1394 / 41/3/012 ) Streszczenie .
- (w) Encyklopedia pierwiastków chemicznych , op. cyt. , s. 261 .
- (w) F. Buhler i WI Axford, HJA Chivers, K. Martin , „ Izotopy helu w zorzy rocznej ” , J. Geophys. Res. , tom. 81, n o 1,1976, s. 111–115 ( DOI 10.1029 / JA081i001p00111 ) Streszczenie .
- (en) Encyklopedia pierwiastków chemicznych , op. cyt. str. 262 .
- (w) PC Hohenberg i PC Martin , " Mikroskopowa teoria helu nadciekłego " , Roczniki Fizyki , tom . 281, n kość 1-2,Październik 2000, s. 636-705 ( DOI 10.1006 / aphy.2000.6019 ) Streszczenie . Artykuł dostępny dla subskrybentów ScienceDirect.
- (w) Encyklopedia pierwiastków , op. cyt. , s. 263 .
- (w) HA Fairbank i CT Lane , „ Stawki Rollin Film w płynnym helu ” , Physical Review , tom. 76 N O 8,Październik 1949, s. 1209–1211 ( DOI 10.1103 / PhysRev.76.1209 ) Streszczenie . Przedmiot oferowany do sprzedaży.
- (w) BV Rollin i F. Simon , " O filmie" "fenomen ciekłego helu II " , Physica , tom. 6, N O 21939, s. 219–230 ( DOI 10.1016 / S0031-8914 (39) 80013-1 ) Streszczenie . Artykuł dostępny dla subskrybentów ScienceDirect.
- (w) Fred Ellis, „ Trzeci dźwięk ” , Wesleyan Quantum Fluids Laboratory ,wrzesień 2005(dostęp 23 czerwca 2009 ) .
- (w) D. Bergman , „ Hydrodynamika i trzeci cienki dźwięk w filmach He II ” , Physical Review , tom. 188 n o 1,Październik 1949, s. 370-384 ( DOI 10.1103 / PhysRev.188.370 ) Streszczenie . Dostępne dla abonentów PROLA lub na sprzedaż.
- (en) „ Układ okresowy: hel ” (dostęp 23 czerwca 2009 ) .
- (w) Naima Tariq Nada Taisan, Vijay Singh i Jonathan Weinstein, „ Spektroskopowe wykrywanie cząsteczki LiHe ” , „ Physical Review Letters” , tom. 110 n O 15,8 kwietnia 2013 r., s. 153201 ( PMID 25167262 , DOI 10.1103 / PhysRevLett.110.153201 , przeczytane online , dostęp 10 grudnia 2017 ).
- SB „ helu wiąże sodowy wysokiego ciśnienia ”, służące do nauki , N O 474kwiecień 2017, s. 10.
- (w) Xiao Dong, Artem R. Oganov i in. , " Stabilny związek helu i sodu pod wysokim ciśnieniem " , Nature Chemistry ,6 lutego 2017( przeczytaj online )
- " Chemia helu, nieznana na Ziemi, może istnieć na gigantycznych planetach " , na futura-sciences.com ,9 lutego 2017(dostęp 9 lutego 2017 )
- (w) Jurong Jian Zhang LV Hefei Li Feng Xiaolei Cheng Lu et al. , „ Rzadki związek zawierający hel FeO 2 He stabilizowany w warunkach głębinowych ” , Physical Review Letters , tom. 121 n O 25,21 grudnia 2018 r., s. 1-6, poz n o 255.703 ( DOI 10,1103 / PhysRevLett.121.255703 , czytać online [PDF] ).
- (w) R. Mark Wilson, „ Związek zawierający hel głęboko wewnątrz Ziemi został znaleziony obliczeniowo ” , Physics Today ,10 stycznia 2019( DOI 10.1063 / PT.6.1.20190110a ).
- (w) " Skupienie: Dom dla helu wewnątrz Ziemi " , Fizyka (w) , tom. 11,21 grudnia 2018 r.Artykuł n o 133 ( czytać online ).
- (w) J. Ackerman i G. Maitland , „ Obliczanie względnej prędkości dźwięku w mieszaninie gazów ” , Undersea Biomed. Res. , tom. 2, n O 4,grudzień 1975, s. 305-310 ( czytaj online ).
- (w) Joe Wolfe, „ Fizyka w mowie ” , phys.unsw.edu.au. (dostęp 23 czerwca 2009 ) .
- Dlaczego hel zmienia głos? na futura-sciences.com .
- (en) Martin Grassberger i Astrid Krauskopf , „ Suicidal uduszenie helem: Sprawozdanie z trzech przypadków. Suizid mit Helium Gas: Bericht über drei Fälle. » , Wiener Klinische Wochenschrift , tom. 119, nr . 9-102007, s. 323–325 ( DOI 10.1007 / s00508-007-0785-4 )Podsumowanie w języku niemieckim. Dostępna pierwsza strona. Przedmiot oferowany do sprzedaży.
- (w) Daniel Engber, „ Trzymaj się z dala od balonu! " , Slate.com,2006(dostęp 23 czerwca 2009 ) .
- (w) JC Eostain , C. Lemaire , MC-Gardette Chauffour , J. Doucet i R. Naquet , „ Oszacowanie ludzkiej podatności na zespół nerwowy wysokiego ciśnienia ” , Journal of Applied Physiology , tom. 54, n o 4,Kwiecień 1983, s. 1063-1070 ( czytaj online )Dostępne w abonamencie osobistym lub instytucjonalnym.
- (w) WL Hunger Jr. i PB Bennett , „ Przyczyny, mechanizmy i zapobieganie syndromowi wysokiego ciśnienia nerwowego ” , Undersea Biomedical Research , tom. 1, N O 1,1974, s. 1-28 ( ISSN 0093-5387 , OCLC 2068005 , PMID 4619860 , czytaj online ).
- (w) Glenn Considine D. (red.), Van Nostrand Encyclopedia of Chemistry , Wylie-Interscience, ( ISBN 0-471-61525-0 ) , rozdz. "Hel" , s. 764–765 .
- (w) IE Beckwith i CG Miller III , „ Aerotermodynamika i przejście w szybkim tunelu aerodynamicznym w Langley NASA ” , Roczny przegląd mechaniki płynów , tom. 22,1990, s. 419–439 ( DOI 10.1146 / annurev.fl.22.010190.002223 ).
- (w) CI Morris, Shock Induced Combustion in High Speed Wedge Flows , Stanford University Thesis , 2001 [ przeczytaj online (dostęp 23 czerwca 2009)] .
- https://www.lemondeinformatique.fr/actualites/lire-un-disque-dur-helium-16-to-pour%C2%A0datacenter%C2%A0chez-toshiba-75335.html
- (w) James R. Belcher i William V. Slaton, Richard Raspet Henry E. Bass, Jay Lightfoot , „ Gazy robocze w silnikach termoakustycznych ” , The Journal of the Acoustical Society of America , tom. 105 n O 5,1999, s. 2677-2684 ( DOI 10.1121 / 1.426884 )Dostępne w ramach subskrypcji.
- (w) Arjun Makhijani Kevin Gurney, Naprawa dziury ozonowej: nauka, technologia i polityka , MIT Press , 1995 ( ISBN 0-262-13308-3 ) .
- (w) H. Jakobsson , „ Symulacja dynamiki wielkiego ziemskiego teleskopu słonecznego ” , „ Astronomical & Astrophysical Transactions” , tom. 13, n o 1,1997, s. 35–46 ( DOI 10.1080 / 10556799708208113 ) Streszczenie . Artykuł subskrypcyjny.
- (w) O. Engvold i RB Dunn RN Smartt, WC Livingston , „ Testy próżni VS hel w teleskopie słonecznym ” , Applied Optics , tom. 22,1983, s. 10-12 ( DOI 10.1364 / AO.22.000010 , przeczytaj online ) Streszczenie . Przedmiot oferowany do sprzedaży.
- (w) „ CERN-LHC: Fakty i liczby – Przewodnik po broszurze LHC ” ( Archiwum • Wikiwix • Archive.is • Google • Co robić ) [PDF] , CERN (dostęp 23 czerwca 2009 ) .
- (w) " Kriogenika: Niska temperatura, wysoka wydajność | CERN ” , na home.cern (dostęp 7 lutego 2019 r . ) .
- (w) B. Fowler i KN Ackles, G. Porlier , „ Skutki narkozy gazów obojętnych to zachowanie-A Critical Review ” , Undersea Biomedical Research Journal ,1985( PMID 4082343 , przeczytaj online ).
- (w) JR Thomas , „ Odwrócenie narkozy azotowej u szczurów przez ciśnienie helu ” , Undersea Biomed. Res. , tom. 3 n o 3,1976, s. 249-259 ( PMID 969027 , czytaj online ).
- (en) JC Eostain i MC-Gardette Chauffour, C. Lemaire, R. Naquet , „ Skutki H 2 -He-O 2mieszanina na HPNS do 450 msw ” , Undersea Biomed. Res. , tom. 15 N O 4,1988, s. 257-270 ( ISSN 0093-5387 , OCLC 2068005 , PMID 3212843 , czytaj online ).
- (w) Scott J. Butcher i Richard L. Jones, Jonathan R. Mayne, Timothy C. Hartley, Stewart R. Petersen , „ Upośledzona mechanika wentylacji podczas ćwiczeń z samodzielnym aparatem oddechowym poprawia się dzięki helioksie ” , European Journal of Fizjologia Stosowana , Holandia, Springer, tom. 101 N O 6,grudzień 2007, s. 659-669 ( DOI 10.1007 / s00421-007-0541-5 )Pierwsza strona za darmo, artykuł ograniczony do subskrybentów Springera.
- (en) Albert Stwertka, Przewodnik po elementach: Revised Edition , Oxford University Press , New York, 1998, ( ISBN 0-19-512708-0 ) , s. 24 .
- (w) BM Oliver i James G. Bradley, Harry Farrar IV , „ Stężenie helu w niższych warstwach atmosfery Ziemi ” , Geochimica i Cosmochimica Acta , tom. 48 N O 9,1984, s. 1759-1767 ( DOI 10.1016 / 0016-7037 (84) 90030-9 ) Bezpłatne streszczenie , artykuł dostępny w subskrypcji ScienceDirect.
- (w) „ Atmosfera: wprowadzenie do JetStream — internetowej szkoły pogody ” , National Weather Service , 29 sierpnia 2007 r. (dostęp 23 czerwca 2009 r . ) .
- (i) o. Lie-Svendsen i MH Rees , „ Ucieczka helu z atmosfery ziemskiej: mechanizm wypływu jonów ” , Journal of Geophysical Research , tom. 101 n O A21996, s. 2435-2444 ( DOI 10.1029 / 95JA02208 ) Streszczenie , artykuł w abonamencie AGU.
- (w) Nick Strobel, " Notatki astronomiczne Nicka Strobla rozdz. Atmosfery ” ,2007(dostęp 23 czerwca 2009 ) .
- (w) Melvin A. Cook , „ Gdzie jest radiogeniczny hel Ziemi? » , Przyroda , tom. 179,1957, s. 213 ( DOI 10.1038 / 179213a0 ) Streszczenie , przedmiot oferowany do sprzedaży.
- (w) LT Aldrich i Alfred O. Nier , „ Wystąpienie Hebr. 3w naturalnych źródłach helu ” , Phys. Obrót silnika. , tom. 74,1948, s. 1590-1594 ( DOI 10.1103 / PhysRev.74.1590 ) Streszczenie , artykuł w abonamencie PROLA.
- (w) P. Morrison i J. Pine , „ Radiogeniczne pochodzenie izotopów helu w skale ” , Annals of the New York Academy of Sciences , tom. 62, n o 3,1955, s. 71-92 ( DOI 10.1111 / j.1749-6632.1955.tb35366.x )Brak streszczenia , podziękowania, artykuł na temat subskrypcji Wiley InterScience.
- (w) RE Zartman , „ Hel argon i węgiel w gazach ziemnych ” , Journal of Geophysical Research , tom. 66, n o 1,1961, s. 277-306 ( DOI 10.1029 / JZ066i001p00277 , przeczytaj online )W abonamencie AGU lub w sprzedaży.
- (w) Ronald F. Broadhead , „ Hel w Newmexico – zapotrzebowanie na dystrybucję geologii i możliwości eksploracji zasobów ” , New Mexico Geology , tom. 27 N O 4,2005, s. 93-10 ( czytaj online [PDF] ).
- (en) Hand, E (2016) Ogromne pola helu znalezione w ryftach Tanzanii ; Nauka 08 lipca 2016: obj. 353, wydanie 6295 , s. 109-110 DOI : 10.1126/nauka.353.6295.109 .
- (w) Mark Winter, „ Hel: podstawy ” , University of Sheffield ,2008(dostęp 23 czerwca 2009 ) .
- (w) Encyklopedia pierwiastków chemicznych , op. cyt. , s. 258 .
- (en) EM Smith i TW Goodwin, J. Schillinger , „ Wyzwania dla światowych dostaw helu w następnej dekadzie ” , Postępy w inżynierii kriogenicznej , tom. 49A, N O 710, 2003, s. 119-138 ( DOI 10.1063 / 1.1774674 , przeczytaj online [PDF] ).
- (w) „ Podsumowania surowców mineralnych – hel ” [PDF] , US Geological Survey ,2004(dostęp 23 czerwca 2009 ) .
- (en) VP Belyakov , SG Durgar'yan, BA Mirzoyan i in. , „ Technologia membran – nowy trend w przemysłowej separacji gazów ” , Inżynieria chemiczna i naftowa , tom. 17, n o 1,Dziewiętnaście osiemdziesiąt jeden, s. 19-21 ( DOI 10.1007 / BF01245721 )Pierwsza strona za darmo, kontynuacja w abonamencie SpringerLink lub płatna.
- (w) PI Dee i ETS Walton , „ Fotograficzne badanie transmutacji litu i boru przez protony i jony litu przez ciężki izotop wodoru ” , Proceedings of the Royal Society of London , tom. 141 N O 8451933, s. 733-742 ( DOI 10.1098/rspa.1933.0151 )Płatny lub subskrypcyjny dostęp dla osób niebędących członkami Royal Society .
- (w) RK Kochhar , „ Francuscy astronomowie w Indiach w XVII-XIX wieku ” , Journal of the British Astronomical Association , tom. 101 n O 21991, s. 95-100 ( czytaj online ).
- (w) Encyklopedia pierwiastków chemicznych , op. cyt. , s. 256 .
- (w) William Thomson, Frankland i Lockyer znajdują żółte wypukłości, aby dać bardzo jasną linię Zdecydowałem niedaleko od bramki D Do tej pory nie utożsamiano z żadnym ziemskim płomieniem. Wydaje się wskazywać na nową substancję, którą proponują nazwać Helem. , Rep. Brytyjczyk. dr hab. xcix , 1872.
- definicja Cleveitis .
- (w) Encyklopedia pierwiastków , op. cyt. , s. 257 .
- (w) William Ramsay , „ był gaz ukazujący widmo helu, rzekomą przyczynę D3, jednej z linii w widmie koronalnym. Uwaga wstępna ” , Proceedings of the Royal Society of London , tom. 58,1895, s. 65-67 ( DOI 10.1098 / rspl.1895.0006 )Płatne lub w ramach subskrypcji dla osób niebędących członkami Royal Society .
- (w) William Ramsay , „ Hel, gazowy składnik niektórych minerałów”. Część I ” , Proceedings of the Royal Society of London , tom. 58,1895, s. 80-89 ( DOI 10.1098 / rspl.1895.0010 )Płatne lub w ramach subskrypcji dla osób niebędących członkami Royal Society.
- (w) William Ramsay , „ Hel, gazowy składnik niektórych minerałów”. Część II ” , Proceedings of the Royal Society of London , tom. 59,1895, s. 325-330 ( DOI 10.1098 / rspl.1895.0097 )Płatne lub w ramach subskrypcji dla osób niebędących członkami Royal Society .
- (De) NA Langlet , " Das Atomgewicht des Heliums " , Zeitschrift für anorganische Chemie , tom. 10, n o 1,1895, s. 289-292 ( DOI 10.1002 / zaac.18950100130 )W sprzedaży lub w ramach subskrypcji Wiley InterScience.
- (w) ER Weaver, Chemia przemysłowa i inżynierska , 1919, rozdz. „ Bibliografia Literatury Helowej ” .
- (w) Pat Munday, American National Biography , John A. Garraty i Mark C. Carnes (red.), Oxford University Press , 1999 „ Wpis biograficzny WF Hillebranda (1853-1925), geochemika i administratora amerykańskiego Biura Standardów » , tom. 10-11, s. 227–228 .
- (w) Dirk van Delft , „ Mały kubek helu, wielka nauka ” , Fizyka dzisiaj ,2008, s. 36-42 ( czytaj online [PDF] ).
- (w) " Coldest Cold " , Time Inc. ,1929(dostęp 23 czerwca 2009 ) .
- (w) P. Kapitza , " Lepkość ciekłego helu λ poniżej punktu " , Nature , tom. 141,1938, s. 74 ( DOI 10.1038 / 141074a0 ).
- (w) DD Osheroff i RC Richardson, DM Lee , „ Dowód nowej fazy Solid Heb 3 ” , Phys. Obrót silnika. Łotysz. , tom. 28 N O 141972, s. 885–888 ( DOI 10.1103 / PhysRevLett.28.885 ) Streszczenie . Artykuł chroniony prawem autorskim PROLA.
- (w) DF McFarland , „ Skład gazu ze studni w Dexter, Kan ” , Transakcje Akademii Nauk Kansas , tom. 19,1903, s. 60-62 ( DOI 10.2307 / 3624173 , czytaj online )Pierwsza strona. Pełny artykuł na warunkach JSTOR.
- (w) „ Odkrycie helu w gazie ziemnym ” , Amerykańskie Towarzystwo Chemiczne ,2004(dostęp 23 czerwca 2009 ) .
- (w) HP Cady i DF McFarland , „ Hel w gazie ziemnym ” , Science , tom. 24,1906, s. 344 ( DOI 10.1126 / nauka.24.611.344 )Brak abstraktu . Przedmiot na sprzedaż lub członkowie AAAS.
- (w) HP Cady i DF McFarland , „ Hel w gazie ziemnym Kansas ” , Transakcje Kansas Academy of Science , tom. 20,1906, s. 80–81 ( DOI 10.2307 / 3624645 , przeczytaj online [ archiwum z27 maja 2012] )<Brak abstraktu . Artykuł na warunkach JSTOR.
- (w) Eugene M. Emme, (red.) Aeronautics and Astronautics: An American Chronology of Science and Technology in the Exploration of Space, 1915-1960 , NASA , Washington, DC, 1961 [ dostęp online (dostęp 23 czerwca 2009) )] , rozdz. „ Aeronautyka i Astronautyka Chronologia 1920–1924 ” , s. 11-19 .
- (w) N. Hilleret, S. Turner (red.) CERN Accelerator School, technologia próżniowa: materiały: Centrum Konferencyjne Scanticon, Snekersten, Dania, 28 maja - 3 czerwca 1999 , CERN , Genewa, Szwajcaria, 1999 [ czytaj linię ( strona konsultowana 23 czerwca 2009)] , rozdz. „ Wykrywanie nieszczelności ” , s. 203–212 . „Początek metody wykrywania wycieków helu należy prześledzić wstecz do Projektu Manhattan i bezprecedensowych wymagań dotyczących uszczelnienia zakładów separacji uranu. Czułość wymagana do weryfikacji szczelności doprowadziła do wyboru spektrometru mas zaprojektowanego przez dr AOC Niera i skalibrowanego na masę helu. "
- (w) John G. Williamson , „ Energia dla Kansas ” , Transakcje Kansas Academy of Science , Kansas Academy of Science , tom. 71, n o 4,zima 1968, s. 432-438 ( czytaj online )Pierwsza strona. Pełny artykuł na warunkach JSTOR.
- (w) - , " Konserwacja sprzedaży helu " , Rejestr Federalny , tom. 70, n o 1936 października 2005, s. 58464 ( przeczytaj online [PDF] ).
- (w) „ Streszczenie: Wpływ sprzedaży federalnej rezerwy helu ” , nap.edu ( ISBN 978-0-309-07038-6 , dostęp 23 czerwca 2009 ) .
- (w) PV Mullins, RM Goodling Helium , Bureau of Mining / Minerals Yearbook 1949, 1951 [ czytany online (dostęp 21 czerwca 2009)] , s. 599-602 .
- (w) studium Sprzedaż narodowych rezerw helu ,sierpień 2010.
- (w) GR Matos, JB Peterson, „ Helium End User Statistic ” , US Geological Survey (dostęp 23 czerwca 2009 ) .
- (w) Karen H. Kaplan , „ Niedobór helu utrudnia badania i przemysł ” , Physics Today , American Institute of Physics , tom. 60, n o 6,czerwiec 2007, s. 31-32 ( DOI 10.1063 / 1.2754594 , czytaj online ).
- (w) kwaskowaty Basu i Philip Yam (red.) , " Aktualizacje: w powietrzu " , Scientific American , Scientific American, Inc. , Vol. 297 n O 4,październik 2007, s. 18 ( przeczytaj online ).
- Ludovic Pillevesse, „ Prefektura udzieli lub nie we wrześniu wyłącznego zezwolenia na badania helu w Nièvre ”, Le journal du Center ,31 sierpnia 2020 r.( przeczytaj online )
Zobacz również
Bibliografia
w. (en) Z. Cai, R. Clarke, N. Ward, WJ Nuttall, BA Głowacki, „ Modelowanie rynków helu ” [PDF] , University of Cambridge ,2007(dostęp 22 czerwca 2009 ) .
Powiązane artykuły
- Nadciekłość
- Kriogeniki
- Chemia gazu szlachetnego
- Calefaction lub efekt Leidenfrosta
- Konserwowanie mięsa
- Wykrywanie nieszczelności
-
Metastabilny hel

Linki zewnętrzne
- Tekst skomentował „ Odkrycie ciekłego helu w 1908 r. przez Kamerlingha ” , BibNum (konsultowane 21 czerwca 2009 r. ) .
- (pl) „ Dane techniczne dla helu ” (dostęp 23 kwietnia 2016 ) , ze znanymi danymi dla każdego izotopu na podstronach
- Ewidencja organów :
- Uwagi w ogólnych słownikach lub encyklopediach :
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | Hej | |||||||||||||||||||||||||||||||
| 2 | Li | Być | b | VS | NIE | O | fa | Urodzony | |||||||||||||||||||||||||
| 3 | nie dotyczy | Mg | Glin | tak | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | To | Sc | Ti | V | Cr | Mn | Fe | Współ | Lub | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Tak | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Płyta CD | W | Sn | Sb | ty | ja | Xe | |||||||||||||||
| 6 | Cs | Ba | To | Pr | Nd | Po południu | Sm | Miał | Bóg | Tb | Dy | Ho | Er | Tm | Yb | Czytać | Hf | Twój | W | Re | Kość | Ir | Pt | W | Hg | Tl | Pb | Bi | Po | W | Rn | ||
| 7 | Fr | Ra | Ac | Cz | Rocznie | U | Np | Mógłby | Jestem | Cm | Bk | cf | Jest | Fm | Md | Nie | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
|
Metale alkaliczne |
Ziemia alkaliczna |
Lantanowce |
Metale przejściowe |
Słabe metale |
metalem loids |
Długoterminowe metale |
geny halo |
Gazy szlachetne |
Przedmioty niesklasyfikowane |
| aktynowce | |||||||||
| Superaktynowce | |||||||||