Kwas octowy
| Kwas etanowy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wzór szkieletowy i trójwymiarowa reprezentacja kwasu octowego | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nazwa IUPAC | kwas etanowy | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nazwa systematyczna | kwas octowy | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonimy |
lodowaty |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O ECHA | 100 000 528 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O WE | 200-580-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O RTECS | AF1225000 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kod ATC | G01 S02 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DrugBank | DB03166 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 176 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 15366 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E260 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 2006 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| UŚMIECHY |
CC (= O) O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C2H4O2 / c1-2 (3) 4 / h1H3, (H, 3,4) / f / h3H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd | bezbarwna ciecz o ostrym zapachu i silnym occie. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości chemiczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formula |
C 2 H 4 O 2 [Izomery] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa cząsteczkowa | 60,052 ± 0,0025 g / mol C 40%, H 6,71%, O 53,29%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| pKa | 4,76 w 25 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moment dwubiegunowy | 1,70 ± 0,03 D. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Średnica molekularna | 0,442 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości fizyczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuzja | 16,64 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| * Temperatura wrzenia | 117,9 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozpuszczalność | Mieszalny z wodą, acetonem , alkoholem, benzenem , glicerolem , eterem, czterochlorkiem węgla ; Praktycznie bezczelny. w disiarczku węgla | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametr rozpuszczalności δ | 20,7 MPa 1/2 ( 25 ° C ); 18.9 J 1/2 cm -3/2 ( 25 ° C ); |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
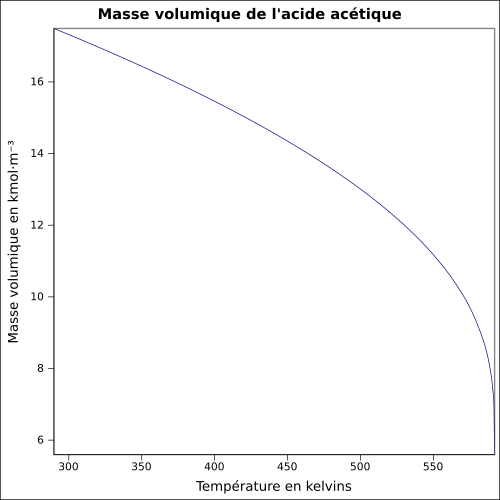
| Masa objętościowa |
1,049 2 g cm −3 (ciecz, 20 ° C )
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura samozapłonu | 465 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura zapłonu | 39 ° C (zamknięty tygiel) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Granice wybuchowości w powietrzu | 5,4–16 % obj | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nasycenie prężności par |
1,5 kPa w 20 ° C
równanie:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lepkość dynamiczna | 1,22 mPa s w 25 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punkt krytyczny | 4,53 MPa w 319,56 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochemia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gaz S 0 , 1 bar | 282,848 J mol −1 K −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 ciecz, 1 bar | 158,0 J mol −1 K −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gaz Δ f H 0 | −433 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 ciecz | −483,52 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 11,728 kJ mol - 1 do 16,75 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 23,7 kJ mol -1 do 117,95 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
123,1 J mol −1 K −1 (ciecz, 25 ° C ) 63,44 J mol −1 K −1 (gaz, 25 ° C ) równanie:
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SZT | 874,2 kJ mol −1 (ciecz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | −875,16 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości elektroniczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 energia re jonizacji | 10,65 ± 0,02 eV (gaz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalografia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klasa kryształu lub grupa kosmiczna | Pna 21 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametry siatki |
a = 13,151 Å b = 3,923 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tom | 297,27 A 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości optyczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Współczynnik załamania światła | 1.3720 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Środki ostrożności | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Niebezpieczeństwo H226, H314, P280, P305, P310, P338, P351, H226 : Łatwopalna ciecz i pary H314 : Powoduje poważne oparzenia skóry i uszkodzenia oczu P280 : Nosić rękawice ochronne / odzież ochronną / ochronę oczu / ochronę twarzy. P305 : W przypadku dostania się do oczu: P310 : Natychmiast skontaktować się z OŚRODKIEM ZATRUĆ lub lekarzem. P338 : Wyjąć soczewki kontaktowe, jeśli ofiara je nosi i można je łatwo zdjąć. Kontynuuj płukanie. P351 : Ostrożnie płukać wodą przez kilka minut. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  B3, E, B3 : Temperatura zapłonu cieczy palnej = 39 ° C zamknięty tygiel (metoda nie została podana) E : Materiał żrący Transport towarów niebezpiecznych: klasa 8 Ujawnienie przy 1,0% zgodnie z wykazem ujawnień składników |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 3 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
83 : korozyjnego lub wykazujące pewną niewielką korozyjności i par (temperatura zapłonu 23 do 60 ° C włącznie z wartościami granicznymi), numer UN : 2789 : roztworem kwasu octowego, zawierający więcej niż 80 procent (masowy) kwasu; lub GLACIAL ACETIC ACID Klasa: 8 Etykiety: 8 : Substancje żrące 3 : Ciecze łatwopalne Opakowanie: Grupa pakowania II : substancje średnio niebezpieczne;  
80 : żrący lub wykazujący niewielki stopień korozyjności Numer UN : 2790 : KWAS OCTOWY W ROZTWORZE Klasa: 8 Etykieta: 8 : Substancje żrące Opakowanie: Grupa pakowania II / III : substancje umiarkowanie / nieznacznie niebezpieczne.  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoksykologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | 3,31 g kg -1 (szczur, doustnie ) 525 mg kg -1 (mysz, iv ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | -0,31 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Próg zapachu | niski: 0,03 ppm wysoki: 0,15 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Związki pokrewne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izomery | Aldehyd glikolowy | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inne związki | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednostki SI i STP, chyba że określono inaczej. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Etanowego lub kwas octowy jest kwas karboksylowy o teoretycznym łańcuch węglowy C2, podobnie jak etan , masa cząsteczkowa 60 g / mol i wzór chemiczny surowy C 2 H 4 O 2 , częściowo rozwinięty CH 3 - CO-OH lub AcOH krótki formacji , w którym Ac oznacza „ CH 3 CO ”, z grupy acetylowej . Przymiotnik nazwy zwyczajowej pochodzi od łacińskiego acetum , oznaczającego ocet . Rzeczywiście, kwas octowy jest głównym składnikiem octu po wodzie, ponieważ nadaje mu kwaśny smak i ostry zapach wykrywalny od 1 ppm .
Destylacja octu, poświadczona od średniowiecza w Europie, umożliwiła otrzymanie czystego kwasu octowego, bezbarwnej palnej cieczy o silnym zapachu octu, o gęstości około 1,05 g cm- 3 w temperaturze 20 ° C, która krzepnie przez zwykłe zanurzenie w łaźni wodnej z lodem. Nadal jest znany jako lodowaty kwas octowy lub wcześniej silny ocet . Jest to pierwszy znany kwas przemysłowy.
Ta bardzo słabo przewodząca, bezbarwna, łatwopalna i higroskopijna ciecz stanowi obok kwasu mrówkowego w temperaturze pokojowej jeden z najprostszych kwasów monokarboksylowych . Jego kwasowość charakteryzowana w roztworze wodnym przez pK a = 4,76 wynika z jego zdolności do czasowej utraty protonu swojej funkcji karboksylowej , przekształcając go w ten sposób w jon octanowy CH 3 COO - . To słaby kwas .
Kwas ten koaguluje lateks i posiada właściwości bakteriostatyczne, dzięki czemu może być stosowany jako środek dezynfekujący. Znajduje również zastosowanie jako składnik insektycydów i środków czyszczących do produkcji półprzewodników. Działa żrąco, a jego opary działają drażniąco na nos i oczy.
Działa silnie żrąco na tkanki organiczne i żywe, dlatego należy się z nim obchodzić ostrożnie. Chociaż nie stwierdzono, aby był rakotwórczy ani szkodliwy dla środowiska, może powodować oparzenia, a także trwałe uszkodzenie ust, nosa, gardła i płuc. W określonych dawkach i przy przewlekłej równoczesnej ekspozycji z produktem rakotwórczym, jego drażniący charakter sprawia, że jest on promotorem guzów nowotworowych (łagodnych i złośliwych). Zostało to zademonstrowane eksperymentalnie na szczurach.
W organizmie ludzkim kwas octowy jest normalnie wytwarzany po spożyciu alkoholu : etanol przekształca się w aldehyd octowy, który następnie pod wpływem enzymu dehydrogenazy acetaldehydu przekształca się w kwas octowy, a następnie w acetylo-coA przez ligazę octan-CoA.
Produkcja
Globalne zapotrzebowanie na kwas octowy wynosi około 6,5 mln ton rocznie (Mt / rok). W przemyśle jest wytwarzany przez utlenianie n- butanu w fazie ciekłej lub odzyskiwany przy produkcji octanu celulozy lub polialkoholu winylowego .
Używa
Jest odczynnikiem szeroko stosowanym w przemyśle czy laboratoriach, aw szczególności:
- jako rozpuszczalnik: miesza się z wodą i różnymi rozpuszczalnikami organicznymi, takimi jak etanol , eter dietylowy , glicerol, ale nierozpuszczalny w dwusiarczku węgla , jest również dobrym rozpuszczalnikiem dla gum , żywic , fosforu , siarki i kwasów halogenowodorowych ? ;
- w produkcji bezwodnika octowego , octanu celulozy , monomeru octanu winylu i innych octanów, a także leków , pestycydów , barwników , produkcji wyrobów fotograficznych;
- w żywności (produkcja octów owocowych itp.), dodatek do żywności ;
- tekstylnych ;
- jako środek czyszczący (do półprzewodników );
- koagulant ( naturalny lateks );
- bakteriostatyczny (w roztworze);
- w produkcji tworzyw sztucznych, takich jak politereftalan etylenu (PET) lub octan celulozy , przydatnych do produkcji octanu winylu (farby, kleje) i rozpuszczalników organicznych;
- jako dodatek do wyrobów tytoniowych ( aromat ).
- wytrawianie podczas barwienia skrawków histologicznych (np. barwienie karminowo-zielone )
- proces hydrolizy , kondensacji i / lub żelowania podczas wytwarzania katalizatora lub podczas procesu zol-żel
- przeciwbakteryjne i zakwaszenie żołądka w hodowli, zwłaszcza świń.
Nomenklatura
Dawne trywialne nazwa pochodzi od kwasu octowego octu słowa Łacińskiej co oznacza ocet lub aceti-Vinum . Nadal jest najczęściej używany we francuskojęzycznym i anglojęzycznym świecie, ale IUPAC ujednolicił termin kwas etanowy zamiast starej francuskiej nazwy chemicznej kwas etylowy . Bardziej tolerancyjni niż nomenklatura IUPAC z 1960 r., Chemical Abstracts zachowała jednak nazwy zwyczajowe dla pierwszych dwóch kwasów karboksylowych w C1 i C2, kwas mrówkowy i kwas octowy.
Lodowaty kwas octowy to również banalna nazwa, która powszechnie odnosi się do czystego kwasu octowego w laboratorium. Podobnie jak w przypadku niemieckiej nazwy „Eisessig” (dosłownie: ocet mrożony), nazwa ta jest wyjaśniona przez przypominające lód kryształki kwasu octowego, które tworzą się w temperaturze nieco poniżej temperatury pokojowej (poniżej 17 ° C). , Temperatura topnienia czystego kwasu octowego kwas).
Najczęstszym skrótem dla kwasu octowego jest AcOH lub HOAc, Ac, oznaczający acetylową grupę funkcyjną CH 3 −CO−.
Surowy wzór kwasu octowego to C 2 H 4 O 2 . Często jest też napisane CH 3 COOH lub CH 3 CO 2 H, aby lepiej przetłumaczyć jego strukturę. Jon powstały w wyniku utraty protonu H + nazywany jest octanem. Octan może również odnosić się do soli zawierającej ten anion lub do estru kwasu octowego.
Historyczny
Mocny ocet jest znany w Mezopotamii od ponad 3000 lat przed naszą erą. AD . Te bakterie kwasu octowego do wytwarzania kwasu octowego z winem i tlen zostały opisane przez aptekarza Pasteur . Są obecne w całym cywilizowanym świecie, a każda kultura, która warzy piwo lub wino , nieuchronnie odkryła ocet, naturalny wynik ewolucji tych napojów alkoholowych pozostawionych na otwartej przestrzeni.
Stosowanie kwasu octowego w chemii sięga starożytności. Na III th century BC. AD , grecki filozof Theophrastus opisuje, jak ocet działa na metal i w ten sposób wytwarza pigmenty przydatne w sztuce, w tym biały ołów ( węglan ołowiu ) i patyną , zieloną mieszaninę soli miedzi, w tym octan miedzi II (wszystkie produkty toksyczne ). Starożytni Rzymianie gotowali „ kwaśne wino ” w ołowianych naczyniach, aby uzyskać bardzo słodki syrop zwany sapa . SAPA bogaty w octan ołowiu , słodki substancja zwana cukier ołowiu lub Saturn cukru i która spowodowała liczne zatrucia ołowiu w rzymskiej arystokracji The choroba odpowiada ostrym lub przewlekłym ołowiu zatrucia jest szczególnie nazwie Zatrucie . Perski alchemik Jabir Ibn Hayyan (Geber) stężonego kwasu octowego z octem przez destylację .
W okresie renesansu „lodowaty” kwas octowy otrzymywano metodą suchej destylacji octanów metali. Na XVI p wieku niemiecki alchemik Andreas Libavius do opisanego i porównano czystego kwasu tak wytworzonej kwaśny. Obecność wody w occie ma taki wpływ na właściwości kwasu octowego, że przez wieki wielu chemików uważało, że lodowaty kwas octowy i kwas octowy to dwie różne substancje. To francuski chemik Pierre Auguste Adet udowodnił, że są to ten sam związek chemiczny.
W 1847 roku niemiecki chemik Hermann Kolbe po raz pierwszy zsyntetyzował kwas octowy z materiałów nieorganicznych. Sekwencja reakcji był chlorowanie z dwusiarczku węgla z czterochlorkiem węgla , a następnie przez pirolizę na czterochloroetylenu i chlorującym wody w kwasie trichlorooctowym i ostatecznie kończą się na redukcji poprzez elektrolizę w celu uzyskania kwasu octowego.
Do 1910 r. Większość lodowatego kwasu octowego otrzymywano z „piroligneous ługu” wytwarzanego przez destylację drewna. Kwas octowy wyodrębniono działając wodorotlenkiem wapnia , a otrzymany w ten sposób octan wapnia zakwaszono następnie przez dodanie kwasu siarkowego w celu zreformowania kwasu octowego. W tym czasie Niemcy produkowały go rocznie 10 000 ton, z czego 30% wykorzystano do produkcji barwnika indygo .
Właściwości fizykochemiczne
Kwasowość
Atom wodoru (H) grupy karboksylowej (–COOH) kwasów karboksylowych, takich jak kwas octowy, może zostać uwolniony jako jon H + ( proton ). To właśnie zdolność uwalniania tego protonu nadaje mu kwasowość. Kwas octowy jest słabym kwasem , mono- protonowej w roztworze wodnym, o pK od około 4,8 do 25 ° C . Roztwór o stężeniu 1,0 mol / l (stężenie octu domowego) ma pH 2,4, co oznacza, że dysocjuje tylko 0,4% cząsteczek kwasu octowego.
Cykliczny dimer
Struktura krystaliczna kwasu octowego pokazuje, że cząsteczki łączą się w dimery połączone wiązaniami wodorowymi . Te dimery można zaobserwować w postaci gazowej w temperaturze 120 ° C . Prawdopodobnie występują również w fazie ciekłej czystego kwasu octowego, ale szybko ulegają rozpadowi przy najmniejszej obecności wody. Ta dimeryzacja występuje w innych kwasach karboksylowych. Odbywa się to także w wodnym roztworze z stała asocjacji K D , którego wartość jest bliska 1.
Rozpuszczalnik
Ciekły kwas octowy jest hydrofilowym ( polarnym ) rozpuszczalnikiem protonowym , podobnym do etanolu i wody . Przy średniej stałej dielektrycznej 6,2 może rozpuszczać nie tylko związki polarne, takie jak sole nieorganiczne i cukry , ale także związki niepolarne, takie jak oleje, czy czyste substancje, takie jak siarka i diod . Łatwo miesza się z wieloma innymi polarnymi lub niepolarnymi rozpuszczalnikami, takimi jak woda, chloroform lub heksan . Te właściwości rozpuszczalnika i mieszalność kwasu octowego sprawiają, że jest on szeroko stosowany w przemyśle chemicznym.
Reakcje chemiczne
Kwas octowy powoduje korozję wielu metali , w tym żelaza , magnezu i cynku . Tworzy wodór i sole metali zwane octanami . Z aluminium utworzonego po zetknięciu z tlenem cienka warstwa tlenku glinu jest stosunkowo odporna, która pokrywa jego powierzchnię. Dlatego do transportu kwasu octowego często stosuje się zbiorniki aluminiowe. Octany metali mogą być wytwarzane z mieszaniny kwasu octowego i odpowiedniej zasady, jak w przypadku wodorowęglanu sodu + octu reakcji co daje wody i CO 2 . Z godnym uwagi wyjątkiem octanu chromu (II) , prawie wszystkie octany są rozpuszczalne w wodzie.
- Mg ( s ) + 2 CH 3 COOH ( aq ) → (CH 3 COO) 2 Mg (aq) + H 2 ( g )
- NaHCO 3 (s) + CH 3 COOH (aq) → CH 3 COONa (aq) + CO 2 (g) + H 2 O ( l )

Kwas octowy również podlega typowym reakcjom kwasów karboksylowych , w szczególności tworzeniu etanolu przez redukcję i tworzeniu pochodnych, takich jak chlorek acetylu, przez nukleofilową substytucję acylu . Wśród innych pochodnych zastępczych jest bezwodnik octowy . Ten bezwodnik jest wynikiem utraty jednej cząsteczki wody przez dwie cząsteczki kwasu octowego. Estry kwasu octowego może zostać wyszkolony przez estryfikację Fischera , a to może być również stosowane do wytwarzania amidów . Podgrzany do temperatury powyżej 440 ° C kwas octowy rozkłada się na dwutlenek węgla i metan lub wodę i keten .
Wykrycie
Kwas octowy można rozpoznać po jego charakterystycznym zapachu. Sole kwasu octowego rozpuszczone w roztworze chlorku żelaza (III) dają ciemnoczerwony kolor, który znika po zakwaszeniu. Ogrzewając octany trójtlenkiem arsenu , uzyskuje się tlenek kakodylu, który można rozpoznać po jego śmierdzących oparach.
Biochemia
Grupa acetylowa pochodząca z kwasu octowego ma fundamentalne znaczenie dla biochemii prawie każdego życia. Kiedy związana koenzymu A , to ma zasadnicze znaczenie w metabolizmie z węglowodanów i tłuszczów . Jednak stężenie wolnego kwasu octowego w komórkach jest utrzymywane na niskim poziomie, aby nie zakłócać kontroli pH. W przeciwieństwie do innych kwasów karboksylowych o długim łańcuchu węglowym ( kwasy tłuszczowe ), kwas octowy nie występuje w tworzeniu naturalnych trójglicerydów . Istnieje sztuczny trójgliceryd kwasu octowego, triacetyna (trioctan glicerylu), który jest powszechnie stosowany jako dodatek do żywności (w kosmetykach, żywności i niektórych lekach) oraz jako rozpuszczalnik .
Kwas octowy jest naturalnie wytwarzany i wydzielany przez niektóre bakterie, w szczególności Acetobacter i Clostridium acetobutylicum (en), a także drożdże Saccharomyces cerevisiae .
Bakterie te są obecne w niektórych produktach spożywczych, wodzie, mleku ( bakterie kwasu mlekowego ) i glebie , a kwas octowy powstaje naturalnie, gdy rozkładają się owoce lub inne produkty spożywcze. Kwas octowy jest również składnikiem nawilżenia pochwy u ludzi i innych naczelnych , gdzie wydaje się działać jako środek przeciwbakteryjny .
Produkcja i synteza
Kwas octowy jest wytwarzany syntetycznie lub w wyniku fermentacji bakteryjnej. Obecnie metoda ekologiczna dotyczy tylko 10% produkcji, ale pozostaje ważna przy produkcji octu, ponieważ w większości krajów prawo stanowi, że ocet spożywczy musi być pochodzenia organicznego. Około 75% kwasu octowego celem przemysłu chemicznego jest wytwarzany przez karbonylowanie w metanolu , szczegóły poniżej. Reszta składa się z różnych alternatywnych metod.
Całkowitą produkcję kwasu octowego szacuje się na 5 Mt / rok (mln ton rocznie), z czego około połowa pochodzi ze Stanów Zjednoczonych. Produkcja europejska wynosi około 1 Mt / rok i spada. Ostatecznie 0,7 Mt / r jest wytwarzane w Japonii. 1,5 Mt / rok poddaje się recyklingowi, co daje 6,5 Mt / rok na rynku światowym . Dwóch największych producentów to Celanese i BP Chimie. Głównymi producentami są również Millenium Chimie, Sterling Chimie, Samsung, Eastman i Svens Etanolkemi.
Karbonylowanie metanolu
Większość unrecycled kwas octowy wytwarza się przez karbonylowanie w metanolu . W tym procesie metanol i tlenek węgla reagują z wytworzeniem kwasu octowego zgodnie z równaniem: CH 3 OH + CO → CH 3 COOH
Proces ten wykorzystuje kwas jodowodorowy jako półprodukt i przebiega w trzech etapach. Do karbonylowania potrzebny jest katalizator , zwykle kompleks metalu (etap 2).
- CH 3 OH + HI → CH 3 I + H 2 O
- CH 3 I + CO → CH 3 COI
- CH 3 COI + H 2 O → CH 3 COOH + HI
Modyfikując proces, bezwodnik octowy może być wytwarzany w tej samej roślinie. Ponieważ metanol i tlenek węgla są powszechnymi surowcami, karbonylowanie metanolu od dawna stanowi atrakcyjną metodę produkcji kwasu octowego. Henry Dreyfus z British Celanese opracował pilotażową instalację do karbonylowania metanolu już w 1925 r. Jednak brak odpowiedniego wyposażenia do przechowywania korozyjnej mieszaniny reakcyjnej pod niezbędnym ciśnieniem ( 200 atm lub więcej) przez pewien czas utrudniał komercjalizację tej metody. . Pierwszy skomercjalizowane proces karbonylowania metanolu, który wykorzystuje kobaltu jako katalizatora, został opracowany przez niemiecką Chemical Company BASF w roku 1963. W roku 1968, nowy katalizator na bazie rodu ( cis - [Rh (CO) . Odkryto 2 I 2 ] - ) zdolne do skutecznego działania przy niskim ciśnieniu i przy bardzo niewielkiej ilości produktów ubocznych. Pierwsza instalacja wykorzystująca ten katalizator została zbudowana przez amerykańską firmę Monsanto w 1970 roku, a karbonylowanie metanolu katalizowanego rodem stało się dominującą metodą wytwarzania kwasu octowego (znanego jako proces Monsanto ). Pod koniec lat 90-tych BP wprowadziło na rynek katalizator Cativa ([Ir (CO) 2 I 2 ] - ), preferowany przez ruten. Ten proces jest bardziej przyjazny dla środowiska i wydajniejszy niż poprzedni iw dużej mierze wyparł proces Monsanto, często w tych samych fabrykach.
Utlenianie aldehydu octowego
Przed proces Monsanto był komercyjnie, większość kwasu octowego wytwarza się przez utlenianie z aldehydu octowego . Metoda ta pozostaje drugą najważniejszą drogą syntezy kwasu octowego, chociaż nie jest konkurencyjna w stosunku do karbonylowania metanolu. Aldehyd octowy można wytwarzać przez utlenianie butanu lub lekkiej benzyny ciężkiej, utlenianie etylenu lub alternatywnie przez hydratację acetylenu .
Gdy lekki butan lub nafta jest podgrzewana na powietrzu w obecności różnych jonów metali, zwłaszcza manganu , kobaltu i chromu , tworzy się nadtlenek, który następnie rozpada się na kwas octowy: 2 C 4 H 10 + 5 O 2 → 4 CH 3 COOH + 2 H 2 O Pracujemy z kombinacją temperatury i ciśnienia, aby mieszanina reakcyjna była jak najgorętsza, jednocześnie utrzymując butan w stanie ciekłym. 150 ° C i 55 atm to normalne warunki. Może również powstać kilka produktów ubocznych, w tym butanon , octan etylu , kwas mrówkowy i kwas propionowy . Te produkty uboczne mają również wartość rynkową, a warunki reakcji można zmienić, aby produkować ich więcej, jeśli ma to korzyść ekonomiczną. Jednak oddzielenie kwasu octowego od jego produktów ubocznych zwiększa koszty procesu. W warunkach i katalizatorach podobnych do tych stosowanych do utleniania butanu, aldehyd octowy może być utleniany tlenem z powietrza w celu wytworzenia kwasu octowego: 2 CH 3 CHO + O 2 → 2 CH 3 COOH
Dzięki nowoczesnym katalizatorom reakcja ta może osiągnąć wydajność ponad 95%. Głównymi produktami ubocznymi są octan etylu , kwas mrówkowy i formaldehyd . Wszystkie te związki mają niższą temperaturę wrzenia niż kwas octowy i można je łatwo oddzielić przez destylację .
Utlenianie etylenu
Acetaldehyd można wytworzyć z etylenem przez w procesie Wacker , a następnie utlenia się w sposób opisany powyżej. Niedawno jednoetapowa przemiana etylenu w kwas octowy została skomercjalizowana przez firmę Shōwa Denkō , która otworzyła zakład utleniania etylenu w Oita w Japonii w 1997 roku. Proces jest katalizowany metalowym katalizatorem opartym na palladzie przy pomocy heteropolikwas, taki jak kwas wolstokrzemowy. Proces ten mógłby konkurować z karbonylowaniem metanolu w przypadku małych zakładów (100–250 kt / rok ) w zależności od ceny etylenu.
Synteza malonowa
- Synteza malonowa z użyciem halogenometanu jako podstawnika (RX).
Handel
W 2014 roku Francja była importerem netto kwasu octowego, zgodnie z francuskimi zwyczajami. Średnia cena importowa za tonę wynosiła 430 EUR.
Różnorodny
Kwas octowy, stosowany miejscowo w laryngologii, jest częścią listy leków niezbędnych Światowej Organizacji Zdrowia (lista zaktualizowana w kwietniu 2013 r.).
Uwagi i odniesienia
- kwasem octowym, bezpieczeństwo arkusz (-y) Międzynarodowego Programu Bezpieczeństwa Chemicznego , konsultowany w dniu 9 maja 2009
- „KWAS” w Hazardous Substances Data Bank , obejrzano 16 lipca 2012
- (w) David R. Lide, Podręcznik chemii i fizyki , CRC,16 czerwca 2008, 89 th ed. , 2736 str. ( ISBN 142006679X i 978-1420066791 ) , str. 9-50
- (w) Yitzhak Marcus, The Properties of Solvents , vol. 4, Anglia, John Wiley & Sons Ltd,1999, 239 pkt. ( ISBN 0-471-98369-1 )
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- (i) W. M Haynes CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press / Taylor i Francis,2011, 91 th ed. , 2610 s. ( ISBN 978-143982-077-3 ) , str. 3-4
- (w) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 II wyd. , 1076, s. ( ISBN 0387690026 , czytaj online ) , str. 294
- (en) Şerban Moldoveanu, Przygotowanie próbki w chromatografii , Elsevier,2002, 930 pkt. ( ISBN 0444503943 ) , str. 258
- (en) Robert H. Perry i Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , str. 2-50
- Wagner, Frank S. (1978) „Kwas octowy”. W: Grayson, Martin (wyd.), Kirk-Othmer Encyclopedia of Chemical Technology , 3 -tego wydania, Nowy Jork: Wiley.
- (en) "Acetic acid" , w NIST / WebBook , dostęp 28 sierpnia 2009
- (w) Carl L. Yaws, Podręcznik diagramów termodynamicznych , t. 1, Huston, Teksas, Gulf Pub. Współ.,1996( ISBN 0-88415-857-8 )
- (w) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18 czerwca 2002, 83 th ed. , 2664 s. ( ISBN 0849304830 , prezentacja online ) , str. 5-89
- (w) David R. Lide, Podręcznik chemii i fizyki , CRC,2008, 89 th ed. , 2736 str. ( ISBN 978-1-4200-6679-1 ) , str. 10-205
- „ Acetic acid ” , na www.reciprocalnet.org (dostęp 12 grudnia 2009 )
- Numer indeksu w tabeli 3.1 załącznika VI do rozporządzenia WE nr 1272/2008 (16 grudnia 2008)
- SIGMA-ALDRICH
- „ kwas octowy ” w bazie produktów chemicznych Reptox z CSST (Quebec organizacji odpowiedzialnej za bezpieczeństwo i higienę pracy), dostęp 24 kwietnia 2009
- (w) „ Acetic acid ” on ChemIDplus , dostęp 28 sierpnia 2009
- „ Acetic acid ”, pod adresem hazmap.nlm.nih.gov (dostęp: 14 listopada 2009 )
- „Acetic acid” , w ESIS , dostęp 3 marca 2010
- „ Acid acetic - Société Chimique de France ” , na www.societechimiquedefrance.fr (dostęp 10 października 2020 )
- INRS, Karta toksykologiczna , ulotka 8 pp Ref FT 24, wersja 2019
- Temperatura topnienia wynosi około 16,6 ° C . Jego temperatura wrzenia jest nieco mniejsza niż 117,9 ° C . Produkt jest palny o temperaturze zapłonu powyżej 40 ° C , podczas gdy temperatura samozapłonu wzrasta do 465 ° C .
- Khelifi, L., Ghorbel, A., Garbowski, E. i Primet, M. (1997). Przygotowanie zol-żel katalizatorów Pt / Al2O3 do spalania katalitycznego. Journal of Physical Chemistry , 94, 2016-2026.
- Rezgui, S., Ghorbel, A. i Gates, BC (1995). Kontrola przygotowania mieszanych katalizatorów tlenkowych chromu i glinu metodą zol-żel . Journal of Physical Chemistry, 92, 1576-1588 | podsumowanie .
- Barbara Brutsaert, " Kwasy organiczne i średniołańcuchowe kwasy tłuszczowe ", 9. dzień Produkcja trzody chlewnej i drobiu ,2009( czytaj online )
- Pierre de Menten , Słownik chemii: podejście etymologiczne i historyczne , De Boeck,2013, 395 str. ( ISBN 978-2-8041-8175-8 , czytaj online ) , s.20
- Goldwhite, Harold (2003). Sekta New Haven. Byk. Am. Chem. Soc. (Wrzesień 2003) .
- Martin, Geoffrey (1917). Chemia przemysłowa i produkcyjna , część 1, organiczna. Londyn, Crosby Lockwood, str. 330–31 .
- Schweppe, Helmut (1979). „Identyfikacja barwników na starych tekstyliach” . J. Am. Inst. Konserwacja 19 (1/3), 14–23.
- Jones, RE; Templeton, DH (1958). „Struktura krystaliczna kwasu octowego”. Acta Crystallogr. 11 (7), 484–87.
- J. Chen, CL Brooks i H. Sherega, „Revisiting the Carboxylic Acid Dimers in Awater Solution”, J. Phys. Chem. B , tom. 112, strony 242-249, 2008.
- Lafon-Lafourcade, S., Lucmaret, V. i Joyeux, A. (1980). Kilka obserwacji dotyczących tworzenia kwasu octowego przez bakterie mlekowe. OENO One, 14 (3), 183-194 | podsumowanie .
- Dictionary of Organic Compounds ( 6th Edn.) , T. 1 (1996). Londyn: Chapman & Hall. ( ISBN 978-0-412-54090-5 )
- Yoneda, Noriyki; Kusano, Satoru; Yasui, Makoto; Pujado, Peter; Wilcher, Steve (2001). Appl. Catal. O: Gen. 221 , 253–265.
- „Raport z produkcji”. Chem. Inż. News (11 lipca 2005), str. 67–76.
- Suresh, Bala (2003). „Kwas octowy” . Raport CEH 602.5000, SRI International.
- Lancaster, Mike (2002) Green Chemistry, tekst wprowadzający , Cambridge, Royal Society of Chemistry, str. 262–266 . ( ISBN 978-0-85404-620-1 ) .
- Sano, Ken-ichi; Uchida, Hiroshi; Wakabayashi, Syoichirou (1999). Catalyst Surveys from Japan 3 , 55–60.
- „ Wskaźnik importu / eksportu ” , na Generalnej Dyrekcji Celnej. Wskazać NC8 = 29152100 (dostęp 7 sierpnia 2015 r. )
- Wzorcowa lista podstawowych leków WHO, 18. lista , kwiecień 2013 r
Bibliografia
- Avom, J., Mbadcam, JK, Matip, MRL, & Germain, P. (2001). Izotermiczna adsorpcja kwasu octowego na węglu pochodzenia roślinnego . African Journal of Science and Technology, 2 (2).
- Brodzki, D., Denise, B., & Pannetier, G. (1977). Właściwości katalityczne kompleksów metali szlachetnych: karbonylowanie metanolu do kwasu octowego w obecności związków irydu (I). Journal of Molecular Catalysis, 2 (3), 149–161.
- Pastor L (1862). Nowy proces przemysłowy produkcji octu . Mallet-Bachelier.