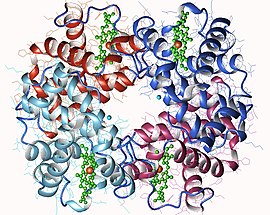
Hemoglobina
Hemoglobiny , powszechnie symbolizowane Hb czasami Hgb jest pigment oddechowego (rodzina cząsteczkowa metaloprotein tu zawierającego żelazo ) występuje głównie w krwi od kręgowca , w swych krwinkach czerwonych i w tkankach niektórych bezkręgowców . Jego funkcją jest transport tlenu O 2z układu oddechowego ( płuca , skrzela ) do reszty ciała . Ilość hemoglobiny to parametr mierzony podczas morfologii krwi .
Rola
Hemoglobina uwalnia do tkanek tlen niezbędny do tlenowego oddychania komórkowego , który poprzez metabolizm dostarcza energii niezbędnym do życia procesom biologicznym.
U człowieka hemoglobina jest białkiem hetero - tetramerycznym utworzonym z łańcuchów peptydowych, które są identyczne dwa na dwa. Hemoglobina A (HbA) stanowi około 95% cząsteczek hemoglobiny u dorosłych i składa się z dwóch łańcuchów α i dwóch łańcuchów β; istnieje również Stężenie hemoglobiny 2 (HbA 2 ) o wzorze α 2 δ 2i hemoglobinę F (HbF, płodowa) o wzorze α 2 γ 2. Każdy z czterech kanałów jest związany z grupę prostetyczną o nazwie hemu , składający się z kationem w żelaza skompleksowanego z porfiryny . Dlatego hemoglobina jest hemoproteiną .
U ssaków hemoglobina stanowi blisko 96% suchej masy krwinek czerwonych, a około 35% ich całkowitej zawartości, w tym woda. Każda cząsteczka hemoglobiny może wiązać do czterech cząsteczek tlenu O 2a hemoglobina we krwi może zawierać 1,34 ml O 2na gram białka, co pozwala mu przenosić 70 razy więcej tlenu niż ilość O 2rozpuszczony we krwi. Hemoglobina bierze również udział w transporcie gazów innych niż tlen. W szczególności zapewnia transport części dwutlenku węgla CO 2wyprodukowany przez oddychanie komórkowe, a także przenosi tlenku azotu NO, które odgrywają istotną rolę w komórkowych sygnałów pewnych fizjologicznych procesach , a który jest uwalniany razem z tlenem, po czym transportuje się na tiolowej grupy z apoproteiny .
większość hemoglobiny znajduje się w krwinkach czerwonych, które są wytwarzane przez szpik kostny. Jednak nie cała hemoglobina jest skoncentrowana w krwinkach czerwonych. Znajduje się więc na przykład w neuronach dopaminergicznych z grupy A9 istoty czarnej , w makrofagach , komórkach pęcherzyków płucnych oraz w nerkach , w komórkach mezangium . W tych tkankach hemoglobina pełni rolę przeciwutleniacza i regulatora metabolizmu żelaza .
Hemoglobina i różne pokrewne cząsteczki są również obecne w dużej liczbie bezkręgowców, grzybów i roślin . W tych organizmach hemoglobina służy do transportu tlenu O 2, ale może również działać jako transporter i regulator innych substancji chemicznych, takich jak dwutlenek węgla CO 2, tlenek azotu NO, siarkowodór HS i anion siarczkowy S 2– . Odmiana hemoglobiny, zwana leghemoglobiną , usuwa tlen z układów beztlenowych , na przykład z guzków Rhizobium w fabaceae , zanim je dezaktywuje.
Struktura i działanie
Podjednostki
Hemoglobina ma czwartorzędową strukturę charakterystyczną dla wielu białek z podjednostkami kulistymi . Większość jej pozostałości z aminokwasów zaangażowanych w alfa helis połączonych segmentów nie będących segmentami śrubowymi. Spiralne odcinki są stabilizowane przez wiązania wodorowe, które nadają białku charakterystyczną trójwymiarową strukturę, zwaną globinowym fałdowaniem, podobnie jak w innych globinach z hemową grupą prostetyczną , taką jak mioglobina . To charakterystyczne pofałdowanie posiada wnękę, w której szczelnie umieszczona jest cząsteczka hemu stanowiąca grupę prostetyczną białka. Dlatego hemoglobina zawiera jedną cząsteczkę hemu na podjednostkę.
-
Ogólna reprezentacja cząsteczki hemoglobiny, pokazująca cztery podjednostki, identyczne parami, każda z cząsteczką hemu umieszczoną we wnękach w podjednostkach.
U większości kręgowców cząsteczka hemoglobiny jest zbiorem czterech podjednostek kulistych w przybliżeniu czworościennym . Te podjednostki są utrzymywane razem przez wiązania wodorowe, jonowe i efekt hydrofobowy . U dorosłych ludzi najpowszechniejszym rodzajem hemoglobiny jest hemoglobina A, składająca się z dwóch podjednostek α i dwóch podjednostek β, z których każda składa się odpowiednio z 141 i 146 reszt aminokwasowych. Struktura ta jest symbolizowana przez α 2 β 2. Te podjednostki są strukturalnie bardzo podobne i mają w przybliżeniu ten sam rozmiar. Każdy ma masę cząsteczkową około 16 kDa lub 64 kDa ( 64 458 g · mol- 1 ) dla białka o pełnej długości. U dzieci główna hemoglobina nazywana jest hemoglobiną F (płodowa) o wzorze α 2 γ 2przy czym podczas wzrostu łańcuchy γ są stopniowo zastępowane przez łańcuchy β.
Heme
Hem jest złożona z kationów z żelaza ( II ) koordynowanej do czterech atomów od azotu z porfiryny , A tetrapirolowych cząsteczka jest płaska. Ten kation Fe 2+ jest również kowalencyjnie związany z resztą histydynową F8 globiny, do której hemu jest wstawiony; ta reszta, zwana proksymalną histydyną , znajduje się poniżej płaszczyzny hemu. Fe 2+ może również wiązać się odwracalnie poprzez koordynujące wiązanie kowalencyjne z cząsteczką tlenu O 2powyżej płaszczyzny hemu, naprzeciwko histydyny bliższym wypełniającej sześcio- ligand ośmiościenny geometrii koordynacyjny żelaza ( II ), kationu w hemoglobiny; w przypadku braku tlenu w deoksyhemoglobinie to szóste miejsce zajmuje bardzo słabo związana cząsteczka wody .
Żelazo żelaza w deoksyhemoglobina jest w wirowania, stan , który oznacza, że wszystkie jego pięć dni orbitale są zajęte, głównie przez pojedyncze elektrony, w związku z jonowego promieniem rzędu 92 pm , podczas gdy w oksyhemoglobiny, stopów żelaza jest w postaci stan niskiego spinu , tj. jego orbitale d są zajęte przez sześć sparowanych elektronów, które są ograniczone do trzech orbitali o najniższej energii, stąd promień jonowy tylko 75 µm . Z tego powodu jon Fe 2+ jest przesunięty o około 40 µm od płaszczyzny hemu w deoksyhemoglobinie, ale tylko o 10 µm w oksyhemoglobinie. Ta zmienność leży u podstaw przełączania między napiętą formą a zrelaksowaną formą hemoglobiny.
- Struktura hemu b , grupa protetyczna hemoglobiny.
-
(en) Schematyczny diagram wiązania cząsteczki tlenu O 2na hemie , symbolizowany tutaj grubą linią. Jon ponadtlenkowy O 2• - w wyniku jest połączony po jednej stronie do kationu z żelaza ( III ) za pomocą współrzędnych wiązaniem kowalencyjnym , a z drugiej strony do histydyny dalszym. Fe ( II ), kationu z deoksyhemoglobina jest w wirowania, stanu i przesunięty względem płaszczyzny hemowej wobec histydyny bliższej, ale doprowadza się w tej płaszczyźnie przez przemieszczenie się do niskiego wirowania stanie przez wiązania L. Tlenem, który zmienia histydyna w pobliżu hemu i sprzyja przesunięciu reszty białka z formy naprężonej (T) do postaci zrelaksowanej (R).
Kation żelaza może znajdować się na stopniu utlenienia +2 lub +3: w tym drugim przypadku mamy do czynienia z methemoglobiną , która wiąże się z tlenem mniej odwracalnie niż hemoglobina, a także z mniejszym powinowactwem. Rzeczywiście, kiedy wiąże się z hemem żelazawym, cząsteczką tlenu O 2ma tendencję do redukcji do jonu ponadtlenkowego O 2• - podczas gdy kation Fe 2+ ma tendencję do utleniania się do Fe 3+ , co jest mechanizmem odwracalnym podczas uwalniania tlenu; przeciwnie, wiązanie tlenu z hemem żelazowym jest zasadniczo nieodwracalne i ma tendencję do blokowania białka w postaci R, co zapobiega uwalnianiu tlenu i hamuje jego działanie jako transportera tlenu. Cytochromu b 5 reduktazy lub methemoglobiny reduktazy jest enzym , który zapewnia redukcję methemoglobiny hemoglobinę przez redukcję kationów Fe 3+ do Fe 2+ , dzięki czemu enzym zasadniczy w utrzymaniu właściwości krwi.
Forma napięta (T) i forma zrelaksowana (R)
Odtleniona hemoglobina (deoksyhemoglobina) ma tak zwaną konformację T, czyli napiętą , podczas gdy hemoglobina utleniona (oksyhemoglobina) ma tak zwaną konformację R, czyli zrelaksowaną . Forma T ma niskie powinowactwo do tlenu i dlatego ma tendencję do jego uwalniania, podczas gdy forma R ma wysokie powinowactwo do tlenu i ma tendencję do jego wiązania. Kilka czynników sprzyja jednej z tych konformacji. Tak więc formie T sprzyja niskie pH ( kwaśne ), wysokie stężenie CO 2oraz wysoki poziom 2,3-bisfosfoglicerynianu (2,3-BPG), który wspomaga uwalnianie tlenu podczas krążenia krwi w tkankach , podczas gdy postaci R sprzyja wysokie pH, niskie ciśnienie parcjalne CO 2oraz niski poziom 2,3-BPG, który wspomaga pobieranie tlenu, gdy krew krąży na poziomie pęcherzyków płucnych .
-
Schematyczne przedstawienie przełączania hemoglobiny między formami T (deoksy) i R (oksy). Ruchy hemu i proksymalnej histydyny są wyraźnie widoczne w podjednostkach α 1 i β 2 .
-
Szybkość nasycenia O 2hemoglobina jako funkcja ciśnienia parcjalnego O 2 ; czasami nazywana krzywą Barcrofta , jest sigmoidalna ze względu na kooperacyjny efekt towarzyszący wiązaniu tlenu do hemoglobiny.
Przełączanie między formą T a formą R hemoglobiny jest tak zwanym mechanizmem kooperacyjnym , to znaczy allosterycznym , ponieważ wiązanie cząsteczki tlenu z formą T wywołuje zmianę konformacyjną, która rozprzestrzenia się częściowo do sąsiednich podjednostek , których powinowactwo dla tlenu stopniowo wzrasta, gdy inne cząsteczki tlenu wiążą się z hemoglobiną, aż całe białko przyjmie konformację R; odwrotnie, uwolnienie cząsteczki tlenu z formy R wywołuje zmianę konformacyjną, która częściowo rozprzestrzenia się do sąsiednich podjednostek, których powinowactwo do tlenu stopniowo maleje, gdy hemoglobina uwalnia tlen, aż całe białko przyjmie konformację T. To jest powód, dla którego Krzywa wiązania tlenu z hemoglobiną w funkcji ciśnienia parcjalnego tlenu ma postać sigmoidalną , natomiast przy braku allosterii byłaby hiperboliczna .
Krzywa nasycenia tlenem hemoglobiny
Zwyczajowo wykreśla się stopień nasycenia hemoglobiny w tlenie O 2przedstawiony na osi y w funkcji ciśnienia cząstkowego z tlenu O 2, podana na odciętej . Na tej ilustracji krzywa jest esowata i ma tendencję do przesuwania się w lewo, gdy powinowactwo hemoglobiny do tlenu wzrasta, i w prawo, gdy maleje. Ciśnienie parcjalne tlenu, przy którym hemoglobina jest w 50% nasycona tlenem, nazywa się p 50 : im niższa jego wartość, tym wyższe powinowactwo hemoglobiny do tlenu. Orientacyjnie, p50 hemoglobiny u zdrowej osoby dorosłej wynosi zwykle 3,5 kPa , często zapisywane jako 26,6 mmHg , podczas gdy dla mioglobiny wynosi zwykle 130 Pa .
Kilka czynników zwiększa p 50 i dlatego przesuń tę krzywą w prawo:
- spadek pH , który staje się kwaśny : to jest efekt Bohra ;
- wzrost poziomu dwutlenku węgla CO 2 : to jest efekt Haldane ;
- wzrost poziomu 2,3-bisfosfoglicerynianu (2,3-BPG);
- wzrost temperatury, jednak ze stosunkowo niewielkim skutkiem.
Efekty te są odwracalne, a odwrócenie kierunku zmian tych czynników powoduje przesuwanie się krzywej w lewo.
Inne ligandy przenoszone przez hemoglobinę
Oprócz tlenu O 2, który wiąże się z hemoglobiną zgodnie z tzw. mechanizmem kooperacyjnym , białko to przenosi również inne ligandy , z których część jest inhibitorami kompetycyjnymi , np. tlenek węgla CO, a inne są ligandami allosterycznymi, np. dwutlenkiem węgla CO 2i tlenek azotu NO. CO 2odwracalnie wiąże się z grupami aminowymi w apoproteinie, tworząc karbaminohemoglobinę , która zapewnia około 10% transportu CO 2u ssaków reszta jest transportowana głównie w postaci jonów wodorowęglanowych HCO 3- . Tlenek azotu wiąże się odwracalnie z grupami tiolowymi apoproteiny, tworząc S- nitrozotiol . Transport tlenku azotu może pośrednio pośredniczyć w transporcie tlenu przez hemoglobinę, działając jako środek rozszerzający naczynia krwionośne w tkankach, w których ciśnienie parcjalne tlenu jest niskie.
Inhibitory przez współzawodnictwo z tlenemWiązanie tlenu z hemoglobiną jest skutecznie blokowane przez tlenek węgla CO, na przykład z dymu papierosowego , spalin lub niepełnego spalania przez kocioł . Tlenek węgla konkuruje z tlenem w miejscu wiązania tego ostatniego na hemie. Powinowactwo hemoglobiny do tlenku węgla wynosi 230 razy większe niż stężenia hemoglobiny do tlenu, tak, że małe ilości tlenku węgla wystarczająca by znacząco zmniejszać utlenianie hemoglobiny w hematosis , a zatem zdolność krwi do natleniania ciała. Niedotlenienie , które skutkuje z ciągłym kontakcie z 0,16% CO w powietrzu powoduje, zawroty głowy , mdłości , ból głowy i częstoskurcz w ciągu 20 minut i prowadzi do śmierci w ciągu dwóch godzin; 1,28% CO w powietrzu powoduje utratę przytomności już po dwóch do trzech oddechów i śmierć w mniej niż trzy minuty. W połączeniu z tlenkiem węgla hemoglobina jest białkiem zwanym karboksyhemoglobiną, którego bardzo jaskrawoczerwony kolor prawdopodobnie zabarwi różową skórę ofiar zatrucia tlenkiem węgla , które w przeciwnym razie miałyby bladą lub siną cerę.
Podobnie hemoglobina wykazuje, w miejscu wiązania tlenu, konkurencyjne powinowactwo do jonu cyjankowego CN - , tlenku siarki SO i jonu siarczkowego S 2– , tak jak w przypadku siarkowodoru H 2 S. Wiążą się one z kationem żelaza hemu bez zmiany jego stopnia utlenienia, ale mimo to hamują wiązanie tlenu z hemem, stąd ich wysoka toksyczność.
Allosteryczne ligandy hemoglobinyDwutlenek węgla CO 2łatwiej wiąże się z deoksyhemoglobiną, co ułatwia jej eliminację z organizmu. Nazywa się to efektem Haldane'a .
Ponadto CO 2rozpuszczony we krwi przekształca się w anion wodorowęglanowy HCO 3- przez anhydrazę węglanową , w zależności od reakcji:
CO 2+ H 2 O→ H 2 CO 3→ HCO 3- + H + .Wynika z tego, że krew bogata w CO 2jest również bardziej kwaśny , tzn. jego pH jest obniżane pod wpływem kwasu węglowego . Wiązanie protonów H + i cząsteczek CO 2hemoglobina wywołuje zmianę konformacyjną, która faworyzuje formę T, a tym samym uwalnianie tlenu. Protony wiążą się z różnymi miejscami w hemoglobinie, podczas gdy dwutlenek węgla wiąże się z grupami α- aminowymi , tworząc karbaminohemoglobinę . Zmniejszenie powinowactwa hemoglobiny do tlenu w obecności CO 2a kwaśne pH nazywa się efektem Bohra .
Osoby aklimatyzowane na dużych wysokościach mają podwyższony poziom 2,3-bisfosfoglicerynianu (2,3-BPG) we krwi . Ten ostatni jest efektorem heteroalosterycznym, który ma wpływ na zmniejszenie powinowactwa hemoglobiny do tlenu poprzez stabilizację formy T: pod ciśnieniem parcjalnym tlenu niższym niż na poziomie morza spadek powinowactwa hemoglobiny do tlenu skutkuje zwiększeniem ogólnego efektywność transportu tlenu przez hemoglobinę. Mówiąc bardziej ogólnie, wzrost poziomu 2,3-BPG obserwuje się, gdy ciśnienie parcjalne tlenu w tkankach obwodowych spada, na przykład w przypadku hipoksemii , przewlekłej choroby układu oddechowego , anemii , a nawet niewydolności serca . Odwrotnie , poziom 2,3-BPG obniża się w przypadku wstrząsu septycznego i hipofosfatemii (w) .
Biosynteza i degradacja
Biosynteza hemoglobiny obejmuje złożony zestaw etapów. Hemu jest z serii reakcji, które biorą swój początek w mitochondriach i nadal w cytozolu z erytrocytów niedojrzałe, podczas gdy apoproteina jest wytwarzany na rybosomach cytozolu. Produkcja hemoglobiny zachodzi we wczesnych stadiach erytropoezy , od fazy proerytroblastów do fazy retikulocytów w szpiku kostnym . To tutaj erytrocyty ssaków tracą swoje jądro , podczas gdy jądro pozostaje w erytrocytach u ptaków i wielu innych gatunków . Jednak biosynteza apoproteiny trwa po utracie jądra, ponieważ w komórce pozostaje informacyjny RNA , który może być poddawany translacji przez rybosomy cytozolu aż do aktywacji erytrocytów w aparacie sercowo-naczyniowym .
U kręgowców erytrocyty, które osiągnęły koniec swojego życia z powodu starzenia się lub pogorszenia, są usuwane z krwi przez fagocytozę przez makrofagi w śledzionie i wątrobie . W przypadku hemolizy we krwi hemoglobina wiąże się z haptoglobiną , natomiast wolny hem jest wiązany przez hemopeksynę , co ogranicza efekt oksydacyjny. Niecałkowicie degradacji lub hemoglobiny uwalniane w dużych ilościach z uszkodzonych komórek czerwonych krwinek może zatkać naczynia krwionośne , takie jak kapilar tych nerek , który może powodować chorobę nerek . Uwolniona hemoglobina jest usuwana z krwi przez białko CD163 , które jest wyrażane wyłącznie w monocytach i makrofagach. Hemoglobina jest rozkładana w tych komórkach, a żelazo hem jest zawracane, podczas gdy jedna cząsteczka tlenku węgla jest uwalniana na każdą zdegradowaną cząsteczkę hemu: rozkład hemu jest jednym z niewielu naturalnych procesów. Wytwarzanie tlenku węgla w organizmie człowieka i jest odpowiedzialne za obecność CO we krwi ludzi oddychających nawet najczystszym powietrzem. W tym procesie powstaje biliwerdyna , a następnie bilirubina , która ma kolor żółty. Nierozpuszczalny, jest uwalniany przez makrofagi do osocza krwi , gdzie wiąże się z albuminą surowicy , która transportuje ją do hepatocytów . Te ostatnie solubilizują go poprzez sprzęganie z kwasem glukuronowym i wydzielają w jelitach z żółcią . W jelitach bilirubina jest metabolizowana do urobilinogenu , który jest wydalany z kałem w postaci sterkobiliny oraz z moczem . Kiedy bilirubina nie może zostać wydalona, jej stężenie we krwi wzrasta i jest wydalana głównie z moczem, który ciemnieje, a kał zmienia kolor.
Żelazo wytwarzane w wyniku degradacji hemu jest przechowywany w ferritins tych tkankach i transportowane w osoczu krwi przez beta-globuliny , takie jak transferyn .
Genetyczny
Cząsteczki hemoglobiny składają się z podjednostek typu globiny, których sekwencja różni się w zależności od gatunku . Istnieją również warianty hemoglobiny w ramach tego samego gatunku, chociaż jeden z tych wariantów przeważnie przeważa nad pozostałymi. U ludzi dominująca postać hemoglobiny nazywana jest hemoglobiną A; jest kodowany przez HBA1 , HBA2 i Hbb geny znajdują się na chromosomie 16 dwóch pierwszych i chromosomu 11 na ostatnim.
Ewolucja
Ogólnie przyjmuje się, że różnica między hemoglobiną a mioglobiną jest następstwem oddzielenia gnathostomów ( kręgowców do szczęki ) lub minoga . Mioglobina była ukierunkowana na magazynowanie tlenu, podczas gdy hemoglobina była wyspecjalizowana w transporcie tlenu. Podjednostki białka są kodowane przez geny typu globiny α i β. Poprzednicy tych genów powstali podczas duplikacji, która miała miejsce po pojawieniu się gnathostomów, około 450 do 500 milionów lat temu. Pojawienie się genów α i β otworzyło drogę do polimeryzacji tych globin, a tym samym do powstania większego białka składającego się z odrębnych podjednostek . Fakt, że hemoglobina jest białkiem polimerowym, jest podstawą mechanizmu allosterycznego , który w szczególności leży u podstaw kooperatywnego charakteru wiązania tlenu z hemoglobiną. Gen α przeszedł następnie drugą duplikację, która prowadzi do powstania genów HBA1 i HBA2 . Te wielokrotne duplikacje i rozbieżności stworzyły cały zestaw genów związanych z globinami α i β, których regulacja prowadzi do ich ekspresji na różnych etapach rozwoju.
-
Dopasowanie sekwencji łańcuchów α, β i δ ludzkiej hemoglobiny (źródło UniProt ).
Mutacje
Te mutacje genów hemoglobiny może prowadzić do odmian hemoglobiny. Większość z tych wariantów jest funkcjonalna i nie ma wpływu na zdrowie. Z drugiej strony, niektóre mutacje hemoglobiny mogą powodować choroby genetyczne zwane hemoglobinopatiami . Najbardziej znanym z tych schorzeń jest anemia sierpowata , która była pierwszą chorobą człowieka, której mechanizm został wyjaśniony na poziomie molekularnym. W talasemie Kolejną grupę hemoglobinopatie obejmujących takie zmiany w regulacji genów globiny składnik hemoglobiny. Wszystkie te choroby powodują anemię .
Zmiana sekwencji aminokwasów hemoglobiny może mieć charakter adaptacyjny. Jest zatem możliwe było pokazać, który dostosowuje hemoglobiny spadkiem ciśnienia cząstkowego z tlenem obserwowane na dużych wysokościach. Hemoglobina musi wtedy być zdolna do wiązania się z tlenem pod niższym ciśnieniem, co może objawiać się zmianą sekwencji aminokwasów zaangażowanych w powinowactwo hemoglobiny do tlenu, co zaobserwowano na przykład u kolibrów z Andów. cordillera : tak więc u gatunków z rodzaju Oreotrochilus , u kolibra Castelneau , inka violifera, a nawet kolibra olbrzymiego , mutacje te zmniejszają powinowactwo hemoglobiny do kwasu fitynowego , który u tych ptaków odgrywa taką samą rolę jak 2,3- bisfosoglicerynian u ludzi; ten spadek powinowactwa ma wpływ na zwiększenie wydajności transportu tlenu, gdy ciśnienie cząstkowe tego ostatniego jest zmniejszone.
Adaptacja hemoglobiny do dużych wysokości dotyka również ludzi. W ten sposób zidentyfikowaliśmy grupę kobiet tybetańskich, których genotyp koduje hemoglobinę, której powinowactwo do tlenu wzrasta przy niskim ciśnieniu parcjalnym. Ma to wpływ na zmniejszenie śmiertelności niemowląt w tych ekstremalnych warunkach, co daje selektywną korzyść, sprzyjającą osobom będącym nosicielami tych mutacji hemoglobiny.
Ludzkie warianty hemoglobiny
U dorosłych głównym wariantem hemoglobiny jest hemoglobina A lub HbA o wzorze α 2 β 2, co stanowi ponad 97% całkowitej hemoglobiny u zdrowej osoby dorosłej. Innym wariantem hemoglobiny dorosłej jest hemoglobina A 2 lub HbA 2 o wzorze α 2 δ 2, co stanowi od 1,5% do 3,1% całkowitej hemoglobiny zdrowej osoby dorosłej, ale jej odsetek wzrasta u pacjentów z sierpem sierpowatokrwinkowym . Oprócz tych zdrowych odmian dorosłych istnieje tuzin innych wariantów ludzkiej hemoglobiny, które można znaleźć w embrionie , płodzie lub pacjentach z jedną lub kilkoma postaciami hemoglobinopatii .
Hemoglobiny embrionalne
U ludzi znane są cztery typy hemoglobiny zarodkowej :
- Hb Gower-1 o wzorze ζ 2 ε 2, jest stosunkowo niestabilny i łatwo się rozkłada;
- Hb Gower-2 o wzorze α 2 ε 2bardziej stabilny niż wariant Gower-1, występuje w niewielkich ilościach w życiu embrionalnym i płodowym; zaproponowano ją jako leczenie przez reaktywację genu u pacjentów cierpiących na hemoglobinopatie, takie jak β-talasemia, u których reaktywacja hemoglobiny F jest przeciwwskazana z powodu toksyczności;
- Hb Portland-1 o wzorze ζ 2 γ 2, występuje w niewielkich ilościach w życiu embrionalnym i płodowym;
- Hb Portland-2 o wzorze ζ 2 β 2, jest jeszcze bardziej niestabilny niż wariant Gower-1, ale został zaproponowany jako leczenie reaktywacji genów u pacjentów z α-talasemią .
Embrionalna hemoglobina jest czasami symbolizowana przez Hbε, którego nie należy mylić z hemoglobiną E, oznaczoną HbE, która jest patologiczną odmianą HbA wykazującą szkodliwą mutację w podjednostkach β, oznaczoną jako β E („E” w tym przypadku odnosi się do pozostałości z glutaminianem zmodyfikowany przez mutację ).
Hemoglobina płodowa
Płodowej hemoglobiny HbF o wzorze α 2 γ 2zastępuje hemoglobinę embrionalną po 10 do 12 tygodniach rozwoju. Stanowi do 95% krwi noworodka i jest stopniowo zastępowana przez dorosłą hemoglobinę HbA od szóstego miesiąca po urodzeniu; jednak pozostaje obecny w śladowych ilościach u dorosłych, gdzie nie przekracza 1% wszystkich wykrywalnych wariantów hemoglobiny. Pozostaje u dzieci urodzonych w niektórych przypadkach talasemii , czasami do piątego roku życia, a rzadki stan zwany dziedzicznym uporczywością hemoglobiny płodowej (en) ( HPFH ) powoduje produkcję HbF zamiast HbA poza normalny okres. Ponadto produkcję HbF można reaktywować u dorosłych w warunkach terapeutycznych w leczeniu niedokrwistości sierpowatokrwinkowej .
Hemoglobina płodowa charakteryzuje się większym powinowactwem do tlenu niż hemoglobina dorosła, co pozwala płodowi na utlenienie się z krwi matki: w rzeczywistości p 50 HbF wynosi około 19 mmHg ( 2,6 kPa ), w porównaniu do 26,8 mmHg ( 3,6 kPa ) dla HbA. Ta różnica w powinowactwie do tlenu wynika z różnicy w powinowactwie do jednego z allosterycznych efektorów hemoglobiny: 2,3-bisfosfoglicerynianu (2,3-BPG), którego wiązanie z hemoglobiną wpływa na stabilizację formy T tego białka, co odpowiada deoksyhemoglobinie, która zmniejsza powinowactwo hemoglobiny do tlenu. W przypadku hemoglobiny płodowej The γ podjednostka posiada pozostałości z seryny w pozycji 143, w której podjednostka β HbA ma resztę histydyny : pozycja ta znajduje się w miejscu wiązania 2,3-BPG i zastąpienie histydyna, której łańcuch boczny przenosi dodatni ładunek elektryczny , przez elektrycznie obojętną serynę, osłabia oddziaływanie 2,3-BPG z hemoglobiną, ponieważ 2,3-BPG jest małą cząsteczką przenoszącą pięć ujemnych ładunków elektrycznych.
Hemoglobinopatie
W talasemie cechują się niewystarczającą wytwarzania jednego z dwóch typów podjednostek hemoglobinę dorosłych. Rozróżnia się zatem talasemię α , która jest raczej rzadka, w której podjednostki α są wytwarzane w niewystarczającym stopniu, oraz talasemię β , najpowszechniejszą, w której to podjednostki β są wytwarzane w niewystarczającym stopniu. Pierwsza prowadzi do powstania tetramerów β-globiny zwanych hemoglobiną H , o wzorze β 4, które są dość niestabilne. Do a 0 homozygoty ogół nie przetrwać długi po urodzeniu spowodowana głęboką zmianę hemoglobiny płodowej HbF, daje w tych warunkach Barts hemoglobiny , o wzorze ogólnym γ 4.
Główne mutacje hemoglobiny to:
- hemoglobiny C , o wzorze a 2 β C 2, Co odpowiada substytucję E6K, wymiana z glutaminianem reszty w pozycji 6 przez lizynę pozostałości . Pierwsza ma krótki, ujemnie naładowany łańcuch boczny , podczas gdy druga ma długi, dodatnio naładowany łańcuch boczny, który wpływa na ogólną plastyczność erytrocytów . W heterozygot posiada 28% do 44% hemoglobiny C, która pozostaje bezobjawowy, a homozygoty posiada 100% hemoglobiny C, co powoduje łagodną anemię hemolityczną . Gen hemoglobina C występuje głównie w Afryce Zachodniej , gdzie może mieć przewagę ochronnego przeciwko malarii jak inne hemoglobinopatiami, a także w południowej Europie , Ameryce Łacińskiej i regionach. Karaiby ;
- hemoglobiny E " o wzorze a 2 β E 2, co odpowiada podstawieniu E26K, zastąpieniu reszty glutaminianu w pozycji 26 resztą lizyny. Ta mutacja dotyka około 1 miliona ludzi na całym świecie, głównie w Azji Południowo-Wschodniej . To wpływa na ekspresję z beta-globiny przez indukowanie alternatywne splotów na RNA w kodonach 25-27, stąd deficyt w produkcji zwykłego beta-globiny, który prowadzi do p-talasemii . Ponadto podjednostki β E oddziałują słabiej z podjednostkami α, co powoduje, że cząsteczki hemoglobiny E są mniej stabilne w obecności utleniaczy ;
- hemoglobiny S , o wzorze α 2 β S 2, co odpowiada podstawieniu E6V, zastąpieniu reszty glutaminianu w pozycji 6 resztą waliny . To podstawienie, które umieszcza resztę aminokwasu hydrofobową na powierzchni białka, tworzy strefę adhezji, która sprzyja wytrącaniu się hemoglobiny S w długich włóknach, które wydłużają erytrocyty, dając im sierp ( po angielsku sierp , stąd „S”) tego wariantu), stąd też i tej chorobie nadana jest nazwa anemia sierpowata, zwana także anemią sierpowatą . Gen S występuje głównie w Afryce Subsaharyjskiej , na Bliskim Wschodzie i w środkowych Indiach : w 2013 r. Oszacowano na 3,2 mln liczbę homozygot cierpiących na niedokrwistość sierpowatą oraz na 43 mln heterozygot z cechą sierpowatokrwinkową. . Ich anemia chroni je przed malarią , stąd selektywna zaleta, która sprzyja występowaniu genu sierpowatokrwinkowego w regionach dotkniętych malarią.
Cząsteczki analogowe
W roślinach i zwierzętach występuje wiele różnych białek, które wiążą się z tlenem w celu przechowywania lub transportu. Te bakterie , tym pierwotniakami i grzybami mieć wszystkie także hemoglobiny pokrewnych białek, które ze swojej znane lub przewidywane funkcji powiązać z ligandów gazowych odwracalny. Oprócz transportu i wykrywania tlenu, białka te mogą brać udział w usuwaniu tlenu z ośrodków, o których uważa się, że pozostają beztlenowe , jak ma to również miejsce w przypadku leghemoglobiny .
Ponieważ wiele takich białek składa się z globin i hemu , są one często określane jako „hemoglobina”, mimo że ich ogólna struktura bardzo różni się od hemoglobiny u kręgowców . W szczególności rozróżnienie między mioglobiną i hemoglobiną jest często niemożliwe u najprostszych zwierząt przy braku mięśni u tych ostatnich, podczas gdy układ krążenia większości owadów nie bierze udziału w dyfuzji tlenu do organizmu. Szereg stawonogów ( pająki , skorpiony , niektóre skorupiaki ) wykorzystuje się dziurki od klucza , który jest zawierającym miedź wolnego hemu, ale stosując kationy z miedzi bezpośrednio skoordynowane z reszt od histydyny , a białko nie jest homologiczna z hemoglobiną.
Struktura hemoglobin jest bardzo zróżnicowana w zależności od rozpatrywanego gatunku. W bakteriach, pierwotniakach, algach i roślinach występuje często monoblobina , podczas gdy wiele nicieni , mięczaków i skorupiaków ma bardzo duże białka zawierające znacznie większą liczbę podjednostek niż u kręgowców. W szczególności grzyby i pierścienice posiadają chimeryczne hemoglobiny zawierające zarówno globiny, jak i inne rodzaje białek. Zatem, olbrzymia rura robaka z tych hydrotermalnych zawiera wiele hemoglobiny, zawierający nie mniej niż 144 podjednostki globiny, każdy związany z grupą hemu, którego zadaniem jest wychwytywania tlenu O 2i siarkowodór H 2 Sniezbędny dla bakterii żyjących z nim w symbiozie , a także dwutlenku węgla CO 2niezbędny do anabolizmu robaka. Struktury te są niezwykłe, ponieważ mogą transportować tlen w obecności jonów siarczkowych i same transportować te jony bez ich zatrucia, podobnie jak hemoglobiny innych gatunków.
Wśród białek innych niż hemoglobina zdolnych do wiązania się z tlenem można zachować następujące cząsteczki:
- Mioglobina - występująca w mięśniach większości kręgowców , w tym ludzi , nadaje tym tkankom czerwony lub ciemnoszary odcień. Jego struktura jest bardzo podobna do podjednostek globiny hemoglobiny, ale jest monomeryczna , a zatem nie wykazuje efektu współpracy poprzez wiązanie się z tlenem. Jest bardziej zaangażowany w magazynowanie tlenu niż jego transport.
- Hemocyjanina - jest drugim po hemoglobinie najpowszechniejszym nośnikiem tlenu w przyrodzie, występuje w wielu stawonogach i mięczakach . Wykorzystuje grupę protetyczną składającą się z miedzi, a nie żelaza hemowego , i po natlenianiu wykazuje niebieski kolor.
- Hemerytryna - niektóre bezkręgowce morskie i niektóre gatunki pierścienic wykorzystują to niehemowe białko żelaza do transportu tlenu. Ma różowy lub fioletowy kolor, gdy jest natleniony i jest przezroczysty, gdy nie jest natleniony.
- Chlorokruoryna - występująca w wielu pierścieniach, jest bardzo podobna do erytrokruoryny, ale jej grupa hemowa ma wyraźnie inną strukturę. Jest czerwony, gdy jest natleniony, i zielony, gdy jest odtleniony (stąd jego nazwa).
- Erytrokruoryna - występuje w wielu pierścienicach, w tym w dżdżownicach , jest to bardzo duże białko, które może zawierać ponad sto podjednostek białka i jednostek hemu, z których wszystkie mają masę cząsteczkową do 3600 kDa .
- Leghemoglobiny - obecny w strąkach , takich jak lucerny i soi , ma działanie zabezpieczające bakterii wiążących azot tlen pozwalają nitrogenazy do zmniejszenia się azot , który może to zrobić w obecności tlenu.
Zastosowanie kliniczne
W medycynie kilka terminów odnosi się do hemoglobiny:
- Poziom hemoglobiny jest wyrażony wg / 100 ml . Prawidłowe wartości hemoglobiny zależą od płci i wieku badanego. Poziom hemoglobiny poniżej normy definiuje anemię . Wartości referencyjne są wyższe dla mężczyzn niż dla kobiet. Jedno z badań kwestionuje poziomy odniesienia dla hemoglobiny, argumentując, że posiadanie różnych wartości odniesienia dla hemoglobiny dla mężczyzn i kobiet nie jest uzasadnione.
- Nasycenia SaO 2definiowany jako% jest obliczany przez podzielenie ilości oksyhemoglobiny przez całkowitą ilość hemoglobiny we krwi. Nasycenia SaO 2można mierzyć na krwi żylnej lub tętniczej. Jednym z parametrów badania zwanego gazometrią jest wysycenie krwi tlenem . Wartość nasycenia jest uważana za niebezpieczną, jeśli jest mniejsza niż 90% dla krwi tętniczej. Normalna wartość to około 96-100% dla normalnych warunków atmosferycznych. Przy tej wartości mówimy o pojemności O 2krew .
- Sinica jest objawem klinicznym. To jest niebieskawe zabarwienie powłok. Pojawia się, gdy obniżone stężenie hemoglobiny przekracza 5 g / 100 ml krwi włośniczkowej. Może być zamaskowany anemią.
Genetyczne choroby hemoglobiny
Podobnie jak wiele białek, łańcuchy hemoglobiny wykazują różne mutacje, które najczęściej nie mają wpływu klinicznego. Zidentyfikowano ponad 500 nieprawidłowych hemoglobin. Niektóre mutacje (Hb Köln, Indianapolis itp.) Powodują niestabilność wytrącającego się tetrameru w ciele Heinza lub methemoglobinemię (hemoglobina M).
Czasami ta mutacja powoduje nienormalne powinowactwo do tlenu, to znaczy, tak jak Hb Hope, spadek powinowactwa z wysokim P50 dającym dobrze tolerowaną anemię i sinicę w spoczynku, wysiłek i wysokość są źle podtrzymywane., Lub tak jak Hb Chesapeake, Malmö lub Olympia, wzrost powinowactwa z obniżoną P50 i kompensacyjną czerwienicą prowadzącą do objawów klinicznych od pewnego wieku.
Inni mogą być odpowiedzialni za przewlekłą hemolizę, HbS (przez mutację glutaminy do waliny, która spowoduje polimeryzację Hb), HbC, lub pogorszyć w stanie heterozygotycznym inną hemoglobinopatię, HbO Arab, HbD Punjab lub Hb Lepore lub β-talasemię, HbE.
Wreszcie uszkodzenie genetyczne może dotyczyć nie pierwotnej struktury białka, ale ilościowego defektu w jego syntezie lub nienormalnie wysokiej trwałości hemoglobiny płodowej HbF.
Wady syntezy, czyli anomalia molekularna są opisane pod nazwami:
Historyczny
Pierwsze badania hemoglobiny zostały przewiezione do XIX th wieku w Niemczech . Odkryta w 1840 roku przez Hünefelda, hemoglobina została skrystalizowana w 1851 roku przez Otto Funke (en) i to Felix Hoppe-Seyler zademonstrował odwracalne wiązanie tlenu na tym białku w 1866 roku. Tetrameryczny charakter i masa cząsteczkowa hemoglobiny zostały ustalone przez Gilbert Smithson Adair (en) w 1925 r., Mierząc ciśnienie osmotyczne roztworów hemoglobiny, który również zidentyfikował podstawy wspólnego efektu wiązania tlenu z tym białkiem przez allosteria .
Trójwymiarową strukturę hemoglobiny została założona przez Max Perutz w 1959 roku przez krystalografii rentgenowskiej , co doprowadziło do jego udostępniania 1962 Nagrodę Nobla w dziedzinie chemii z John Kendrew , który prowadził podobną pracę na mioglobiny .
Hemoglobina w sztuce
W 2005 roku artysta Julian Voss-Andreae stworzył rzeźbę Heart of Steel (Hemoglobin) , wzorowaną na kręgosłupie białka. Rzeźba wykonana jest ze szkła i stali Corten . Zardzewiały wygląd dzieła jest zamierzony i wywołuje fundamentalną reakcję chemiczną wiązania tlenu z żelazem zawartym w hemoglobinie.
Artysta z Montrealu Nicolas Baier stworzył rzeźbę Luster (Hemoglobin) , polerowaną rzeźbę ze stali nierdzewnej, która pokazuje strukturę cząsteczki hemoglobiny. Rzeźba znajduje się w atrium centrum badawczego McGill University Health Center w Montrealu. Wielkość rzeźby to około 10 metrów na 10 metrów na 10 metrów.
Uwagi i odniesienia
- (w) G. Fermi, MF Perutz i B. Shaanan , „ Struktura krystaliczna ludzkiej deoksyhemoglobiny przy rozdzielczości 1,74 A ” , Journal of Molecular Biology , tom. 175 n O 2 15 maja 1984, s. 159-174 ( PMID 6726807 , DOI 10.1016 / 0022-2836 (84) 90472-8 , czytaj online )
- Wartości masy i liczba reszt wskazanych tutaj są związki o prekursora białka otrzymanego z translacji z genu przed potranslacyjnych modyfikacji , i mogą różnią się znacznie od wartości odpowiadających wartościom dla funkcjonalnego białka .
- (w) Robert I. Weed, Claude F. Reed i George Berg , „ Czy rok strukturalny hemoglobiny jest niezbędnym składnikiem ludzkich błon erytrocytów? ” , Journal of Clinical Investigation , vol. 42,Kwiecień 1963, s. 581-588 ( PMID 13999462 , PMCID 289318 , DOI 10,1172 / JCI104747 , czytać online )
- (w) E. Domínguez de Villota, MT García Carmona, JJ Rubio i S. Andrés Ruiz , „ Równość zdolności wiązania tlenu in vivo i in vitro hemoglobiny u pacjentów z ciężkimi chorobami układu oddechowego ” , British Journal of Anesthesia , vol. 53 N O 12,Grudzień 1981, s. 1325-1328 ( PMID 7317251 , PMCID 289318 , DOI 10.1093 / BJA / 53.12.1325 , czytać online )
- (w) Connie CW Hsia , „ Funkcja oddechowa hemoglobiny ” , The New England Journal of Medicine , vol. 338 n O 4, 22 stycznia 1998, s. 239-247 ( PMID 9435331 , DOI 10.1056 / NEJM199801223380407 , czytaj online )
- (w) Mr. Biagioli, Mr. Pinto, D. et al Cesselli. , „ Niespodziewana ekspresja α- i β-globiny w śródmózgowiowych neuronach dopaminergicznych i komórkach glejowych ” , Proceedings of the National Academy of Sciences of the United States of America , vol. 106 n O 36, 8 września 2009, s. 15454-15459 ( PMID 19717439 , PMCID 2732704 , DOI 10.1073 / pnas.0813216106 , czytaj online [PDF] )
- (en) Roy E. Weber i Serge N. Vinogradov, „ Nonvertebrate hemoglobins: functions and molecular adaptations ” , Physiological Review , tom. 81 N O 2, Kwiecień 2001, s. 569-628 ( PMID 11274340 , czytaj online )
- (w) Ross C. Hardison , „ Krótka historia hemoglobin: roślin, zwierząt, protistów i bakterii ” , Proceedings of the National Academy of Sciences of the United States of America , vol. 93 N O 12, 11 czerwca 1996, s. 5675-5679 ( PMID 8650150 , PMCID 39118 , DOI 10.1073 / pnas.93.12.5675 , JSTOR 39604 , Bibcode 1996PNAS ... 93.5675H , czytaj online )
- (w) Mireille Van CP Beekvelt Willy NJM Colier, Ron A. Wevers i Van Engelen Baziel GM , „ Wydajność spektroskopii w bliskiej podczerwieni w lokalnym zużyciu O2 i pomiarze przepływu krwi w mięśniach szkieletowych ” , Journal of Applied Physiology , vol. 90 N O 2 Luty 2001, s. 511-519 ( PMID 11160049 )
- (en) RD Shannon , „ Effective ionic radii Revised and systematic studies of interatomic distance in halides and Chalcogenides ” , Acta Crystallographica Section A: Crystal Physics, Diffraction, Theoretical and General Crystallography , Vol. 32, n o 5 września, str. 1976 ( DOI 10.1107 / S0567739476001551 , Bibcode 1976AcCrA..32..751S , czytaj online )
- (w) Wray H. Huestis i Michael A. Raftery , „ Konformacja i kooperatywność w hemoglobinie ” , Biochemistry , tom. 14 N O 9,6 maja 1975, s. 1886-1892 ( PMID 235969 , DOI 10.1021 / bi00680a013 , czytaj online )
- (w) Frank B. Jensen , „ Podwójne role czerwonych krwinek w dostarczaniu tlenu do tkanek: nośniki tlenu i regulatory lokalnego przepływu krwi ” , Journal of Experimental Biology , t. 212 n O Pt 21listopad 2009, s. 3387-3393 ( PMID 19837879 , DOI 10.1242 / jeb.023697 , czytaj online )
- (w) D. Nicholas Bateman , „ Tlenek węgla ” , Medycyna , t. 31 N O 10, Październik 2003, s. 41-42 ( DOI 10.1383 / medc.31.10.41.27810 , czytaj online )
- (in) CL i RL Townsend Maynard , „ Wpływ na zdrowie długotrwałego narażenia na niskie stężenia tlenku węgla ” , Medycyna pracy i środowiskowa , tom. 59 N O 10, Październik 2002, s. 708-711 ( PMID 12356933 , PMCID 1740215 , DOI 10.1136 / oem 59.10.708 , JSTOR 27731796 , czytaj online )
- (w) John Haldane , „ Działanie tlenku węgla na człowieka ” , The Journal of Physiology , tom. 18, n kość 5-6, 16 listopada 1895, s. 430-462 ( PMID 16992272 , PMCID 1514663 , DOI 10.1113 / jphysiol.1895.sp000578 , czytaj online )
- (w) Mark Goldstein , „ Zatrucie tlenkiem węgla ” , Journal of Emergency Nursing , tom. 34, n o 6, grudzień 2006, s. 538-542 ( PMID 19022078 , DOI 10.1016 / j.jen.2007.11.014 , czytaj online )
- (w) Tim Struttmann Amy Scheerer, T. Scott Prince i Linda A. Goldstein , „ Niezamierzone zatrucie tlenkiem węgla z mało prawdopodobnego źródła ” , Journal of the American Board of Family Medicine , t. 11 N O 6, Listopad-grudzień 1998, s. 481-484 ( PMID 9876005 , DOI 10.3122 / jabfm.11.6.481 , czytaj online )
- (w) Edward R. Burka , „ Charakterystyka degradacji RNA w komórkach erytroidalnych ” , Journal of Clinical Investigation , Vol. 48, n o 7, Lipiec 1969, s. 1266-1272 ( PMID 5794250 , PMCID 322349 , DOI 10.1172 / JCI106092 , czytaj online )
- (w) Goro Kikuchi, Tadashi Yoshida Masato Noguchi , " Oksygenaza hemowa i degradacja hemu " , Biochemical and Biophysical Research Communications , tom. 338 n o 1, 9 grudnia 2005, s. 558-567 ( PMID 16115609 , DOI 10.1016 / j.bbrc.2005.08.020 , czytaj online )
- (w) Ross C. Hardison , „ Ewolucja hemoglobiny i jej genów ” , Cold Spring Harbor Perspectives in Medicine , tom. 2 N O 12, Grudzień 2012, a011627 ( PMID 23209182 , PMCID 3543078 , DOI 10.1101 / cshperspect.a011627 , czytaj online )
- (in) Morris Goodman, William G. Moore i Genji Matsuda , „ Darwinian Evolution in the genealogy of hemoglobin ” , Nature , vol. 253 n O 5493, 20 lutego 1975, s. 603-608 ( PMID 1089897 , DOI 10.1038 / 253603a0 , Bibcode 1975Natur.253..603G , czytaj online )
- (en) Jay F. Storz, Juan C. Opazo i Federico G. Hoffmann , „ Duplikacja genów, duplikacja genomu i funkcjonalna dywersyfikacja globin kręgowców ” , Molecular Phylogenetics and Evolution , tom. 66 N O 2 luty 2013, s. 469-478 ( PMID 22846683 , PMCID 4306229 , DOI 10.1016 / j.ympev.2012.07.013 , czytaj online )
- (w) EA Zimmer, SL Martin, Beverley SM, YW Kan i AC Wilson , „ Szybka duplikacja i utrata genów kodujących łańcuchy alfa hemoglobiny ” , Proceedings of the National Academy of Sciences of the United States , vol. 77, n o 4, Kwiecień 1980, s. 2158-2162 ( PMID 6929543 , PMCID 348671 , DOI 10.1073 / pnas.77.4.2158 , czytaj online )
- (w) Cynthia M. Beall, Kijoung Song, Robert C. Elston i Melvyn C. Goldstein , „ Wyższe przetrwanie potomstwa tybetańskiego wśród kobiet z genotypami o wysokim nasyceniu tlenem zamieszkującym na wysokości 4000 m ” , Proceedings of the National Academy of Sciences of the United Stany Ameryki , t. 101 n O 39, 28 września 2004, s. 14300–14304 ( PMID 15353580 , PMCID 521103 , DOI 10.1073 / pnas.0405949101 , czytaj online )
- (i) Zhenning on i J. Russell Eric , „ Ekspresja, oczyszczanie i charakterystyka hemoglobiny ludzkiej Gower-1 (ζ 2 ε 2 ), Gower-2 (α 2 ε 2) i Portland-2 (ζ 2 β 2) złożone w złożone myszy transgeniczne - knockout ” , Blood , t. 97, n o 4,15 lutego 2001, s. 1099-1105 ( PMID 11159543 , czytaj online )
- (w) J. Eric Russell i Stephen A. Liebhaber , „ Reversal of Lethal α- i β-thalassemias in Mice by Expression of Human Embryonic globins ” , Blood , Vol. 92 N O 9, Listopad 1998, s. 3057-3063 ( PMID 9787139 , czytaj online )
- (w) Sophie Lanzkron John J. Strouse, Renee Wilson, Mary Catherine Beach, Carlton Haywood Park Haesong Catherine Witkop, Eric B. Bass i Jodi B. Segal , „ Systematic Review: Hydroxyurea for the Treatment of Adults with Sickle Cell Disease ” , Roczniki chorób wewnętrznych , t. 148 n O 12, 17 czerwca 2008, s. 939-955 ( PMID 18458272 , PMCID 3256736 , DOI 10.7326 / 0003-4819-148-12-200806170-00221 , czytaj online )
- (w) Amoz I. Chernoff Virginia Minnich, Supa Na Nakorn, Soodsarkorn Tuchinda, Channivat Kashemsant i Renate R. Chernoff , „ Badania nad hemoglobiną S - I. Kliniczna, hematologiczna i genetyczna charakterystyka zespołów hemoglobiny E ” , Dziennik Medycyny Laboratoryjnej i Klinicznej , t. 47, n o 3, Marzec 1956, s. 455-489 ( PMID 13353880 , czytaj online )
- (in) „ Częstość występowania, chorobowość i liczba lat w skali globalnej, regionalnej i krajowej Żył z niepełnosprawnością z powodu 301 ostrych i przewlekłych chorób i urazów w 188 krajach, 1990–2013: systematyczna analiza dla badania Global Burden of Disease 2013 ” , Lancet , vol. 386 n O 9995, 22 sierpnia 2015, s. 743-800 ( PMID 26063472 , DOI 10.1016 / S0140-6736 (15) 60692-4 , czytaj online )
- (w) William E. Royer Jr., Hitesh Sharma, Kristen Strand, James E. Knapp i Balaji Bhyravbhatla , „ Lumbricus Erythrocruorin at 3,5 A Resolution: Architecture of a megadalton Respiratory Complex ” , Structure , vol. 14 N O 7, lipiec 2006, s. 1167-1177 ( PMID 16843898 , DOI 10.1016 / j.str.2006.05.011 , czytaj online )
- (w) Luc Int Panis, Boudewijn Goddeeris i Rudolf Verheyen , „ Stężenie hemoglobiny Chironomus cf. Plumosus l. (Diptera: Chironomidae) larwy z dwóch siedlisk lentic ” , Netherland Journal of Aquatic Ecology , vol. 29, n o 1, Kwiecień 1995, s. 1-4 ( DOI 10.1007 / BF02061785 , czytaj online )
- (w :) Franck Zal, Francis H. Lallier, Brian N. Green, Serge N. Vinogradov i Andre Toulmond , „ System multi-hemoglobiny w hydrotermalnym robaku z rur wentylacyjnych. II. Kompletny skład łańcucha polipeptydowego zbadany za pomocą analizy maksymalnej entropii widm masowych ” , Journal of Biological Chemistry , tom. 271 n O 15, 12 kwietnia 1996, s. 8875-8881 ( PMID 8621529 , DOI 10.1074 / jbc.271.15.8875 , czytaj online )
- (w) Zoran Minic i Guy Hervé , „ jochemiczne i enzymologiczne aspekty symbiozy entre les głębinowych tubeworm olbrzym tubeworm i jego bakteryjny endosymbiont ” , The FEBS Journal , vol. 271 n O 15, Sierpień 2004, s. 3093-3102 ( PMID 15265029 , DOI 10.1111 / j.1432-1033.2004.04248.x , czytaj online )
- „ Jakie są dowody na różnice płci w ferrytynie i hemoglobinie? » (Dostęp 2 listopada 2019 r. )
- Hematologia Bernarda Dreyfusa, Médecine-Sciences- Flammarion, 1992
- (de) Felix Hoppe-Seyler , „ Über die oksydacja w lebendem blute ” , Med-chem Untersuch Lab , 1866, s. 133–140
- (w) Gilbert S. Adair , „ Ciśnienie osmotyczne hemoglobiny w nieobecności soli ” , Proceedings of the Royal Society of London. Seria B, zawierające dokumenty o charakterze biologicznym , t. 98, n o 692, Październik 1925, s. 524 ( DOI 10.1098 / rspa.1925.0126 , JSTOR 94515 , Bibcode 1925RSPSB..98..524A , czytaj online )
- (en) MF Perutz, Rossmann MG, Ann F. Cullis, Hilary MUIRHEAD, GEORG WILL & ACT NORTH , „ Structure of Hemoglobin: A Three-Dimensional Fourier Synthesis at 5,5-Å. Rozdzielczość, uzyskana przez analizę rentgenowską ” , Nature , vol. 185 n O 4.711 13 lutego 1960, s. 416-422 ( PMID 18990801 , DOI 10.1038 / 185416a0 , czytaj online )
- (en) Max Perutz F. , „ Struktura hemoglobiny ” , Brookhaven Symposia in Biology , vol. 13, 1960, s. 165-183 ( PMID 13734651 )
-
(w) „ Nagroda Nobla w dziedzinie chemii w 1962 r. ” (Dostęp 6 listopada 2016 r. ) :
„ Nagroda Nobla w dziedzinie chemii w 1962 r. Została przyznana wspólnie Maxowi Ferdinandowi Perutzowi i Johnowi Cowdery Kendrew„ za badania struktur białek kulistych ” . "
- (w) Constance Holden , „ Blood and Steel ” , Science , vol. 309 n O 5744,30 września 2005, s. 2160 ( DOI 10.1126 / science.309.5744.2160d , przeczytaj online [PDF] )
- (w) Moran L Horton RA Scrimgeour G, Perry M, Principles of Biochemistry , Boston, MA, Pearson ,2011, 786 s. ( ISBN 978-0-321-70733-8 i 0-321-70733-8 ) , str. 127
- (w) Sean Henry, „ Rzuć okiem na kolekcję dzieł sztuki MUHC ” w CBC News ,7 sierpnia 2014(dostęp na 1 st lutego 2016 )
- " Luster (hemoglobina) 2014 " na Public Art Montrealu (dostęp na 1 st lutego 2016 )
- " Nicolas Baier " na McGill University Health Centre (dostęp na 1 st lutego 2016 )
Zobacz też
Bibliografia
- Banerjee, R., & Sagaert, L. (1967). Dysocjacja ludzkiej hemoglobiny w środowisku kwaśnym . Biochimica and Biophysica Acta (BBA) -Protein Structure, 140 (2), 266-273 ( streszczenie ).
- Blum, N., Maleknia, M. i Schapira, G. (1970). Wolne α- i β-globiny oraz biosynteza hemoglobiny. Biochimica et Biophysica Acta (BBA) -Nucleic Acids and Protein Synthesis, 199 (1), 236–247.
- Breton-Gorius, J. (1970). Zastosowanie diaminobenzydyny do demonstracji pod mikroskopem elektronowym hemoglobiny wewnątrzkomórkowej . Nowy Obrót silnika. Fr. Hematology, 10, 243-256.
- Caffin, JP, Chauvet, JP i Acher, R. (1969). Hemoglobiny płazów: oddzielenie i wstępna charakterystyka łańcuchów hemoglobiny ropuchy Bufo bufo . Listy FEBS, 5 (3), 196-198 ( streszczenie ).
- Bardakdjian-Michau, J., Dhondt, JL, Ducrocq, R., Galactéros, F., Guyard, A., Huchet, FX, ... & Wajcman, H. (2003, lipiec). Dobre praktyki w badaniu hemoglobiny . W Annals of Clinical Biology (tom 61, nr 4, str. 401-409).
- Bernard, M., Bordas-Fonfrède, M., Grimaldi, A., Guillemin, C., Stahl, A., Leutenegger, M., & Gillery, P. (1995). Odpowiednie zainteresowania oznaczeniami hemoglobiny glikowanej i fruktozaminy w monitorowaniu cukrzycy . W Annals of Clinical biology (tom 53, nr 6, str. 321-327). John Libbey Eurotext.
- Bert, P. (1882). O bogactwie hemoglobiny we krwi zwierząt żyjących na wyżynach. CR Acad Sci Paris, 94, 805–807.
- Bloch-Raphaël, C. (1939). Lokalizacja, powstawanie i niszczenie hemoglobiny w pierścienicach wieloszczetów (rozprawa doktorska).
- Eaton, WA i Hofrichter, J. (1990). Polimeryzacja hemoglobiny sierpowatokrwinkowej . Postępy w chemii białek, 40, 263-279.
- Foettinger, A. (1880). O istnieniu hemoglobiny u szkarłupni . Łuk. Biol. Paryż, 1, 405–415.
- Kruh, J., Dreyfus, JC i Schapira, G. (1964). Aktywacja bezkomórkowej syntezy hemoglobiny przez kwas rybonukleinowy: III. Działanie całkowitego kwasu rybonukleinowego wątroby . Biochimica et Biophysica Acta (BBA) -Specialized Section on Nucleic Acids and Related Subjects, 91 (3), 494-505 ( streszczenie ).
- Kruh, J., Dreyfus, JC, Rosa, J. i Schapira, G. (1962). Synteza hemoglobiny przez bezkomórkowe układy retikulocytów . Biochimica et Biophysica Acta (BBA) -Specialized Section on Nucleic Acids and Related Subjects, 55 (5), 690-703.
- Lambert, PP, Grégoire, F. i Royers, E. (1955). Kłębuszkowa hemodynamika i wydalanie hemoglobiny . Archives Of Physiology And Biochemistry, 63 (1), 7-34 ( streszczenie ).
- Lena-Russo, D., North, ML, & Girot, R. (1992). Epidemiologia chorób hemoglobiny genetycznej we Francji metropolitalnej . The Practitioner Review, 42 (15), 1867-1872.
- Robert, M. (1975). Powinowactwo hemoglobiny do tlenu . Szpital kantonowy, oddział medyczny, przychodnia lecznicza.
- Uriel, J. (1958). Wykrywanie aktywności katalazy i peroksydazy hemoglobiny po elektroforezie agarowej . Biuletyn Towarzystwa Chemii Biologicznej, 40, 277-280.
- White, CT, Murray, AJ, Smith, DJ, Greene, JR i Bolin, RB (1986). Synergistyczna toksyczność endotoksyny i hemoglobiny. J Lab Clin Med, 108 (2), 132–137.