Podtlenek azotu
| Podtlenek azotu | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Cząsteczka tlenku azotu |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nazwa IUPAC | Podtlenek azotu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O ECHA | 100,030,233 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O WE | 233-271-0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kod ATC | R07 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 145068 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| UŚMIECHY |
N = O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / HNO / c1-2 / h1H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd | bezbarwny sprężony gaz. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości chemiczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formula |
N O [Izomery] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa cząsteczkowa | 30,0061 ± 0,0005 g / mol N 46,68%, O 53,32%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moment dwubiegunowy | 0,15872 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości fizyczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuzja | -163,6 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| * Temperatura wrzenia | -151,8 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozpuszczalność | w wodzie w 0 ° C : 7,4 ml / 100 ml | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa objętościowa |
1,3 kg · l -1 (płyn)
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nasycenie prężności par |
równanie:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punkt krytyczny | 65,8 bar , -93,35 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Szybkość dźwięku | 325 m · s -1 ( 10 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochemia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gaz S 0 , 1 bar | 211 J / Mol K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gaz Δ f H 0 | 90,29 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 ciecz | 87,7 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 13,83 kJ · mol -1 ( 1 atm , -151,74 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości elektroniczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 energia re jonizacji | 9,26438 ± 0,00005 eV (gaz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Środki ostrożności | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
    A, C, D1 A, E, A : Temperatura krytyczna sprężonego gazu = -93 ° C C : Materiał utleniający powoduje lub przyspiesza spalanie innego materiału poprzez uwolnienie tlenu D1A : Bardzo toksyczny materiał powodujący poważne natychmiastowe skutki Transport towarów niebezpiecznych: klasa 2.3 E : Materiał żrący Transport towarów niebezpiecznych : klasa 8 Stopień ujawnienia na poziomie 1,0% zgodnie z wykazem składników |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dyrektywa 67/548 / EWG | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 T +  VS  O Symbole : T + : Bardzo toksyczny C : Produkt żrący O : Utleniający Zwroty R : R8 : Kontakt z materiałami zapalnymi może spowodować pożar . R26 : Działa bardzo toksycznie przez drogi oddechowe. R34 : Powoduje oparzenia. Zwroty S : S9 : Przechowywać pojemnik w dobrze wentylowanym miejscu. S17 : Trzymać z dala od materiałów zapalnych. S26 : W przypadku kontaktu z oczami natychmiast przemyć dużą ilością wody i skonsultować się ze specjalistą. S28 : Zanieczyszczoną skórę natychmiast przemyć obficie… (odpowiednie produkty wskazane przez producenta). S45 : W przypadku awarii lub jeżeli źle się poczujesz, niezwłocznie zasięgnij porady lekarza - jeżeli to możliwe, pokaż etykietę. S36 / 37/39 : Nosić odpowiednią odzież ochronną, rękawice i ochronę oczu / twarzy. Zwroty R : 8, 26, 34, Zwroty S : 9, 17, 26, 28, 36/37/39, 45, |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
265 : trujący i utleniający gaz (sprzyja pożarowi) Numer UN : 1660 : TLENEK AZOTU SPRĘŻONY; lub TLENEK AZOTU, SPRĘŻONY Klasa: 2.3 Etykiety: 2.3 : Gazy toksyczne (odpowiadają grupom oznaczonym przez duże T, tj. T, TF, TC, TO, TFC i TOC). 5.1 : Substancje utleniające 8 : Substancje żrące    |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inhalacja | Niebezpieczne, mogą prowadzić do śmierci | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skóra | Drażniący | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oczy | Może powodować podrażnienie | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Przyjmowanie pokarmu | Używany w celach terapeutycznych, ale ma skutki uboczne i jest niebezpieczny w przypadku przedawkowania | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoksykologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Próg zapachu | niska: 0,29 ppm wysoka: 0,97 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednostki SI i STP, chyba że określono inaczej. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Tlenek azotu , tlenek azotu , tlenek azotu, albo NR jest związek chemiczny tworzy z atomem z tlenu i atomu azotu . Jest gazem w normalnych warunkach temperatury i ciśnienia . Jest ważnym neuroprzekaźnikiem u ssaków ; rozpuszczony, łatwo przenika przez błony biologiczne i przenosi się z jednej komórki do drugiej, stanowiąc „idealnego posłańca parakrynowego” .
Tlenek azotu (NO) nie powinien być mylony z innymi tlenkami azotu , takimi jak podtlenek azotu N 2 O, który jest nazywany „gazem rozweselającym” i który jest środkiem znieczulającym ogólnie, ani dwutlenkiem azotu NO 2 , niezwykle drażniącym i szkodliwym czerwonym -gaz brunatny, który powstaje w wyniku szybkiego utleniania NO przez tlen z powietrza.
Jego duża reaktywność (szczególnie w fazie rozpuszczalnej) w stosunku do związków rodnikowych, takich jak tlen cząsteczkowy - który jest dwurodnikiem - lub anion ponadtlenkowy wynika z faktu, że sam jest związkiem rodnikowym - całkowita elektronika jego spinu wynosi 1/2. W środowisku biologicznym okres półtrwania szacuje się na od 1 do 5 sekund, a nawet 30 sekund. Otrzymane nadtlenoazotyny są silnymi środkami utleniającymi i nitrującymi. To wyjaśnia wszechobecne skutki, które wciąż są słabo poznane, od odpowiedzi immunologicznej po ataki drobnoustrojów i procesy zapalne po wstrząs septyczny i śmierć neuronów w fazie niedokrwienia . Bierze również udział w komórkowych mechanizmach uczenia się pamięci , czy w zjawisku erekcji .
Efekty produkcyjne i środowiskowe
Gaz ten może być syntetyzowany w niewielkich ilościach przez wiele organizmów, w tym organizm ludzki.
W naturze w wysokiej temperaturze azot i tlen reagują tworząc tlenek azotu, na przykład pod wpływem wyładowań atmosferycznych .
Aktywność ludzkiej radykalnie zmienione wytwarzanie tlenku azotu w biosferze , ze względu na tworzenie się dużej ilości tego gazu w komorze spalania w silnikach spalinowych , w niektórych kotłów i maszyn przemysłowych, w niektórych procesach w przemyśle chemicznym . Jednym z celów katalizatorów spalin jest odwrócenie tej reakcji i zmniejszenie emisji tego gazu.
Nieruchomości
Właściwości chemiczne tlenku azotu są bardzo liczne. Poniżej znajduje się krótki przegląd metod jego przygotowania i szybkości reakcji.
Przygotowanie
Tlenek azotu powstaje z pierwiastków w wysokiej temperaturze, jak wspomniano powyżej.
Można go zsyntetyzować w laboratorium zgodnie z następującymi reakcjami redoks, w których pochodna azotu o stopniu utlenienia wyższym niż + II (kwas azotowy: + V; kwas azotawy: + III) jest poddawana działaniu odpowiedniego środka redukującego. Wszystkie te reakcje muszą być przeprowadzane pod nieobecność tlenu, ponieważ ten szybko utlenia NO do dwutlenku azotu. :
Stąd redukcja kwasu azotowego rozcieńczonego miedzią
8 HNO 3 + 3 Cu → 3 Cu (NO 3 ) 2 + 4 H 2 O + 2 NOlub kwasu azotawego (utworzonego in situ) przez jodek lub jony żelazawe
2 NaNO 2 + 2 NaI + 2 H 2 SO 4 → I 2 + 4 NaHSO 4 + 2 NO2 NaNO 2 + 2 FeSO 4 + 3 H 2 SO 4 → Fe 2 (SO 4 ) 3 + 2 NaHSO 4 + 2 H 2 O + 2 NOPoprzednia reakcja jest prostą metodą uzyskania NO w laboratorium.
Tlenek azotu można również otrzymać w środowisku bezwodnym dzięki redukcji azotanów i azotynów przez chrom (III):
3 KNO 2 (l) + KNO 3 (l) + Cr 2 O 3 (s) → 2 K 2 CrO 4 (s) + 4 NOPrzemysłowej syntezy NO obejmuje utleniania amoniaku za pomocą tlenu w obecności czerni platynowej do 750 do 900 ° C .
Reaktywność
Redukcja utleniania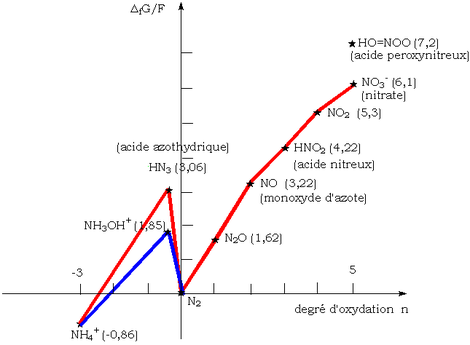
Schemat mróz na pH = 0 azotu wyraźnie pokazuje, że tlenek azotu jest niestabilny i nie powinny nieproporcjonalne do azotu N 2.i kwas azotowy HNO 3. W rzeczywistości bardzo łatwo utlenia się do dwutlenku azotu NO 2bardziej stabilne dzięki obecności tlenu w powietrzu. Dlatego czerwonawe opary tego ostatniego gazu są obserwowane, gdy miedź utlenia się stężonym kwasem azotowym.
Prawdopodobna hipoteza głosi, że dwurodnikowy O 2 wiąże się z dwoma rodnikami NO, dając ON-OO-NO, który następnie ulega rozerwaniu homolitycznemu prowadzącemu do NO 2 .
Jednak przy braku tlenu dysproporcjonuje on w temperaturze około 50 ° C do podtlenku azotu N 2 O(gaz rozweselający) i dwutlenek azotu NO 2(czerwone opary). W 25 ° C szybkość reakcji jest praktycznie zerowa, a NO jest tam metastabilny.
W roztworze wodnym NO rozpuszcza się dając kwas azotawy HNO 2, zgodnie z następującym możliwym schematem reakcji:
4 NO + O 2 + 2 H 2 O → 4 HNO 2NO reaguje z fluorem , chlorem i bromem, dając związki typu X-NO, znane jako halogenki nitrozylu. Jod jest zbyt słabo utleniający, aby powodować tworzenie się jodku nitrozylu.
Jodotrifluorometan reaguje z NO, dając jeden z niewielu znanych niebieskich gazów, nitrozotrifluorometan:
NIE + CF 3 I → I 2 + CF 3 NOSzybkość tworzenia jonu nadtlenoazotynowego z tlenku azotu i jonu ponadtlenkowego wynosi 1,9 x 10 10 mol- 1 s- 1 , co implikuje obecność nadtlenoazotynu in vitro i in vivo przy mniejszym nadmiarze jego dwóch prekursorów.
DimeryzacjaW przeciwieństwie do dwutlenku azotu, tlenek azotu nie ma tendencji do dimeryzacji. To zachowanie przypisuje się rozkładowi pojedynczego elektronu w całej cząsteczce, a także temu, że najbardziej prawdopodobna struktura O = NN = O pozostawiłaby całkowitą liczbę wiązań niezmienioną (2 × 2,5).
W fazie ciekłej następuje częściowa dimeryzacja. Forma C 2v (cis) jest bardziej stabilna niż jej homolog trans, a forma C 2h (prostokątna cząsteczka z wiązaniem atomu azotu jednej cząsteczki z atomem tlenu drugiej i odwrotnie) nie jest obserwowana.
Obliczenia ab inito SCF wykazały, że postać cis dimeru (NO) 2 miałaby odległości d (NN) = 174 μm id (OO) = 116 μm i kąt ONN = 107 °. Wartości te znacznie różnią się od tych wydedukowanych z nieuporządkowanych danych z dyfrakcji rentgenowskiej na fazie stałej (patrz rysunek obok). Ta rozbieżność wartości potwierdza trudność badania dimeru, którego tworzenie jest ulotne.
Tlenek azotu jest również ligandem
Cząsteczka tlenek azotu jest związana z tą tlenku węgla CO, z tą różnicą, że ma dodatkowy elektron, który zajmuje anty klejenie orbitalnej . W ten sposób NO tworzy kompleksy tego samego typu jak te utworzone z CO, przy czym kąt wiązania MN = O jest praktycznie równy 180 ° - w rzeczywistości ten kąt waha się między 160 ° a 180 ° .
Dlatego te kompleksy są uważane za liniowe. W tym przypadku azot formalnie włącza swój wolny dublet w wiązanie koordynacyjne. Jednak azot jest utleniany, ponieważ oddaje swój pojedynczy elektron metalowi, który koordynuje, a zatem jest on redukowany. Tak więc kompleksy tetrakarbonylonickelu, nitrozylotrikarbonylokobaltu i dikarbonylodinitrozylofera są izostrukturalne (tetraedryczne), ponieważ są izoelektroniczne .
N O mogą tworzyć kompleksy przekazując tylko jednego elektronu z metalu. Prowadzi to do grupy MNO, w której kąt wiązania wynosi od 120 ° do 140 ° .
Może również działać jako pomost między dwoma metalowymi centrami za pośrednictwem azotu.
Reakcje kompleksów nitrozylowychChemia związków koordynujących NO jest obszerna i zostanie omówiona tylko pokrótce. Na przykład NO jest wstawiany pomiędzy niob i ligand metylowy w następującej reakcji:
Charakterystyka skoordynowanego NOKońcowe NO można rozpoznać po ich intensywnej absorpcji w podczerwieni przy 1610 cm -1 . Liczby fal absorpcji IR pochodnych kątowych są niższe.
Analiza ilościowa
Najbardziej klasyczna ilościowa analiza tlenku azotu obejmuje prostą reakcję chemiluminescencyjną z ozonem.
patrz Pomiar tlenków azotu
Próbka zawierająca NO jest mieszana z nadmiarem ozonu. Tlenek azotu reaguje z wytworzeniem tlenu i di tlenku z azotem . Reakcja uwalnia również energię w postaci fal elektromagnetycznych w widzialnym: to jest chemiluminescencja. Natężenie wytwarzanego światła, mierzone za pomocą fotodetektora, jest proporcjonalne do ilości tlenku azotu. Przykładem terapeutycznego zastosowania NO jest jego pomiar w wydychanym powietrzu pacjentów (głównie astmatyków). Zasada polega na wdmuchiwaniu aparatu do chemiluninescencji i mierzeniu wydychanego NO, a tym samym mierzeniu stanu zapalnego dróg oddechowych.
Możliwe jest również oznaczanie różnymi metodami elektrochemicznymi ( potencjometria z nadmanganianem potasu , polarografia )
Zastosowania techniczne
Funkcje biologiczne
NO to endogenna cząsteczka uwalniana przez komórki śródbłonka , makrofagi , komórki wątroby i neurony .
W organizmie tlenek azotu pełni kilka funkcji.
Jest naturalnie syntetyzowana przez organizm z L- argininy i tlenu przez kilka enzymów zwanych syntazami NO (NOS), które są hemoproteinami zbliżonymi do cytochromu P450. Katalizator do utleniania przez tlen grupy iminourea argininy jest zatem żelazo od hemu , który przechodzi ze stopnia utlenienia II do + stopni + III + IV i i vice versa.
Wiązanie NO w niskiej masie cząsteczkowej tioli - takich jak glutation - prowadzi do wytworzenia S-nitrozotiole, co byłoby ważnym czynnikiem w aktywności transportu i NO. Związki te mogą następnie działać jako donory NO i tym samym znacznie zwiększać ich okres półtrwania.
Aktywność komórkowa tlenku azotu przebiega dwoma zasadniczymi szlakami, polegającymi na wytwarzaniu wewnątrzkomórkowego cyklicznego monofosforanu guanozyny (cGMP) z trifosforanu guanozyny (GTP) oraz tworzeniu cytotoksycznych nadtlenoazotynów. Wzrost stężenia cyklicznego GMP wiąże się z aktywacją cytoplazmatycznej ( niebłonowej ) cyklazy guanylanowej .
Rozszerzający naczynia krwionośne
Śródbłonka z naczyń krwionośnych, nie wykorzystuje do wyzwalania relaksacji jego mięśni gładkich bluzy , co powoduje rozszerzenie naczyń i zwiększenie przepływu krwi i zmniejszenia agregacji płytek krwi (trombocytów) . Jest to najważniejszy z „nieadrenergicznych, niecholinergicznych” neuroprzekaźników ; działa przy erekcji (penis, łechtaczka, sutki), a także wydaje się odgrywać ważną rolę w zachowaniu śródbłonka . Stwierdzono, że u dużej części ludzi ta synteza NO jest niewystarczająca, co zwiększa ryzyko wystąpienia chorób układu krążenia . Ten mechanizm wyjaśnia zastosowanie azotanów, takich jak tritrinitryna, w leczeniu tych samych chorób serca: Leki te są przekształcane w NO, w sposób jeszcze nie do końca zrozumiały, co z kolei rozszerza tętnice wieńcowe , naczynia krwionośne irygują serce, zwiększenie jej ukrwienia.
EDRF (czynnik relaksujący pochodzący ze śródbłonka) to stara nazwa NO. Byli lekarze zauważyli jego rolę środka rozszerzającego naczynia krwionośne, ale nie zidentyfikowali go jeszcze chemicznie.
Środek bakteriobójczy
Te makrofagi , komórki układu odpornościowego , wytwarzają NO w celu wyeliminowania bakteryjnych czynników chorobotwórczych nie który może, w pewnych przypadkach może powodować szkodliwe skutki uboczne, to jest w przypadku tak zwanej piorunującego zakażenia posocznicy , w którym Nadmierne wytwarzanie NO w makrofagach prowadzi do masywne rozszerzenie naczyń krwionośnych , główna przyczyna niedociśnienia tętniczego we wstrząsie septycznym .
Neurotransmitter
NO działa jako neuroprzekaźnik między komórkami nerwowymi . W przeciwieństwie do większości innych neuroprzekaźników, których działanie w szczelinie synaptycznej jest ukierunkowane wyłącznie na neuron postsynaptyczny, mała cząsteczka NO dyfunduje szeroko i może dotrzeć do kilku otaczających neuronów, w tym neuronów niepołączonych synapsami. Uważa się, że proces ten jest związany z zapamiętywaniem poprzez zapewnienie zapamiętywania długoterminowego . W endokanabinoidy , lipidowe neuroprzekaźników, mają podobne właściwości dyfuzyjne.
Relaksujące mięśnie gładkie
NO występuje w wielu narządach przewodu pokarmowego jako neuroprzekaźnik nieadrenergiczny, niecholinergiczny. Odpowiada za rozluźnienie mięśni gładkich przewodu pokarmowego. W szczególności zwiększa zdolność żołądka do przechowywania płynów spożywczych.
Regulator apoptozy
Tlenek azotu jest podstawowym regulatorem apoptozy komórek. Może mieć działanie przeciwapoptotyczne lub odwrotnie, efekt apoptotyczny. Ten przełącznik jest ściśle powiązany z obecnością lub brakiem reduktorów komórkowych, takich jak glutation .
W obecności wysokiego poziomu jonu ponadtlenkowego O 2 - tlenek azotu umożliwia tworzenie się jonu nadtlenoazotynowego , odpowiedzialnego prawdopodobnie za modyfikację potencjału błony mitochondrialnej, a także wiele zjawisk apoptozy komórkowej, w szczególności apoptozy komórek, w szczególności komórek układ odpornościowy.
Egzogenni dawcy NO
Są to substancje z jednym lub więcej wiązaniami azot - tlen, azot - azot lub hamujące niszczenie NO ( viagra ). Są azotany , azotyny , azotany, azydki ...
Zastosowania terapeutyczne
Zastosowania terapeutyczne:
- Jest stosowany w medycynie jako wziewny środek rozszerzający naczynia krwionośne . Stosowanie wziewnych leków rozszerzających naczynia krwionośne wybiórczo rozszerzających naczynia krwionośne naczyń włosowatych w dobrze wentylowanych obszarach płuc. Umożliwia to zmniejszenie tętniczego nadciśnienia płucnego związanego z niedotlenieniem skurczu naczyń i zwiększenie utlenowania krwi.
- Związek zwany Asymmetric Dimethyl Arginine (ADMA) jest znanym inhibitorem syntezy NO i dlatego jest uważany za biologiczny marker dysfunkcji sercowo-naczyniowej.
- Produkcja NO odgrywa również ważną rolę w osiągnięciu i utrzymaniu długotrwałej erekcji. Zwiększone stężenie cGMP prowadzi do lepszego rozszerzenia naczyń krwionośnych i erekcji. Uważa się, że efekt „ poppers ” otrzymuje się także za pośrednictwem NO, co powoduje rozluźnienie mięśni gładkich włókien, które otaczają tętniczek zaopatrujących ciał jamistych z penisem i zwiększając przepływ krwi. Sildenafilu (Viagra) i tadalafil (Cialis) stanowią konkurencyjne inhibitory tego enzymu fosfodiesterazy typu 5 (PDE5) odpowiedzialnej za dezaktywację cyklicznego GMP w GMP.
Odkrycie biologicznych właściwości NO w latach 80. było zupełnie nieoczekiwane i wywołało pewne zamieszanie. W 1992 r. Czasopismo Naukowe nazwane „Molekułą Roku” NIE, powstało Towarzystwo Naukowe NO i ukazało się czasopismo naukowe w całości poświęcone NO. Nagroda Nobla w dziedzinie fizjologii i medycyny otrzymał w 1998 roku do Ferid Murad , Robert Furchgott i Louis J. Ignarro za pracę o funkcjach neurotransmisją NO. Ta praca jest podstawą powstania francuskiej firmy farmaceutycznej Nicox . Szacuje się, że 3000 rocznie publikuje artykuły naukowe dotyczące roli tlenku azotu w biologii .
bezpieczeństwo
Odniesienie ONZ do transportu towarów niebezpiecznych :
- Nazwa (w języku francuskim): Tlenek azotu, skompresowany
- Klasa: 2
- numer: 1660
Bibliografia
- Nathan S Bryan, Janet Zand, Bill Gottlieb, Rozwiązanie: tlenek azotu (NO) , Naukowo-Techniczny Instytut Środowiska i Zdrowia (ISTES), 2014, strony 188.
Uwagi i odniesienia
- TLENEK AZOTU , Karta (y) Bezpieczeństwa Międzynarodowego Programu Bezpieczeństwa Chemicznego , konsultacja 9 maja 2009
- (w) David R. Lide, Podręcznik chemii i fizyki , CRC,16 czerwca 2008, 89 th ed. , 2736 str. ( ISBN 978-1-4200-6679-1 i 1-4200-6679-X ) , str. 9-50
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- (en) Robert H. Perry i Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , str. 2-50
- „ Properties of Various Gases ” na stronie flexwareinc.com (dostęp 12 kwietnia 2010 )
- (w) W. M Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 s. ( ISBN 978-1-4398-2077-3 ) , str. 14-40
- (w) Irvin Glassman, Richard A. Yetter, Combustion , Elsevier,2008, 4 th ed. , 773 s. ( ISBN 978-0-12-088573-2 ) , str. 6
- (w) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 s. , Twarda oprawa ( ISBN 978-1-4200-9084-0 )
- (w) David R. Lide, Podręcznik chemii i fizyki , CRC,2008, 89 th ed. , 2736 str. ( ISBN 978-1-4200-6679-1 ) , str. 10-205
- „ Tlenek azotu ” w bazie produktów chemicznych Reptox z CSST (Quebec organizacji odpowiedzialnej za bezpieczeństwo i higienę pracy), dostęp 25 kwietnia 2009
- „ Tlenek azotu ” , na hazmap.nlm.nih.gov (dostęp 14 listopada 2009 )
- Crépel, F. i Lemaire, G. (1995) Tlenek azotu . ; Czasopismo MS (medycyna / nauka); 11: 1639-42 (PDF, 4 strony)
- Gabbai, FB, Garcia, GE i wsp. , Rola tlenku azotu w fizjologii i patofizjologii kłębuszków , Adv Nephrol Necker Hosp 24, 3-18 (1995)
- RA Schroeder i PC Kuo, Tlenek azotu: fizjologia i farmakologia , Anesth Analg 81, 1052-9 (1995)
- Entalpia izomeryzacji jonu nadtlenoazotynowego do azotanu
- Sennequier, N. i Vadon-Le Goff, S. (1998). Biosynteza tlenku azotu (NO): mechanizm, regulacja i kontrola. SM. Médecine sciences, 14 (11), 1185-1195 ( http://cat.inist.fr/?aModele=afficheN&cpsidt=1584829 résumé])
- De Soete, G. (1993). Tlenek azotu ze spalania i przemysłu: chemia, emisje i kontrola Tlenek azotu ze spalania i przemysłu: chemia, emisje i techniki redukcji ( podsumowanie ).
- RB King; Chemia nieorganiczna głównych elementów grupy, VCH Publishers, Nowy Jork, 1995.
- Química Nova - Skład chemiczny nadtlenoazotynu, toksyny biologicznej
- Greenwood NN i Earnshaw A. (1997). Chemia pierwiastków. 2 th Ed. Elsevier, str. 446 .
- Skanckea PN i Boggsb JE (1973). Teoretyczne badanie struktury (NO) 2. Listy dotyczące fizyki chemicznej (21) str. 316-317 .
- Lipscomb WN, Wang FE, May WR i Lippert EL (1961). Uwagi dotyczące struktury 1,2-dichloroetanu i N202. Acta.Cryst. (14) str. 1100-01 .
- FA Cotton, G. Wilkinson, CA Murillo, M. Bochmann; Advanced Inorganic Chemistry, 6th ed. Wiley-Interscience, Nowy Jork, 1999.
- Fischer G i Becknell D; Analny. Chem. , 44,863,1972
- Kieselbach, Ind. Inż. Chem., Anal. Ed., 16 , 766, 1944
- Pharmacorama; Podtlenek azotu
- Syntaza tlenku azotu jest cytochromem P-450 typu h… [Biochemistry. 1992] - Wynik PubMed
- Andrews, KL, Triggle, CR i in. NIE i układ naczyniowy: skąd się bierze i co robi? Heart Fail Rev 7, 423-45 (2002)
- Metabolizm tlenku azotu
- Giuliano, F., Rampin, O., Benoit, G. i Jardin, A. (1997). Farmakologia obwodowa erekcji . Postępy w urologii, 7 (1), 24-33.
- Tlenek azotu jako dwufunkcyjny regulator apoptozy
- Chemia nadtlenoazotynów
- Kontrastowy wpływ NO i nadtlenoazotynów na ekspresję HSP70 i apoptozę w ludzkich monocytach; Adrie C i in. Am J Physiol Celi Physiol 279: 452-460, 2000.
- Badania funkcjonalne peroksydazy glutationowej kodowanej przez HIV-1
- Dawcy NO i NO
- Azydek sodu jako pośredni dawca tlenku azotu: badania izolowanych segmentów aorty szczura; Ukr Biokhim Zh. Lipiec-sierpień 2005; 77 (4): 120-3
- Kliniczne zastosowanie tlenku azotu; Olson G.
- 1998 Nagroda Nobla w dziedzinie medycyny za odkrycie roli NO w regulacji układu krążenia
- Rozwiązanie: tlenek azotu (NO) , Czytanie notatki Louis-Marie Houdebine, pseudo-sciences.org, 31 grudnia 2014
Zobacz też
- Zespół ostrej niewydolności oddechowej
- Neurotransmitter
- EDRF: Nazwa czynnika relaksującego pochodzącego ze śródbłonka, nadana tej samej cząsteczce, zanim poznamy jej wzór chemiczny
- Przekazywanie sygnału
- Pomiar tlenków azotu
Link zewnętrzny
- Tlenek azotu: Biology and Chemistry , czasopismo naukowe








