Aceton
| Aceton | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
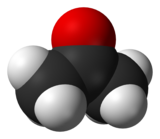 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Półrozwinięta formuła i trójwymiarowa reprezentacja acetonu. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nazwa IUPAC | propan-2-on | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonimy |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O ECHA | 100 000 602 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O WE | 200-662-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 180 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 3326 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| UŚMIECH |
CC (= O) C , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C3H6O / c1-3 (2) 4 / h1-2H3 InChIKey: CSCPPACGZOOCGX-UHFFFAOYAF Std. InChI: InChI = 1S / C3H6O / c1-3 (2) 4 / h1-2H3 Std. InChIKey: CSCPPACGZOOCGX-UHFFFAOYSA-N |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd | bezbarwna ciecz o charakterystycznym zapachu. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości chemiczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formuła |
C 3 H 6 O [Izomery] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa cząsteczkowa | 58,0791 ± 0,0031 g / mol C 62,04%, H 10,41%, O 27,55%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| pKa | 20 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moment dipolarny | 2,88 ± 0,03 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Średnica cząsteczkowa | 0,482 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości fizyczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuzja | -94,6 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° wrzenia | 56,05 ° C ( 760 mm Hg ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozpuszczalność | mieszalny z wodą, etanolem , eterem dietylowym , estrami , benzenem , dimetyloformamidem , chloroformem , większością olejów | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametr rozpuszczalności δ |
20,3 MPa 1/2 ( 25 °C ); 22,1 J 1/2 · cm -3/2 ( 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa objętościowa |
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura samozapłonu | 465 °C lub 538 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura zapłonu |
-18 °C (kubek zamknięty), -9,4 °C (kubek otwarty) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Granice wybuchowości w powietrzu | 2,15 - 13 % obj. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
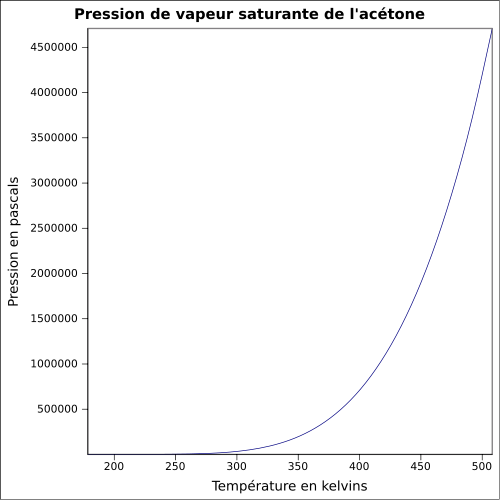
| Prężność pary nasyconej |
228 mbar przy 20 °C 360 mbar przy 30 °C 814 mbar przy 50 °C 1385 mbar przy 65 °C równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lepkość dynamiczna | 0,32 cP ( 20 °C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punkt krytyczny | 235 °C , 46,4 atm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Potrójny punkt | -94,5 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prędkość dźwięku | 1203 m · s -1 do 20 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochemia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 płynny, 1 bar | 200,4 J · mol -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 stały | -249,4 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gaz | -218,5 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 ciecz | -41 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ FUS H ° | 5,7 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ VAP H ° | 31,3 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
125,5 J · mol -1 · K -1 (ciecz) 75 J · mol -1 · K -1 (gaz) równanie:
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SZT | 1 789,9 kJ · mol -1 (ciecz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości elektroniczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 Re jonizacja energia | 9,703 ± 0,006 eV (gaz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stała dielektryczna | 21.01 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalografia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klasa kryształowa lub grupa kosmiczna | Pbcm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametry siatki |
a = 6,393 Å b = 5,342 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tom | 366,55 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości optyczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Współczynnik załamania światła | 1.3560 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Środki ostrożności | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Niebezpieczeństwo H225, H319, H336, EUH066, P210, P233, P261, P280, P303 + P361 + P353, P370 + P378, H225 : Wysoce łatwopalna ciecz i pary H319 : Działa drażniąco na oczy H336 : Może wywoływać senność lub zawroty głowy EUH066 : Powtarzające się narażenie może powodować wysuszanie lub pękanie skóry P210 : Przechowywać z dala od źródeł ciepła / iskier / otwartego ognia / gorących powierzchni. - Zakaz palenia. P233 : Przechowywać pojemnik szczelnie zamknięty. P261 : Unikać wdychania pyłu/dymu/gazu/mgły/par/rozpylonej cieczy. P280 : Stosować rękawice ochronne/odzież ochronną/ochronę oczu/ochronę twarzy. P303 + P361 + P353 : W przypadku kontaktu ze skórą (lub włosami): Natychmiast zdjąć całą zanieczyszczoną odzież. Spłucz skórę wodą/prysznicem. P370 + P378 : W przypadku pożaru: Użyć… do gaszenia. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  B2, D2B, B2 : Temperatura zapłonu cieczy palnej = -20 ° C zamknięty tygiel (metoda nie podana) D2B : Materiał toksyczny powodujący inne efekty toksyczne Podrażnienie oczu u zwierząt 1,0% ujawnienie zgodnie z wykazem składników |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 1 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
33 : wysoce łatwopalny materiał ciekły (temperatura zapłonu poniżej 21 ° C ) Numer UN : 1090 : ACETON Klasa: 3 Etykieta: 3 : Ciecze łatwopalne  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inhalacja | podrażnienie oskrzeli, problemy z oddychaniem, pijaństwo, zmętnienie | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oczy | zaczerwienienie, ból | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Przyjmowanie pokarmu | pijaństwo, obsesja | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoksykologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | > 5000 mg · kg -1 (doustnie), 20 g · kg -1 (skóra królika) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | -0,24 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Próg zapachu | niski: 3,6 ppm , 47,5 mg · m- 3 ; góra: 653 ppm , 1 613,9 mg · m -3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednostki SI i STP, chyba że zaznaczono inaczej. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Aceton (rzeczownik) jest chemia związek najprostszymi rodziny ketonów . O wzorze empirycznym C 3 H 6 O, jest izomerem propanalu . Jego oficjalna nazwa IUPAC to propanon, ale jest również znany pod nazwami keton dimetylowy i beta-ketopropan .
File Lander z Rosetta sondy przestrzeni wykrył to dziesięcio- atom związek o komety 67P / Tchourioumov-Guérassimenko , która świadczy o obecności tej cząsteczki w układzie słonecznym .
Właściwości fizykochemiczne
Aceton jest bezbarwną, palną cieczą o charakterystycznym raczej owocowym zapachu . Jego temperatura topnienia wynosi -94,6 °C, a temperatura wrzenia 56,05 °C . Ma ciężar właściwy 0,783 i 0,819 w temperaturze 0 °C . Jest związkiem bardzo dobrze rozpuszczalnym w wodzie (jest polarną cząsteczką o krótkim łańcuchu węglowym ), w etanolu i eterze . Aceton jest najprostszą pochodną serii ketonów alifatycznych, a obecność podwójnego wiązania węgiel-tlen nadaje mu największą reaktywność. Jest polarnym rozpuszczalnikiem aprotonowym .
Aceton tworzy hydrazon z fenylohydrazyną i oksym z hydroksyloaminą . Redukcja przez amalgamat z sodu przekształca go w alkoholu izopropylowym ; utlenianie kwasem chromowym daje tlenek węgla i kwas octowy . Reaguje z amoniakiem tworząc di- i triacetonoaminę (en) (TAA). Łączy się również bezpośrednio z cyjanowodorem, tworząc nitryl kwasu 2-hydroksy-2-metylomasłowego. Ta cyjanohydryna , która jest produktem pośrednim, jest przekształcana przez kwas siarkowy (H 2 SO 4) siarczanowany ester metakryloamidu, którego hydroliza daje wodorosiarczan amonu i kwas metakrylowy .
Pod wpływem działania różnych odczynników, takich jak wapno , kaustyczny potaż lub kwas solny , aceton przekształca się w produkty kondensacji , w tlenek mezytylu C 6 H 10 O, w foronie C 9 H 14 O, Itd.
Przekształca się w mezytylen C 9 H 12(symetryczny trimetylobenzen) przez destylację w obecności kwasu siarkowego. Aceton był stosowany do wytwarzania farbowania z indygo sztuczne. W obecności jodu , zasady i wody, daje jodoform .
Aceton jest również używany jako chłodziwo , ponieważ mieszanka z suchym lodem (CO 2ciało stałe) prowadzi do -78 °C .
Produkcja i synteza
Syntezę acetonem został opisany przez Jean Béguin 1610, przygotowanej przez pirolizę z octanem ołowiu .
Aceton, dawniej ekstrahowany z kwasu pirolignowego powstałego w wyniku pirolizy drewna , był później produktem ubocznym kwasu octowego .
W 1915 roku , Chaim Weizmann odkryto tani sposób otrzymania acetonu z skrobi , co umożliwiło wytwarzanie kordytu , jest wybuchowy .
W 2008 roku najszerzej stosowaną metodą produkcji acetonu był proces kumenu , podczas którego wytwarzano go (podobnie jak fenol ) z benzenu i propylenu . Globalna produkcja acetonu wynosi około 1,5 miliona ton rocznie.
posługiwać się
Aceton jest rozpuszczalnikiem szeroko stosowanym w przemyśle i laboratorium, ponieważ ma tę zaletę, że szczególnie szybko rozpuszcza liczne związki organiczne i jest mieszalny z wodą. Jest także związkiem będącym podstawą produkcji tworzyw sztucznych , leków i innych produktów przemysłu syntetycznego. Aceton jest używany w szczególności w przemyśle do produkcji bisfenolu A w reakcji z fenolem . Bisfenol A jest ważny składnik wielu polimerów , takich jak poliwęglan i poliuretan , jak i żywic epoksydowych . Aceton jest również używany na dużą skalę do transportu i przechowywania acetylenu : pojemnik z materiałem porowatym wypełnia się acetonem, w którym acetylen jest następnie rozpuszczany (jeden litr acetonu rozpuszcza około 250 l acetylenu).
Aceton jest również głównym składnikiem niektórych rozpuszczalników używanych do usuwania lakieru do paznokci . Jest również stosowany jako rozpuszczalnik do rozpuszczania kleju i włókien celulozowych . Nie zaleca się stosowania acetonu na włókna sztuczne (octan, trioctan i akryl). Aceton jest również używany do odtłuszczania przemysłowego.
Kąpiele acetonowe służą do przygotowania ciał podczas plastynacji .
Aspekt biologiczny i mikrobiologiczny
Aceton jest ciałem ketonowym , zwykle występującym w bardzo małych ilościach w moczu i krwi . Większe ilości można znaleźć po poszczeniu oraz u pacjentów z cukrzycą ( u których kontrola poziomu cukru we krwi jest słaba) z ciężkim niedoborem insuliny ; Jednym z objawów cukrzycowej kwasicy ketonowej jest owocowy zapach w wydychanym powietrzu spowodowany przez aceton .
Aceton występuje naturalnie w roślinach , drzewach , gazach wulkanicznych , pożarach lasów oraz jako produkt rozkładu tłuszczu zwierzęcego. Występuje w spalinach , tytoniu i na składowiskach odpadów . Działalność człowieka produkuje go więcej niż natura.
Jest to jeden z produktów uformowanych przez destylacji z drewna , cukier , celuloza , itd. , iz tego powodu jest zawsze obecny w duchu surowego drewna, którego dużą część można odzyskać przez destylację frakcyjną .
Skutki BHP
Kontakt z acetonem może powodować podrażnienie lub uszkodzenie skóry . Duże i długotrwałe narażenie może spowodować utratę przytomności .
Badania na zwierzętach laboratoryjnych wykazały uszkodzenie nerek , wątroby i nerwów , a także płodu przy długotrwałej ekspozycji na duże dawki acetonu. Samce również wykazywały zaburzenia rozrodu, a nawet niezdolność do pracy. Nie wiadomo, czy tego rodzaju efekty można zaobserwować u ludzi.
Nietoksyczne milimolowe dawki acetonu wykazują działanie przeciwdrgawkowe w zwierzęcych modelach padaczki. W Unii Europejskiej dopuszczalną wartość narażenia zawodowego (OELP) ustalono na 500 ppm ( 1210 mg · m- 3 ) .
Wdychanie acetonu może powodować podrażnienie oskrzeli, problemy z oddychaniem, a spożycie acetonu może powodować zatrucie i zmętnienie .
Toksykologia zawodowa
Źródło.
Aceton w wysokich stężeniach powoduje depresję ośrodkowego układu nerwowego i podrażnienie błon śluzowych. Powtarzające się narażenie skóry może wywołać kontaktowe zapalenie skóry. Ze względu na niebezpieczeństwo pożaru i wybuchu podczas przechowywania i obchodzenia się z acetonem należy podjąć środki zapobiegawcze i ochronne: dobór środków ochrony osobistej będzie dokonywany w zależności od warunków na stanowisku pracy, nie mogą one być źródłem elektryczności statycznej. Podczas wizyt wstępnych i okresowych badanie kliniczne będzie szukać oznak uszkodzenia neurologicznego, ocznego, skórnego lub przewlekłego układu oddechowego. Kobiety, które chcą zajść w ciążę, będą w jak najmniejszym stopniu narażone ze względu na czerwone flagi dotyczące płodności.
Uwagi i referencje
- ACETON , karta (y) bezpieczeństwa Międzynarodowego Programu Bezpieczeństwa Substancji Chemicznych , skonsultowana w dniu 9 maja 2009 r.
- (i) " ACETON " na substancjach niebezpiecznych Data Bank (dostęp 3 lutego 2010 ) .
- (w) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press/Taylor and Francis,17 czerwca 2008, 89 th ed. , 2736 s. ( ISBN 9781420066791 , prezentacja online ) , s. 9-50.
- (en) Icchak Marcus, Właściwości rozpuszczalników , tom. 4, Anglia, John Wiley & Sons,1999, 239 s. ( ISBN 0-471-98369-1 ).
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- Aceton , INRS, karta toksykologiczna FT3, 2008.
- (w) James E. Mark , Podręcznik właściwości fizycznych polimerów , Springer,2007, 2 II wyd. , 1076 s. ( ISBN 0-387-69002-6 , czytaj online ) , s. 294.
- (en) Robert H. Perry i Donald W. Green , Perry's Chemical Engineers' Handbook , Stany Zjednoczone, McGraw-Hill,1997, 7 th ed. , 2400 pkt. ( ISBN 0-07-049841-5 ) , s. 2-50.
- (w) William M. Haynes , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press/Taylor and Francis,1 st lipca 2010, 91 th ed. , 2610 s. ( ISBN 9781439820773 , prezentacja online ) , s. 14-40.
- (w) Carl L. Yaws , Handbook of Thermodynamic Diagrams , tom. 1, Huston, Teksas, Gulf Pub. Współ.,1996( ISBN 0-88415-857-8 ).
- (w) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18 czerwca 2002, 83 th ed. , 2664 s. ( ISBN 0849304830 , prezentacja online ) , s. 5-89.
- (w) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press/Taylor and Francis,17 czerwca 2008, 89 th ed. , 2736 s. ( ISBN 9781420066791 , prezentacja online ) , s. 10-205.
- „ Aceton ” , na stronie www.reciprocalnet.org (dostęp 12 grudnia 2009 ) .
- Karta charakterystyki dostarczona przez Sigma-Aldrich, konsultowana w dniu28 września 2019 r..
- „ aceton ” w bazie danych chemikaliów Reptox z CSST (Quebec organizacji odpowiedzialnej za bezpieczeństwo i higienę pracy), dostęp 25 kwietnia 2009.
- (in) " aceton " na hazmap.nlm.nih.gov (dostęp 14 listopada 2009 ) .
- „aceton” , na ESIS (konsultowane w10 lutego 2009).
- (w) Fred Goesmann Helmut Rosenbauer, Jan Hendrik Bredehöft Michel Hut, Pascale Ehrenfreund Thomas Gautier, Chaitanya Giri, Harald Krüger, Lena Roy, Alexandra J. MacDermott, Susan McKenna-Lawlor, Uwe J. Meierhenrich Guillero M. Muñis Raulin , Reinhard Roll, Andrew Steele, Harald Steininger, Robert Sternberg, Cyril Szopa, Wolfram Thiemann i Stephan Ulamec, „ Związki organiczne na komecie 67P / Churyumov-Gerasimenko ujawnione przez spektrometrię mas COSAC ” , Science , tom. 349 n O 6247,31 lipca 2015 r.( DOI 10.1126 / science.aab0689 , czytaj online ).
- Jean Béguin, przeł. Jean Lucas Du Roi, Les elemens de chymie, de maistre Iean Beguin almosnier du Roy , at Mathieu Le Maistre, rue sainct Iean de Laterran à l'Arbre sec,1620( przeczytaj online ).
- Likhodii i in. , 2003.
- Karta toksykologiczna INRS FT3 ,październik 2018.
Zobacz również
Linki zewnętrzne
- Międzynarodowa Karta Bezpieczeństwa , na cdc.gov .
- (en) Aceton , na stronie webbook.nist.gov .
- (en) Baza danych niebezpiecznych substancji chemicznych na ull.chemistry.uakron.edu .