Kwas rybonukleinowy
Kwas rybonukleinowy lub RNA (w języku angielskim, RNA do kwasu rybonukleinowego ) jest kwas nukleinowy obecny w praktycznie wszystkich istot żywych , a także w niektórych wirusów . RNA jest chemicznie bardzo zbliżone do DNA i jest również generalnie syntetyzowane w komórkach z matrycy DNA, której jest kopią. Komórki użyciu RNA w szczególności jako nośnik pośredni dla genów do syntezy tych białek są potrzebne. RNA może spełniać wiele funkcji, w szczególności interweniować w reakcjach chemicznych w metabolizmie komórki .
Chemicznie RNA jest liniowym polimerem składającym się z łańcucha nukleotydów . Każdy nukleotyd zawiera fosforan grupę , A cukier ( rybozę ) oraz zasadę azotową (lub nukleinowego zasada). Nukleotydy są połączone ze sobą wiązaniami fosfodiestrowymi . W RNA znajdują się cztery zasady nukleinowe: adenina , guanina , cytozyna i uracyl .
RNA ma wiele podobieństw do DNA , jednak z pewnymi istotnymi różnicami: ze strukturalnego punktu widzenia RNA zawiera reszty rybozy , gdzie DNA zawiera dezoksyrybozę , co sprawia, że RNA jest mniej stabilny chemicznie; ponadto tymina w DNA jest tam zastąpiona uracylem, który ma te same podstawowe właściwości parowania z adeniną. Funkcjonalnie RNA najczęściej występuje w komórkach w postaci jednoniciowej , czyli jednoniciowej, podczas gdy DNA występuje jako dwie komplementarne nici tworzące podwójną helisę . Wreszcie cząsteczki RNA obecne w komórkach są krótsze niż DNA genomu , ich wielkość waha się od kilkudziesięciu do kilku tysięcy nukleotydów, wobec kilku milionów do kilku miliardów nukleotydów dla kwasu dezoksyrybonukleinowego (DNA).
W komórce RNA jest produkowany przez transkrypcję z DNA (który znajduje się w jądrze eukariontów). RNA jest zatem kopią regionu jednej z nici DNA. Enzymy tworzące kopię DNA → RNA nazywane są polimerazami RNA . Tak wytworzone RNA mogą pełnić trzy główne typy funkcji: mogą być nośnikami informacji genetycznej jednego lub więcej genów kodujących białka (mówi się wtedy o informacyjnym RNA ), mogą przyjmować stabilną strukturę drugorzędową i trzeciorzędową oraz pełnić funkcje katalityczne ( na przykład rybosomalny RNA ), mogą ostatecznie służyć jako przewodnik lub matryca dla funkcji katalitycznych wykonywanych przez czynniki białkowe (co ma miejsce na przykład w przypadku mikroRNA ).
Struktura RNA
Rybonukleotydy
Struktura chemicznaRNA jest kwasem nukleinowym , to znaczy cząsteczką zbudowaną z łańcucha ( polimeru ) nukleotydów . Każda jednostka nukleotydowa RNA składa się z pentozy , rybozy , której atomy węgla są ponumerowane od 1 from do 5, zmiennej zasady azotowej lub zasady nukleinowej oraz grupy fosforanowej . Nukleozasada jest połączony przez atom o azotu do dwutlenku węgla jednym rybozy; a grupa fosforanowa nukleotydu jest związana z węglem 5'. Nukleotydy wiążą się ze sobą poprzez grupy fosforanowe, przy czym grupa fosforanowa jednego nukleotydu (związanego z węglem 5') łączy się poprzez wiązania fosfodiestrowe przy węglach 3' następnego nukleotydu.
Cztery główne zasady RNA i jedyne stosowane w transferowym RNA to adenina ( oznaczenie A), uracyl (oznaczenie U), cytozyna (oznaczenie C) i guanina (oznaczenie G). W porównaniu z DNA, tymina w DNA jest zastąpiona uracylem w RNA. Różnica między tymi dwiema zasadami polega na zastąpieniu grupy metylowej w pozycji 5 tyminy atomem wodoru w uracylu. Ta modyfikacja strukturalna nie zmienia właściwości parowania z adeniną.
Rybozymy , w szczególności rybosomalnego RNA i trna zawierać inne zmodyfikowane nukleotydy, ponad sto zostały zidentyfikowane.
StereochemiaStrukturalnie, obecność atomu tlenu w pozycji 'rybozy wpływami z 2 pokroju z tym furanozowej pierścienia rybozy. Ten pięcioatomowy heterocykl nie jest płaski, co prowadzi do powstania dwóch głównych konformerów cukru, zwanych C2 C-endo i C3′-endo. W RNA, który ma atom tlenu w pozycji 2', preferowana jest pozycja C3'-endo, która głęboko modyfikuje strukturę podwójnych helis zawierających nici RNA. Te dupleksy RNA tworzą helisę typu A, różną od tej, którą obserwuje się głównie w konwencjonalnym DNA, która jest helisą typu B, w której dezoksyryboza jest w konformacji C2′-endo.
Podwójna helisa RNA
Helisa typu A, którą przyjmuje RNA tworząc dupleks, ma zupełnie inne właściwości geometryczne niż helisa typu B. Po pierwsze, liczba par zasad na obrót helisy wynosi 11 zamiast 10 dla DNA w formie B. Płaszczyzna par zasad nie jest już prostopadła do osi spirali, ale tworzy z nią kąt około 75 °. Powoduje to przemieszczenie osi spirali, która nie przechodzi już przez środek sparowania podstaw, ale wewnątrz dużego rowka. Powoduje to wzrost średnicy helisy, która zmienia się z około 20 Å dla DNA w formie B do około 26 Å dla RNA w formie A. Wreszcie geometria dwóch rowków jest głęboko zaburzona: główny rowek staje się bardzo dostępny, podczas gdy mały rowek staje się bardzo głęboki, wąski i ściśnięty. Ma to wpływ na to, jak dwuniciowy RNA może oddziaływać z białkami, ponieważ wąska bruzda mniejsza stanowi barierę dla dostępności ligandów białkowych.
Struktura in vitro
Większość naturalnie występujących RNA występuje w komórce w postaci jednoniciowej (jednoniciowej), w przeciwieństwie do DNA, który ma postać sparowanej podwójnej nici. Te nici RNA krotnie głównie od siebie, tworząc struktury wewnątrzcząsteczkowej, które mogą być bardzo stabilne i bardzo zwarty. Podstawą tej struktury jest tworzenie wewnętrznych par, pomiędzy komplementarnymi zasadami ( A z U , G z C i czasami G z U ). Opis wewnętrznych par między zasadami RNA nazywa się strukturą drugorzędową . Ta drugorzędna struktura może być uzupełniona zdalnymi interakcjami, które następnie definiują strukturę trójwymiarową lub strukturę trzeciorzędową .
Tworzenie struktury RNA jest bardzo często zależy od otaczających fizykochemicznych warunkach , a w szczególności na obecność w roztworze , z dwuwartościowych kationów , takich jak magnez jonami Mg 2+ . Te kationy oddziałują z grupami fosforanowymi szkieletu i stabilizują strukturę, w szczególności osłaniając odpychanie elektrostatyczne między ujemnymi ładunkami tych fosforanów.
Struktura trzeciorzędowa RNA jest podstawą bogactwa swoich obowiązków, a zwłaszcza ich zdolność do katalizowania przez reakcje chemiczne ( rybozymy ).
Struktura drugorzędna
Wtórna struktura z RNA jest opis wszystkich wewnętrznych par w jednoniciowej cząsteczce. Ten zestaw parowania indukuje określoną topologię składającą się z regionów helikalnych (pręty) i regionów niesparowanych (pętle). Co więcej, struktura drugorzędowa obejmuje również opis tej topologii.
Tworzenie struktur drugorzędowych w jednoniciowym RNA wynika z istnienia regionów zawierających sekwencje palindromiczne , które mogą się parować, tworząc lokalnie strukturę podwójnej helisy. Na przykład, jeśli RNA zawiera następujące dwie sekwencje : --GUGCCACG ------ CGUGGCAC-- , tworzą one sekwencję palindromiczną, przy czym nukleotydy drugiego segmentu są komplementarne do nukleotydów pierwszego, po odwróceniu ich sensu czytania; te dwa segmenty mogą następnie sparować się w sposób antyrównoległy, tworząc lokalnie region dupleksowy. Obszar pomiędzy dwoma segmentami tworzy „pętlę” łączącą dwie sparowane pasma, przy czym to połączenie tworzy „pręt”. Jest to następnie określane jako „szpilka do włosów” lub struktura typu „ rod-loop” .
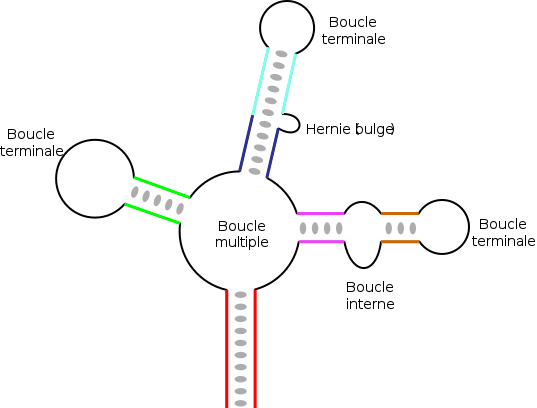
W RNA o większej długości mogą występować bardziej złożone struktury, które wynikają z parowania kilku komplementarnych lub palindromicznych regionów . W zależności od sposobu, w jaki te różne regiony są „zagnieżdżone”, uzyskuje się różne elementy topologiczne , z sparowanymi prętami lub regionami oraz różnego rodzaju pętlami:
- te pętle zaciskowe , znajdujące się na końcu drążka;
- te wewnętrzne pętle , która łączy dwa pręty;
- z wieloma pętlami , które łączą trzy lub więcej łodyg i tworzą strukturę punkty przyłączenia;
- przepuklinę (angielski zgrubienie ) lub boczne pętle , które znajdują się na jednej z dwóch nici helisy. Na ogół nie ma to wpływu na ciągłość spirali, a podstawy pozostają współosiowo ułożone po obu stronach przepukliny.
Nie zawsze istnieje jedna stabilna struktura dla danej sekwencji i zdarza się, że niektóre RNA mogą przyjąć kilka alternatywnych konformacji w zależności od wiązania liganda ( białko , mała cząsteczka itp.) lub warunków fizykochemicznych ( siła jonowa , pH ). Ogólnie rzecz biorąc, tworzenie lub fuzję struktury drugorzędowej RNA można śledzić za pomocą pomiarów spektroskopowych . Tak więc, na przykład, absorpcja zasad RNA w ultrafiolecie jest większa w stanie rozłożonym niż w stanie złożonym (zjawisko hiperchromowości ).
Struktura trzeciorzędowa
Pary niekanonicznePoza topologią pętli i helis składających się ze standardowych par zasad, RNA może przyjąć zwartą strukturę trójwymiarową lub strukturę trzeciorzędową , jak białko . W ramach tej struktury helisy kanoniczne są uzupełniane przez pary niekanoniczne, to znaczy różne od par klasycznych, Watsona - Cricka ( A = U i G ≡ C ) i chybotanie ( kołysanie , G = U ). Wiele różnych takich parowań zaobserwowano w trójwymiarowych strukturach RNA rozdzielonych za pomocą krystalografii rentgenowskiej lub magnetycznego rezonansu jądrowego . Są to, na przykład, Pary Hoogsteena i „sheared” Pary . Istnieją również interakcje zasada - ryboza , zwłaszcza z 2' hydroksylem , które mogą tworzyć wiązania wodorowe . Systematyczna nomenklatura wszystkich tych interakcji została zaproponowana przez Erica Westhofa i jego współpracowników. Zaobserwowano ponad 150 typów par, które zostały pogrupowane w dwanaście rodzin wielodzietnych. Te niekanoniczne pary zawsze obejmują wiązania wodorowe między zasadami, które są współpłaszczyznowe , jak w parach Watsona-Cricka.
Interakcje na odległośćPary kanoniczne lub niekanoniczne mogą występować pomiędzy odległymi obszarami struktury wtórnej, często ułożonymi w pętle, co umożliwia stabilizację zwartego fałdowania struktury.
Niektóre z tych długodystansowych interakcji niekanonicznych obejmują:
- z pseudoknots , struktury utworzone przez oddziaływanie pętli z regionu znajduje się na zewnątrz od trzonu, która ogranicza;
- potrójny nici , które pojawiają się, gdy jeden obszar nici jest włożona do większego rowka w obszarze śrubowej;
- przez Interakcje tetraloop nadawczo- : hyperstable interakcje między pętlami czterech nukleotydów (tétraboucles) i struktur dupleksowych lub quasi-dupleksie.
Różnice między DNA a RNA
Główne różnice między tymi dwiema cząsteczkami to:
- RNA dla cukru ryboza , gdzie DNA deoksyrybozę ;
- zasada uracylowa pełni w RNA funkcję pełnioną przez tyminę w DNA;
- RNA na ogół występuje w postaci jednoniciowej (jednoniciowej), z wyjątkiem kilku wirusów, takich jak reowirusy, gdzie występuje jako dwuniciowy RNA , podczas gdy DNA jest dwuniciowy (dwuniciowy) o strukturze podwójnej helisy;
- RNA jest krótkie: od kilkudziesięciu do kilku tysięcy nukleotydów dla komórkowego RNA (mRNA lub ustrukturyzowanego RNA), wobec kilku milionów do kilku miliardów (trzy miliardy u ludzi ) w DNA, które stanowi genom komórki.
Pierwsze trzy różnice powodują, że RNA jest znacznie mniej stabilne niż DNA:
- ryboza grupa ma grupę hydroksylową w pozycji 2”, który jest nieobecny w dezoksyrybozy do DNA . Ta funkcja 2'-OH ma wiele implikacji dla struktury RNA. Przede wszystkim na poziomie chemicznym ta funkcja alkoholu sprawia, że RNA jest wrażliwe na hydrolizę alkaliczną. Obecność dwóch tlenu cis w pozycjach 2' i 3' umożliwia cyklizację fosforanu w pozycjach 2' i 3', która następuje bardzo szybko, gdy zasada odrywa proton od 2'-OH. Ta cyklizacja nukleotydu powoduje odcięcie łańcucha rybozo-fosforanowego i uwalnianie cyklicznych końców fosforanowych 5'-OH i 2', 3' ;

- Produkcja uracylu jest mniej kosztowna energetycznie dla organizmów żywych niż tymina, ponieważ wymaga jednego etapu syntezy mniej niż metylacja przez syntazę tymidylanową . Obecność tyminy w DNA pozwala komórce wykryć samoistne uszkodzenie cytozyny wrażliwej na utlenianie . Deaminacja spontaniczne cytozyny w obecności tlenu, konwertuje go w uracyl. Obecność dezoksyurydyny w DNA jest nieprawidłowa, ponieważ komplementarnym dezoksyrybonukleotydem dezoksyadenozyny jest tymidyna . Dzięki temu rozróżnieniu między tyminą i uracylem za pomocą grupy metylowej podstawowy system naprawy przez wycięcie może wykryć i skorygować defekt. W RNA deaminacja cytozyny wytwarza uracyle i nie jest naprawiana. Ponieważ RNA ma znacznie krótszą żywotność niż DNA (rzędu minuty), ulega degradacji i recyklingowi;
- jeśli pojedyncza nić RNA jest uszkodzona, zmiana nie jest naprawiana i uszkodzenie jest nieodwracalne; z drugiej strony, jeśli jedna z dwóch nici DNA jest uszkodzona, komórka może wykorzystać informacje przenoszone przez nienaruszoną nić komplementarną do naprawy uszkodzenia .
Z ewolucyjnego punktu widzenia pewne elementy pozwalają sądzić, że RNA byłoby wcześniejsze od DNA jako nośnika informacji genetycznej, co wyjaśniałoby jego bardziej rozbudowane funkcje i jego uogólnienie. DNA pojawiłoby się później i zastąpiłoby RNA tylko do roli długoterminowego przechowywania, ze względu na jego większą stabilność.
Synteza RNA z DNA
Synteza cząsteczki RNA z DNA nazywana jest transkrypcją . Jest to złożony proces, który obejmuje enzym z rodziny polimeraz RNA oraz związane z nim białka. Różne etapy tej syntezy to inicjacja, elongacja i zakończenie. Proces syntezy RNA jest znacząco różny w organizmach prokariotycznych iw komórkach eukariotycznych . Wreszcie, po właściwej transkrypcji, RNA może przejść szereg modyfikacji potranskrypcyjnych w ramach procesu dojrzewania, podczas którego można zmodyfikować jego sekwencję i strukturę chemiczną (patrz poniżej).
Inicjacja
Rozpoczęcie transkrypcji RNA przez polimerazę RNA odbywa się na poziomie określonej sekwencji DNA, zwanej promotorem . Ten promotor zawiera jeden lub więcej konserwatywnych elementów sekwencji, do których na ogół są przyłączone specyficzne białka, czynniki transkrypcyjne . Tuż przed miejscem inicjacji transkrypcji, proksymalny element jest na ogół bogaty w nukleotydy T i A i dlatego jest nazywany skrzynką TATA u eukariotów lub skrzynką Pribnowa u bakterii. Czynniki transkrypcyjne sprzyjają rekrutacji polimerazy RNA do promotora i otwarciu dupleksu DNA. Następnie z otwartego DNA tworzy się tzw. bańka transkrypcyjna , której jedna z nici (matryca) jest zhybrydyzowana z syntetyzowanym RNA.
Wydłużenie
Po przymocowaniu polimerazy RNA do promotora i utworzeniu pęcherzyka transkrypcyjnego syntetyzuje ona pierwsze nukleotydy w sposób statyczny bez opuszczania sekwencji promotora. Czynniki transkrypcyjne odrywają się i polimeraza RNA staje się procesywna. Następnie dokonuje transkrypcji RNA w kierunku od 5 do 3 , używając jednej z dwóch nici DNA jako matrycy i trifosforanów rybonukleotydów ( ATP , GTP , CTP i UTP ) jako prekursorów.
In vivo w Escherichia coli szybkość wydłużania polimerazy RNA wynosi około 50 do 90 nukleotydów na sekundę.
Zakończenie
Terminacja transkrypcji RNA przebiega według zupełnie innych mechanizmów u bakterii i eukariontów .
U bakterii, główny mechanizm terminacji obejmuje szczególną strukturę RNA, terminator , składający się ze stabilnego pnia-pętli, po którym następuje seria reszt urydyny (U) . Kiedy polimeraza RNA syntetyzuje tę sekwencję, fałdowanie pręcika RNA powoduje zatrzymanie polimerazy. RNA, które nie jest już sparowane z matrycowym DNA, chyba że przez serię słabych par AU, odłącza się bez interwencji innych czynników białkowych. Terminacji można również dokonać poprzez interwencję określonego czynnika białkowego, czynnika Rho.
U eukariontów terminacja transkrypcji przez polimerazę RNA II jest sprzężona z poliadenylacją . Dwa kompleksy białkowe, CPSF (en) i CStF (en) rozpoznają sygnały poliadenylacji (5′-AAUAAA-3′) i rozszczepiania RNA. Rozszczepiają RNA, indukują odłączenie polimerazy DNA i rekrutują polimerazę poli-A, która dodaje ogon poli (A) (patrz poniżej).
Dojrzewanie
Obróbka RNA obejmuje zestaw modyfikacji potranskrypcyjnych obserwowanych głównie u eukariontów i odgrywa ważną rolę w losie dojrzałego RNA. Główne modyfikacje to dodanie czapeczki 5', poliadenylacji 3', splicing , wprowadzenie modyfikacji chemicznych na poziomie zasady lub rybozy i wreszcie edycja .
CzapkaNakrętka lub 5'-cap w języku angielskim jest zmodyfikowany nukleotyd , który jest dodawany do "końca 5 z RNA w eukariotycznych komórkach . Składa się z pozostałości z guanozyną zmetylować połączonych trifosforanu wiązanie 5'-5”od pierwszego nukleotydu transkrypcji przez polimerazę RNA . Modyfikacja ta jest wprowadzana do jądra komórki poprzez kolejne działanie kilku enzymów: polinukleotydu 5'-fosfatazy , guanylotransferazy RNA , metylotransferaz .
Kapturek odgrywa kilka ról: zwiększa stabilność RNA, chroniąc go przed degradacją przez 5′-3′ egzonukleazy, a także umożliwia rekrutację czynników inicjacji translacji niezbędnych do wiązania rybosomu z RNA. Kapturek jest zatem niezbędny do translacji większości mRNA.
PoliadenylacjaPoliadenylacji jest dodanie przedłużenie „koniec RNA składa się wyłącznie z 3 rybonukleotydów typu adenozyny (A). Z tego powodu rozszerzenie nazywa się poli tail (A) . Chociaż składa się ze standardowych nukleotydów, ten ogon poli (A) jest dodawany po transkrypcji przez specyficzny enzym zwany polimerazą poli (A) i nie jest kodowany w genomowym DNA . Ogon poli (A) znajduje się głównie na końcu informacyjnego RNA . U eukariontów poliadenylacja mRNA jest niezbędna do ich translacji przez rybosom i uczestniczy w ich stabilizacji. Ogon poli(A) jest w szczególności rozpoznawany przez PABP ( białko wiążące poli(A) , „ białko wiążące poli(A) ”).
Przeciwnie, w bakteriach iw niektórych mitochondriach poliadenylacja RNA jest sygnałem degradacji.
ŁączenieForniru jest modyfikacja post-transkrypcyjnym , który obejmuje usunięcie intronów i nici z egzonów w mRNA i w niektórych strukturze RNA, takich jak tRNA. Znalezione w organizmach eukariotycznych introny są segmentami RNA, które są kodowane w genomie i transkrybowane do prekursorowego RNA, ale które są usuwane z produktu końcowego. W większości przypadków proces ten obejmuje specyficzną, złożoną maszynerię zwaną spliceosomem . Splicing zachodzi w jądrze komórek eukariotycznych, przed eksportem dojrzałego RNA do cytoplazmy.
Zmodyfikowane nukleotydyNiektóre RNA po transkrypcji przez polimerazę RNA ulegają chemicznym modyfikacjom pod wpływem określonych enzymów . Kluczowe RNA podlegające zmianom to transferowe RNA i rybosomalne RNA . Można również uznać, że metylacje zaangażowane w syntezę czapeczki są modyfikacjami poszczególnych nukleotydów . W ogólnym przypadku modyfikacje mogą dotyczyć zarówno podstawy, jak i rybozy . Główne napotkane modyfikacje to:
- na rybozie: O- metylacje pozycji 2′-OH;
- na bazie :
- izomeryzacja urydyn, w wyniku której powstają pseudourydyny ,
- metylacje, albo na atomach węgla ( rybotymidyna ) albo na atomach azotu ( 7-metyloguanozyna ...),
- redukcji , który zmienia się urydyn dihydrouridines ,
- tiolacje,
- bardziej złożone modyfikacje ( prenylacja , treonylo-karbamoilacja itp.).
W transferowych RNA wprowadzenie zmodyfikowanych nukleotydów przyczynia się do zwiększenia stabilności cząsteczek.
RedagowanieEdycja RNA polega na modyfikacji sekwencji kwasu rybonukleinowego po transkrypcji przez polimerazę RNA. Pod koniec procesu edycji sekwencja RNA jest zatem inna niż sekwencja DNA. Wprowadzone zmiany mogą być modyfikacją zasady, podstawieniem zasady lub dodaniem jednej lub więcej zasad. Zmiany te są realizowane przez enzymy, które działają na RNA, takie jak deaminazy cytydynowej , które przekształcają chemicznie pozostałości z cytydyną do urydyny .
Funkcja w komórce
W komórkach RNA spełniają cztery różne i uzupełniające się role:
- tymczasowe wsparcie dla informacji genetycznej : informacyjne RNA spełnia tę rolę, jest wykorzystywane przez komórkę do przekazywania informacji odpowiadającej danemu genowi poza jądro, a następnie do syntezy białek z tej informacji;
- Katalizator enzymatyczny : Podobnie jak białka , RNA mogą składać się w trzech wymiarach, tworząc złożone struktury. Struktury te pozwalają niektórym RNA zachowywać się jak enzymy , nazywa się to rybozymem . Rybosomu The rybonukleaza P a niektóre introny są rybozymy . Istnieją pośrednie argumenty wskazujące, że mechanizm splicingu informacyjnego RNA ( spliceosom ) jest również rybozymem, chociaż nie zostało to jeszcze formalnie wykazane;
- przewodnik dla enzymów : niektóre RNA są wykorzystywane jako kofaktory przez białka, aby umożliwić ich ukierunkowanie na określone sekwencje . Wśród nich są małe jąderkowe RNA (snoRNA), które kierują enzymami modyfikującymi rybosomalny RNA , telomerowy RNA, który jest kofaktorem telomerazy , enzymu tworzącego końce chromosomów, lub interferujących RNA ;
- regulatory ekspresji genów : pewne niekodujące RNA odgrywają rolę w tłumieniu ekspresji pewnych genów lub grup genów. Tak jest na przykład w przypadku antysensownych RNA, które łączą się z docelowym RNA i blokują jego translację przez rybosom.
Specjalna klasa RNA, transferowe RNA, znajduje się na styku wielu z tych funkcji, kierując aminokwasami podczas translacji .
Wreszcie genom niektórych wirusów składa się wyłącznie z RNA, a nie z DNA. Dotyczy to w szczególności wirusów grypy , AIDS , zapalenia wątroby typu C , polio i Ebola . W zależności od przypadku, replikacja tych wirusów może przejść przez pośredniczący DNA ( retrowirus ), ale może również odbywać się bezpośrednio z RNA na RNA.
RNA jest wszechstronny cząsteczka, która doprowadziła Walter Gilbert , współwynalazcą do sekwencjonowania z DNA , aby zaproponować 1986 założenie, że RNA będzie najstarszy wszystkich makrocząsteczek biologicznych. Ta teoria, znana jako hipoteza świata RNA („ hipoteza świata RNA ”), umożliwia przezwyciężenie paradoksu jaja i kurczaka, który pojawia się, gdy próbuje się dowiedzieć, które z białek ( katalizatory ), a które z DNA (genetyczne). informacje) pojawiły się jako pierwsze. W tym modelu RNA, zdolne do jednoczesnego łączenia obu typów funkcji, byłby uniwersalnym prekursorem.
Komunikator RNA
Informacja genetyczna zawarta w obrębie DNA nie jest wykorzystywany bezpośrednio do komórek do syntezy na białko . W tym celu wykorzystuje przejściowe kopie informacji genetycznej, które są informacyjnymi RNA lub mRNA. Każdy informacyjny RNA zawiera jeden, a czasem kilka cistronów , czyli instrukcje tworzenia pojedynczego białka. Odpowiada zatem kopii tylko jednego z genów genomu (mówi się wtedy o monocistronowym mRNA) lub czasami kilku ( policistronowy mRNA ).
Komunikator RNA zawiera kopię tylko jednej z dwóch nici DNA, tej kodującej, a nie sekwencji komplementarnej. W porównaniu do sekwencji w genie zawarte w DNA genomu, które z odpowiada mRNA może zawierać modyfikacje, w szczególności z powodu składania (patrz wyżej), który eliminuje regionów niekodujących . Komunikator RNA zsyntetyzowany w jądrze komórki jest eksportowany do cytoplazmy w celu translacji na białko. W przeciwieństwie do DNA, który jest odwieczną cząsteczką, obecną przez całe życie komórki, informacyjne RNA mają ograniczoną żywotność, od kilku minut do kilku godzin, po czym ulegają degradacji i recyklingowi.
Informacyjny RNA ma trzy odrębne regiony: nieulegający translacji region 5′ zwany 5′-UTR, położony powyżej cistronu lub cistronów, które niesie; region kodujący odpowiadający temu lub tym cistronom; i wreszcie region niepodlegający translacji 3 ′, zwany 3′-UTR. Posłańcze RNA są tłumaczone na białka przez rybosomy . Nieulegający translacji region 5 na ogół zawiera sygnały translacyjne umożliwiające rekrutację rybosomu na cistronie. Proces translacji obejmuje również transferowe RNA, które zaopatrują rybosom w aminokwasy niezbędne do biosyntezy białek . W rybosomie, poprzez ich antykodon , tRNA parują kolejno z trójkami zasad lub kodonami sekwencji mRNA. Gdy parowanie kodon-antykodon jest prawidłowe, rybosom dodaje aminokwas niesiony przez tRNA do syntetyzowanego białka. Korespondencja między kodonami i aminokwasami stanowi kod genetyczny .
Funkcja informacyjnego RNA jest wielorakie. Z jednej strony umożliwiają zachowanie oryginalnej matrycy DNA, która nie jest bezpośrednio wykorzystywana do translacji, komórka pracuje jedynie na kopii, jaką jest mRNA. Przede wszystkim istnienie informacyjnego RNA zapewnia komórce kluczowy mechanizm regulacji cyklu produkcji białek z genomu. Zapotrzebowanie komórek na określone białko może się różnić w zależności od środowiska, typu komórki, etapu rozwoju. Synteza białek musi zatem zostać aktywowana lub zatrzymana w zależności od warunków komórkowych. Regulacja transkrypcji DNA do mRNA spełnia tę potrzebę i jest kontrolowana przez specyficzne czynniki transkrypcyjne działające na promotory docelowych genów. Gdy ilość danego białka jest wystarczająca, transkrypcja mRNA zostaje zahamowana, ulega stopniowej degradacji i ustaje produkcja białka. Dlatego ważne jest, aby mRNA był cząsteczką przejściową, aby móc przeprowadzić tę niezbędną regulację.
Przenieś RNA
Trna lub tRNA są krótkie RNA o długości około 70 do 100 rybonukleotydu udział w usuwaniu aminokwasów do rybosomu podczas translacji .
Transferowe RNA mają charakterystyczną strukturę liścia koniczyny, składającą się z czterech sparowanych łodyg. Jednym z nich łodygi jest zakończony przez pętlę, która zawiera antykodon , w triplet nukleotydów , które pary z kodonem podczas translacji wystąpienia mRNA przez rybosom . Na drugim końcu tRNA niesie odpowiedni aminokwas dołączony wiązaniem estrowym na swoim końcu 3'-OH. Ta estryfikacja jest katalizowana przez specyficzne enzymy, syntetazy aminoacylo-tRNA . W trzech wymiarach struktura liścia koniczyny fałduje się w kształt litery „L”, z antykodonem na jednym końcu i estryfikowanym aminokwasem na drugim końcu.
Wszystkie żywe komórki zawierają zestaw różnych tRNA niosących różne aminokwasy i zdolnych do odczytywania różnych kodonów.
Transferowe RNA są czasami określane jako „adaptery” między sekwencją genetyczną a sekwencją białka . To Francis Crick zaproponował istnienie tych adapterów, jeszcze przed ich odkryciem w 1958 roku.
Katalityczne RNA lub rybozymy
Odkrycie RNA o pojemności katalizator został złożony w 1980, a zwłaszcza przez zespół Thomas Cech , który pracował w intronów z genu do rybosomalnego RNA z pierwotniaki orzęsków Tetrahymena oraz Sidney Altmana , która badał rybonukleazy P , The enzymu na dojrzewanie w tRNA . Cech i Altman otrzymali za to odkrycie Nagrodę Nobla w dziedzinie chemii w 1989 roku.
W obu przypadkach sam RNA jest zdolny do katalizowania specyficznego rozszczepienia (rozszczepiania) lub reakcji transestryfikacji przy braku białka . Te katalityczne RNA nazwano rybozymami, ponieważ są to enzymy składające się z kwasu rybonukleinowego. W przypadku intronu Tetrahymena jest to samoskładający się intron będący jego własnym substratem , podczas gdy rybonukleaza P jest enzymem działającym in trans na wielu substratach.
Od czasu tych pierwszych odkryć zidentyfikowano inne naturalne rybozymy:
- RNA z wiroidów lub wirusów satelitarnych (wirusoidów), które są zdolne do samodzielnego cięcia;
- dziś istnieją bardzo mocne argumenty, na podstawie uchwały jego struktury 3D, aby twierdzić, że rybosom , kompleks ribonucleoprotein odpowiedzialny za tłumaczenia z mRNA do białek , jest sam rybozym. Dwa aktywne miejsca rybosomu, centrum dekodujące na małej podjednostce i centrum peptydylotransferazy, które tworzy wiązania peptydowe , w rzeczywistości składają się wyłącznie z segmentów rybosomalnego RNA;
- spliceosomu , która katalizuje splicingu z cytoplazmy mRNA w komórkach eukariotycznych , jest prawdopodobnie również rybozymy;
- niektóre ryboprzełączniki , które są ustrukturyzowanymi regionami regulatorowymi niesionymi przez informacyjne RNA, wykazują aktywność cięcia katalitycznego w obecności liganda ;
- Wreszcie istnieją rybozymy syntetyczne, które wyizolowano metodami ewolucyjnymi in vitro , takimi jak technika SELEX . W ten sposób wyizolowano syntetyczne katalityczne RNA zdolne do katalizowania szerokiej gamy reakcji chemicznych i wiązania szerokiej gamy ligandów, co zinterpretowano jako argument na rzecz hipotezy świata RNA . Takie syntetyczne RNA nazywane są czasami aptamerami , ponieważ są „nadające się” do wykonania danego zadania.
Ogólnie rzecz biorąc, we wszystkich tych rybozymach to właśnie ich specyficzne fałdowanie umożliwia rozpoznanie ich substratu i katalizę, tak jak w przypadku enzymów białkowych.
Przewodniki RNA
Przewodnik RNA to RNA, które łączą się z enzymami białkowymi i służą do kierowania ich działaniem na komplementarne sekwencje RNA lub DNA . Kierujący RNA łączy się z kwasem nukleinowym substratu i pomaga ukierunkować aktywność enzymu. Zidentyfikowano kilka typów:
- snorna lub snoARN : w jąderku komórek eukariotycznych, zarówno bezpośrednie działanie enzymów modyfikujących rybosomalnego RNA, a zwłaszcza 2'-O-metylowania za snoARN C / D i przez pseudouridylations H / ACA snoRNAs. Mechanizm ten umożliwia komórce specyficzną modyfikację wielu pozycji rRNA, przy użyciu jednego enzymu wykorzystującego różne snoRNA jako przewodników. SnoRNA są często kodowane przez sekwencje intronowe ;
- że miRNA są również prowadzić RNA zaangażowane w procesie interferencji RNA : związany z białkiem kompleks zwany RISC ( RNA indukowanego tłumiących kompleks ), te małe RNA spowodować pogorszenie docelowego mRNA, które łączą się w pary, albo represję tłumaczeniem ;
- TERC ( komponent RNA telomerazy ), podjednostka RNA telomerazy : ten ustrukturyzowany RNA jest związany z odwrotną transkryptazą, która syntetyzuje telomery , końce chromosomów . Zawiera sekwencję, która służy jako substrat dla telomerazy do syntezy telomerowego DNA o sekwencji komplementarnej. Kieruje zatem aktywnością enzymu, ale służąc jako szablon, a nie tworząc parę z substratem;
- lincARN występuje u ssaków, duże cząsteczki RNA kodujące lecz międzygenowy transkrypcji jako mRNA przez polimerazę RNA II. Ich długość pozwala na przyjęcie złożonej, trójwymiarowej struktury. Struktury te umożliwiają ich oddziaływanie z różnymi kofaktorami transkrypcji, takimi jak hnRNP-K czy PRC2 (głównie inhibitorami transkrypcji). Kompleksy te są następnie kierowane przez lincRNA na sekwencjach regulatorowych genów w celu zahamowania ich ekspresji. Wiązanie lincRNA z DNA obejmuje parowanie zasad RNA z odpowiednimi zasadami DNA po niedopasowaniu podwójnej helisy DNA lub nawet tworzenie potrójnej helisy DNA-DNA-RNA.
Regulatory RNA
Niektóre RNA odgrywają rolę bezpośrednich regulatorów ekspresji genów. Dotyczy to w szczególności niekodujących RNA posiadających regiony komplementarne do komórkowych informacyjnego RNA, które mogą zatem łączyć się z nimi, tworząc lokalnie podwójną nić RNA. Te antysensowne RNA mogą pochodzić z tego samego locus genetycznego, co ich docelowy RNA, przez transkrypcję komplementarnej nici, która jest następnie określana jako cis- regulator RNA . Mogą również pochodzić z transkrypcji innego regionu genomu, są wówczas transregulacyjnymi RNA .
Parowanie regulatorowego RNA z docelowym informacyjnym RNA może wpływać na zdolność tego ostatniego do translacji przez rybosom lub na jego stabilność, co prowadzi do regulacji translacji genu (genów) niesionych przez RNA. . W bakteriach istnieje zatem wiele przykładów antysensownego cis – lub trans- regulacyjnego RNA, które blokują miejsce startu translacji. Na przykład, gen kodujący Porin OmpF reguluje antysensowny RNA o nazwie MicF.
U eukariontów występują również duże regulatorowe RNA, które biorą udział w epigenetycznych procesach regulacyjnych . Najbardziej znanym przykładem jest Xist RNA u ssaków. To dezaktywuje nie gen, ale cały chromosom. Xist obejmuje jeden z dwóch chromosomów X każdej komórki u osobników żeńskich, który w ten sposób staje się nieaktywny. W ten sposób aktywny jest tylko jeden z dwóch chromosomów pary XX, co umożliwia uzyskanie takiego samego poziomu ekspresji genów przenoszonych przez chromosom X, jak u osobników męskich, którzy mają tylko jeden. Inaktywacja X jest procesem losowym, który może prowadzić do ekspresji różnych fenotypów przez różne komórki u tej samej samicy. Tak jest na przykład w przypadku koloru sierści u kotów.
Zastosowania terapeutyczne i biotechnologiczne
RNA jest dziś wykorzystywany w wielu zastosowaniach w biologii molekularnej, w szczególności dzięki procesowi interferencji RNA , który polega na wprowadzaniu do komórek eukariotycznych krótkich fragmentów dwuniciowego RNA zwanych „ Małymi interferującymi RNA ”. Te małe interferujące RNA (pRNA) o długości około dwudziestu par zasad są wykorzystywane przez maszynerię komórkową zdolną do degradacji mRNA w określony sposób. Tylko mRNA zawierające sekwencję odpowiadającą sekwencji pRNAi ulegają degradacji, co umożliwia selektywne obniżenie ekspresji danego białka. To technologiczne podejście jest znacznie prostsze i szybsze niż zakładanie inaktywowanych linii myszy ( knock-out ) i nazywa się knock-down .
Przewiduje się próby wykorzystania tej techniki do celów terapeutycznych, na przykład poprzez celowanie w geny wirusowe w celu zwalczania infekcji lub onkogeny w przypadku nowotworów. Wymagają jednak stabilizacji małych interferujących RNA (pRNAi) , aby uniknąć ich degradacji przez rybonukleazy i skierować ich działanie na odpowiednie komórki.
Historyczny
Te kwasy nukleinowe odkryto w 1868 roku Friedrich Miescher . Miescher nazwał nową substancję „nukleiną”, ponieważ została znaleziona w jądrze komórkowym. Obecność kwasów nukleinowych w cytoplazmie drożdży stwierdzono w 1939 roku i ustalono ich rybonukleinowy charakter, w przeciwieństwie do chromosomów zawierających DNA z dezoksyrybozami.
Około 1940 roku belgijski biolog Jean Brachet badał molekuły dotychczas mało scharakteryzowane, które w tamtych czasach wciąż nazywano „kwasami tymonukleinowymi i zymonukleinowymi” (odpowiednio DNA i RNA). Odkrywa, że kwas tymonukleinowy jest składnikiem chromosomów i jest syntetyzowany podczas podziału komórek po zapłodnieniu . Podkreśla istnienie kwasów zymonukleinowych (RNA) we wszystkich typach komórek: w jądrze , jąderku i cytoplazmie wszystkich komórek (podczas gdy uważano, że cząsteczki te są charakterystyczne dla komórek roślinnych i niższych eukariontów, takich jak drożdże ). Wreszcie pokazuje, że kwasy te są szczególnie obfite w komórkach (szczególnie w ergastoplazmie ), które są bardzo aktywne pod względem syntezy białek . Powstały podstawowe podstawy biologii molekularnej . Był rok 1940. W okresie powojennym do Bracheta dołączył belgijski biolog molekularny Raymond Jeener, który aktywnie uczestniczył w badaniach nad rolą RNA w biosyntezie białek .
Pod koniec lat pięćdziesiątych Severo Ochoa zdołał zsyntetyzować cząsteczki RNA in vitro za pomocą specyficznego enzymu, fosforylazy polinukleotydowej, co umożliwiło badanie właściwości chemicznych i fizycznych RNA.
Rola RNA jako pośrednika „posłańca” pomiędzy informacją genetyczną zawartą w DNA a białkami została zaproponowana w 1960 roku przez Jacquesa Monoda i François Jacoba po dyskusji z Sydneyem Brennerem i Francisem Crickiem . Wykazanie istnienia informacyjnego RNA dokonał François Gros . Następnie rozszyfrowanie kodu genetycznego przeprowadził Marshall Nirenberg w pierwszej połowie lat 60. W tym celu wykorzystał syntetyczne RNA o znanej sekwencji nukleotydowej, której właściwości kodujące badał.
Rybosomy po raz pierwszy zaobserwował belgijski biolog Albert Claude na początku lat 40. Używając technik frakcjonowania subkomórkowego i mikroskopii elektronowej , odkrył „małe cząsteczki” o charakterze rybonukleoproteinowym, obecne we wszystkich typach komórek żywych. Nazwał je „mikrosomami”, później przemianowanymi na rybosomy.
Wtórna struktura z tRNA została założona przez Roberta Holley , który udało się oczyszczanie i analizowanie tRNA sekwencje właściwe dla alaniny w roku 1964. Był to duży postęp w zrozumieniu rozszyfrowanie przekazu genetycznego prowadzone przez nich. Messenger RNA. Trójwymiarowa struktura tRNA została rozwiązana w 1974 r. niezależnie przez zespoły Aarona Kluga i Alexandra Richa, pokazując po raz pierwszy złożoną strukturę RNA. Istnienie katalitycznych właściwości RNA zostało niezależnie stwierdzone przez Sidneya Altmana i Toma Cecha w 1982 r., z jednej strony na rybonukleazę P, az drugiej na samosplatających się intronach. Rozstrzygnięcie struktury poszczególnych podjednostek rybosomu w 2000 roku przez zespoły Toma Steitza , Ady Yonath i Venki Ramakrishnana , a następnie całego rybosomu przez zespół Harry Nollera w 2001 roku, stanowiło istotny postęp w zrozumieniu centralny mechanizm biologii, czyli translacja mRNA na białka. Ponadto pozwoliło wykazać m.in., że rybosom był również rybozymem.
W latach 70. Timothy Leary w swojej pracy „Polityka ekstazy” widział w RNA obietnicę przyszłej modyfikacji świadomości (prawdopodobnie poprzez nowe leki i/lub ćwiczenia duchowe), włączając w to składnik zwiększający zdolności uczenia się kogoś, kto zaangażuje się w takie doświadczenia.
Hipoteza świata RNA
RNA World hipotezą jest hipoteza, według której RNA jest prekursorem wszelkich biologicznych makrocząsteczek , w szczególności DNA i białka, które są dozwolone w abiotycznego środowisku (określone przez prebiotyk chemii, która jest częściowo hipotetyczny) l „wygląd pierwszego mieszka komórki, to znaczy tworzące przedział i zawierające podsystemy informacyjne i metaboliczne.
W kontekście badania początków życia hipoteza ta pozwala na wyjaśnienie pojawiania się różnych funkcji biologicznych poprzez tworzenie pewnych bloków biomolekularnych z prawdopodobnych prebiotycznych produktów pośrednich i cząsteczek opartych na węglu. W 2009 roku zespół Johna Sutherlanda wykazał , że prawdopodobne prekursory rybonukleotydów, aminokwasów i lipidów można uzyskać poprzez redukcyjną homologację cyjanowodoru i niektórych jego pochodnych. Każdy ze znanych podsystemów komórkowych można zatem wyjaśnić chemią węgla, z reakcjami katalizowanymi przez światło ultrafioletowe a priori, bardzo obecnymi przed pojawieniem się warstwy ozonowej , z siarkowodoru jako środka redukującego. Sam cykl fotoredukcyjny mógłby być przyspieszany przez miedź [Cu(I)-Cu(II)].
Uwagi i referencje
- (w) Rebecca K. Montange i Robert T. Batey , „ Struktura elementu regulatorowego mRNA ryboprzełącznika S-adenozylometioniny ” , Nature , tom. 441, n O 7097,29 czerwca 2006, s. 1172-1175 ( PMID 16810258 , czytaj online )
- H. Lodish , A. Berk , P. Matsudaira , CA Kaiser , M. Krieger , MP Scott , L. Zipursky i J. Darnell , Biologia molekularna komórki , Bruksela, de Boeck,2005, 3 e wyd. ( ISBN 978-2804148027 )
- (en) Wolfram Saenger , Zasady struktury kwasów nukleinowych , Springer,1984( ISBN 0-387-90762-9 )
- (w) January Barciszewski i Brian Frederick Carl Clark , biochemia i biotechnologia RNA , Springer,1999, 73–87 s. ( ISBN 0-7923-5862-7 , OCLC 52403776 )
- Modyfikacja i edycja Rna. Henri Grosjean, Rob Benne. ASM Press, 1998.
- Marie-Christine Maurel, Anne-Lise Haenni: Świat RNA: hipotezy, fakty i wyniki eksperymentów.
- (w) Pan Sudaralingam , „ Stereochemia kwasów nukleinowych i ich składniki. IV. Dozwolone i preferowane konformacje nukleozydów, nukleozydów mono-, di-, tri-, tetrafosforanów, kwasów nukleinowych i polinukleotydów ” , Biopolymers , tom. 7 N O 6,1969, s. 821-860 ( czytaj online )
- (w) R. Langridge i PJ Gomatos , „ Struktura RNA. RNA reowirusa i transferowy RNA mają podobne trójwymiarowe struktury, które różnią się od DNA. » , Nauka , tom. 141 n O 4,1963, s. 694-698 ( PMID 13928677 )
- (pl) HR Drew , RM Wing , T. Tanako , C Broka , S Tanaka , K Itakura i RE Dickerson , „ Struktura dodekameru B-DNA: konformacja i dynamika. » , proc. Natl. Acad. Nauka. USA , obj. 78, n o 4,kwiecień 1981, s. 2179-2183 ( PMID 6941276 , czytaj online )
- (w) Peter S. Klosterman , Sapan A. Shah i Thomas A. Steitz , „ Struktury krystaliczne dwóch kontrolnych kopii plazmidowych dupleksów RNA powiązane: 18-par zasad dupleksy przy rozdzielczości 1,20 A i 19 par zasad dupleksy przy 1,55 A . ” , Biochemia , tom. 38 N O 45,1999, s. 14784-14792 ( PMID 10555960 , DOI 10.1021/bi9912793 , czytaj online )
- (en) JM Rosenberg , NC Seeman , JJ Kim , FL Suddath , HB Nicholas i A. Rich , „ Double Helix w atomowej rozdzielczości. » , Przyroda , tom. 243 n O 5403,1973, s. 150-154 ( PMID 4706285 , przeczytaj online )
- (w) RO Day , NC Seeman , MJ Rosenberg i A. Rich , „ Krystaliczny fragment podwójnej helisy: Struktura dinukleozydu fosforanu Guanylilo-3', 5'-Cytydyna. » , proc. Natl. Acad. Nauka. USA , obj. 70, n o 3,Marzec 1973, s. 849-853 ( PMID 4514996 , przeczytaj online )
- (w) Alexander Rich i David R. Davies , „ Nowa dwuniciowa struktura helikalna: poliadenylowy kwas poliurydylowy i kwas ” , J. Am. Chem. Soc. , tom. 78 N O 141956, s. 3548-3549 ( DOI 10.1021/ja01595a086 , przeczytaj online )
- (w) OF Draper , „ Rozpoznawanie białka-RNA ” , Annu. Obrót silnika. Biochem. , tom. 64,1995, s. 593-620 ( PMID 7574494 , czytaj online )
- (w) SA Woodson , „ Jony metali i zwijanie RNA: bardzo naładowany temat z dynamiczną przyszłością ” , Curr. Opinia. Chem. Biol. , tom. 9 N O 2Kwiecień 2005, s. 104-9 ( PMID 15811793 , czytaj online )
- (w) P. Doty , H. Boedtker , JR Fresco , R. Haselkorn i M. Litt , „ Struktura drugorzędowa w kwasach rybonukleinowych ” , Proc. Natl. Acad. Nauka. USA , obj. 45, n o 4,1959, s. 482-499 ( PMID 16590404 )
- F. Dardel i F. Képès , Bioinformatics: genomics and post-genomics , Editions de l'École Polytechnique,2002, 153-180 s. ( ISBN 978-2730209274 )
- (w) AM Michelson , „ Hiperchromity i kwasy nukleinowe. » , Przyroda , tom. 182 n O 4648,1958, s. 1502-1503 ( PMID 13613306 )
- (w) K. Hoogsteen , „ Kryształ i struktura molekularna kompleksu entre-1 i 9-metylotyminy metyloadeniny z wiązaniami wodorowymi. » , Acta Cryst. , tom. 16,1963, s. 907-916 ( DOI 10.1107/S0365110X63002437 )
- (w) HA Heus i A. Pardi , „ Cechy strukturalne, które powodują niezwykłą stabilność spinek do włosów RNA zawierających pętle NRMA. » , Nauka , tom. 253 n O 5.0161991, s. 191-194 ( PMID 1712983 )
- (w) NB Leontis i E. Westhof , „ Pary zasad non-Watson-Crick i ich macierze związane z izosterycznością. ” , Kwasy nukleinowe Res. , tom. 30 N O 162002, s. 3497-3531 ( PMID 12177293 )
- (w) DW Staple i SE Butcher , „ Pseudoknots: Struktury RNA o różnych funkcjach. » , PloS Biol. , tom. 3 N O 6,2005, e213 ( PMID 15941360 , przeczytaj online )
- (w) Mr. Costa i F. Michel , „ Częste stosowanie modelu trzeciorzędowego Sami przez samoskładające się RNA ” , EMBO J. , tom. 14,1995, s. 1276-1285 ( PMID 7720718 , czytaj online )
- (w) PJ Gomatos i I. Tamm , „ Wtórna struktura RNA reowirusa ” , Proc. Natl. Acad. Nauka. USA , tom. 49 N O 5,1963, s. 707-714 ( PMID 16591092 )
- (w) R. Markham i JD Smith , „ Struktura kwasów rybonukleinowych 1. Cykliczne nukleotydy i wytwarzane przez rybonukleazę przez hydrolizę alkaliczną ” , Biochem. J. , tom. 52, n o 4,1952, s. 552-557 ( PMID 13018277 , czytaj online )
- Walter Gilbert, " The RNA World ", Naturę 319, 1986, p. 618
- Biochemia Harpera, Harold Harper, Harold
- (w) ST Smale i JT Kadonaga , „ Promotor rdzenia polimerazy II RNA ” , Ann. Obrót silnika. Biochem. , tom. 72,2003, s. 449-479 ( PMID 12651739 , czytaj online )
- (w) RP Lifton , L. Goldberg , RW Karp i DS Hogness , „ Organizacja genów histonowych u Drosophila melanogaster: implikacje funkcjonalne i ewolucyjne ” , Cold Spring Harb. Miły. Ilość Biol. , tom. 42,1978, s. 1047-1051 ( PMID 98262 , czytaj online )
- (w) D. Pribnow , „ Sekwencja nukleotydowa strony internetowej roku wiązania polimerazy RNA na wczesnym promotorze T7 ” , Proc. Natl. Acad. Nauka. USA , tom. 72,1975, s. 784-788 ( PMID 1093168 , czytaj online )
- (w) BA Hamkalo i OL Miller , „ elektronmikroskopia aktywności genetycznej ” , Annu. Obrót silnika. Biochem. , tom. 42,1973, s. 376-396 ( PMID 4581229 )
- (w) WR McClure i Y. Chow , „ Kinetyka i procesywność polimeraz kwasów nukleinowych ” , Methods Enzymol. , tom. 64,1980, s. 277-297 ( PMID 6990186 , czytaj online )
- (w) H. Bremer i PP Dennis, „Modulacja składu chemicznego i innych parametrów komórki przez tempo wzrostu” w Neidhardt FC, R Curtiss, III, JL Ingraham ECC Lin KB Low, B Magasanik WS Reznikoff, M Riley, M Schaechter i HE Umbarger, Escherichia coli i Salmonella typhimurium Cellular and Molecular Biology , Waszyngton, DC, ASM Press,1996( ISBN 0-914826-89-1 , czytaj online ) , s. 1553-1569
- (w) S. Adhya i Mr. Gottesman , „ Kontrola terminacji transkrypcji ” , Annu. Obrót silnika. Biochem. , tom. 47,1978, s. 967-996 ( PMID 354508 , przeczytaj online )
- (w) MS Ciampi , „ Zależne od Rho terminatory transkrypcji i oznaczanie ” , Microbiology , tom. 152,2006, s. 2515-2528 ( PMID 16946247 , przeczytaj online )
- (w) Mr. Edmonds , „ Historia sekwencji poli A: od formacji przez czynniki do funkcji ” , Prog. Kwas nukleinowy res. Mol. Biol. , tom. 71,2002, s. 285-389 ( PMID 12102557 , czytaj online )
- (en) AK Banerjee , " Cap 5'-końcowa struktura w eukariotycznych przekaźnikowych kwasach rybonukleinowych " , Microbiol. Rev , tom. 44 N O 21980, s. 175-205 ( PMID 6247631 , czytaj online )
- (w) Mr. Edmonds i R. Abrams , „ Biosynteza polinukleotydów: tworzenie sekwencji jednostek adenylanowych z trifosforanu adenozyny przez enzym z jądra grasicy ” , J. Biol. Chem. , tom. 235,1960, s. 1142-1149 ( PMID 13819354 , przeczytaj online )
- (w) Pan Dreyfus i P. Regnier , „ Ogon poli(A) mRNA: ochroniarz u eukariontów, bakterie w padlinożercy ” , Cell , tom. 111,2002, s. 611-613 ( PMID 12464173 , przeczytaj online )
- (w) JP Staley i C. Guthrie , „ Urządzenia mechaniczne spliceosomu: silniki, zegary, sprężyny i rzeczy ” , Cell , tom. 92,1998, s. 315-326 ( PMID 9476892 , przeczytaj online )
- (w) WE Cohn , „ Pseudourydyna, rybonukleozyd związany węgiel-węgiel w kwasach rybonukleinowych: izolacja, struktura i charakterystyka chemiczna ” , Journal of Biological Chemistry , tom. 235,1960, s. 1488-1498 ( PMID 13811056 , czytaj online )
- (w) JA Kowalak JJ Dalluge , JA McCloskey i KO Stetter , „ Rola modyfikacji potranskrypcyjnej w stabilizacji transferowego RNA z hipertermofilnego. ” , Biochemia , tom. 28,1994, s. 7869-7876 ( PMID 7516708 )
- (en) S. Valadkhan , A. Mohammadi , Y. Jaladat i S. Geisler , „ Bezbiałkowe małe jądrowe RNA katalizują dwuetapową reakcję splicingu. » , proc. Natl. Acad. Nauka. USA , tom. 106,2009, s. 11901-11906 ( PMID 19549866 )
- (w) S. Brenner , F. Jacob i M. Meselson , „ Niestabilny produkt pośredni przenoszący informacje z genów do rybosomów do syntezy białek. » , Przyroda , tom. 190,1961, s. 576-581
- (w) BN Ames i RG Martin , „ Biochemiczne aspekty genetyki: operon. » , Annu. Obrót silnika. Biochem. , tom. 33,1964, s. 235-258 ( PMID 14268834 )
- (w) C. Yanofsky , „ Ustalanie natury kodu genetycznego trypletów. ” , Komórka , tom. 128,2007, s. 815-818 ( PMID 17350564 )
- (w) Huijing Shi i Peter B. Moore , „ Struktura krystaliczna drożdżowego tRNA fenyloalaniny w rozdzielczości 1,93 Å: klasyczna struktura ponownie ” , RNA , tom. 6, n O 8, sierpień 2000, s. 1091-1105 ( PMID 10943889 , PMCID 1369984 , DOI 10.1017/S1355838200000364 , czytaj online )
- (w) MB Hoagland , ML Stephenson , JF Scott , HI Hecht i PC Zamecnik , „ Rozpuszczalny związek pośredni kwasu rybonukleinowego w syntezie białek ” , J. Biol. Chem. , tom. 231,1958, s. 241-257 ( PMID 13538965 )
- (w) RW Holley , J. Apgar , GA Everett , JT Madison , M. Marquisee , SH Merrill , JR Penswick i A. Zamira , " Struktura kwasu rybonukleinowego " , Science , vol. 147,1965, s. 1462-1465 ( PMID 14263761 )
- (i) JD Robertus JE Ladner JT Finch , D. Rhodes , RS Brown BF Clark A. Klug , „ Struktura drożdżowego tRNA fenyloalaniny o 3 rozmiar A. » , Przyroda , tom. 250,1974, s. 546-551 ( PMID 4602655 ), (en) SH Kim , FL Suddath , GJ Quigley , A. McPherson , JL Sussman , AH Wang , NC Seeman i A. Rich , „ Trójwymiarowa trzeciorzędowa struktura RNA transferowego fenyloalaniny drożdży. » , Nauka , tom. 250,1974, s. 546-551 ( PMID 4601792 )
- (w) Francis H. Crick , „ My protein Synteza ” , Symp. Soc. Eksp. Biol. , tom. 12,58, s. 138-163 ( PMID 13580867 , czytaj online )
- (i) K Kruger PJ Grabowski AJ Zaug J. Sands , DE Gottschling i TR Cech , „ Self-splicingu RNA: autoexcision i autocyclization rybosomalnego RNA interwencji sekwencji Tetrahymena. ” , Komórka , tom. 31,1982, s. 147-157 ( PMID 6297745 )
- (i) C Guerrier-Takada , K. Gardiner , T. Marsh , N. Tempo i S. Altmana , „ Ugrupowanie RNA rybonukleazy P jest podjednostka katalityczna enzymu. ” , Komórka , tom. 35,1983, s. 849-857 ( PMID 6197186 )
- (w) AC Forster i Davies , „ Charakterystyka samorozszczepiania wiroidowych i wirusoidowych RNA. " , Metody Enzymol. , tom. 181,1990, s. 583-607 ( PMID 2199768 )
- (w) TR Cech , „ Biologia strukturalna. Rybosom jest rybozymem. » , Nauka , tom. 289,2000, s. 878-879 ( PMID 10960319 )
- (w) I Barrick , KA Corbino , WC Winkler , A. Nahvi , Pan Mandal , J. Collins , Pan Lee , A. Roth , N. Sudarsan I. Jona , JK Wickiser i RR Breaker , „ Nowe motywy RNA proponują rozszerzenie zakresu ryboprzełączników w kontroli genetycznej bakterii. » , proc. Natl. Acad. Nauka. USA , tom. 101,2004, s. 6421-6426 ( PMID 15096624 )
-
(w) AD Ellington i JW Szostak , " selekcji in vitro cząsteczek RNA, które wiążą się specyficzne ligandy. » , Przyroda , tom. 346,1990, s. 818-822 ( PMID 1697402 )
(en) C. Tuerk i L. Gold , „ Systematyczna ewolucja ligandów przez wykładnicze wzbogacanie: ligandy RNA do polimerazy DNA bakteriofaga T4. » , Nauka , tom. 249,1990, s. 505-510 ( PMID 2200121 ) - (w) Z. Kiss-László , Y. Henry , JP Bachellerie , Mr. Caizergues Ferrer i T. Kiss , „ Site-specyficzna metylacja rybozy przedrybosomalnego RNA: nowa funkcja dla małych jąderkowych RNA. ” , Komórka , tom. 85,1996, s. 1077-1088 ( PMID 8674114 )
- (en) J. Liu , „ Nowe małe jąderkowe RNA kodowane przez intron. ” , Komórka , tom. 75,1993, s. 403-405 ( PMID 8221882 )
- (w) B. Sollner-Webb , „ Kontrola syntezy białek i degradacji mRNA przez mikroRNA. " , Curr. Opinia. Biol. , tom. 20,2008, s. 214-221 ( PMID 18329869 )
- (w) D. Shippen-Lentz i EH Blackburn , „ Funkcjonalne dowody na matrycę RNA w telomerazie. » , Nauka , tom. 247,1990, s. 546-552 ( PMID 1689074 )
- (w) Pan Huarte , T. Jacks i JL Rinn , „ Duży międzygenowy niekodujący RNA indukowany przez p53 pośredniczy w globalnej represji genów w odpowiedzi p53 ” , Cell , tom. 142,2010, s. 409-419 ( PMID 20673990 )
- (w) EG Wagner i RW Simons , „ Kontrola antysensownego RNA w bakteriach, fagach i plazmidach. » , Annu. Obrót silnika. Mikrobiol. , tom. 48,1994, s. 713-742 ( PMID 3685996 )
- (en) E. Heard , „ Ostatnie postępy w dezaktywacji chromosomu X. " , Curr. Opinia. Biol. , tom. 16,2004, s. 247-255 ( PMID 15145348 )
- (w) A. Fire , S. Xu , Mr. Montgomery , S. Kostas S. Driver i C. Mello , „ Potężna i specyficzna interferencja genetyczna przez dwuniciowy RNA w Caenorhabditis elegans . » , Przyroda , tom. 391, 1998, s. 806-811
- Claude Hélène , “ Obietnice terapeutycznego RNA = Genetyczna interferencja przez RNA. », Le Concours Medical , tom. 124,2002, s. 2550-2552
- (w) R Dahm , „ Friedrich Miescher i odkrycie DNA ” , Dev. Biol. , tom. 278 n O 22005, s. 274–88 ( PMID 15680349 , DOI 10.1016 / j.ydbio.2004.11.028 )
- (w) T. Caspersson i J. Schultz , „ Pentose nukleotydy w cytoplazmie rosnących tkanek ” , Nature , tom. 143,1939, s. 602-3 ( DOI 10.1038 / 143602c0 )
- https://www.ulb.ac.be/ibmm/histoire.html
- (w) F. Jacob i J. Monod , „ Genetyczne mechanizmy regulacyjne w syntezie białek. ” , Journal of Molecular Biology , tom. 3,1961, s. 318-356 ( PMID 13718526 )
- François Jacob , Posąg wewnętrzny , Gallimard, coll. "Folio" ( N O 2156)1990, 438 s. ( ISBN 978-2-070-38246-0 i 2-070-38246-X , informacja BNF n O FRBNF35085459 )
- (w) F. Gros , H. Hiatt , W. Gilbert , CG Kurland , RW Risebrough i JD Watson , „ Niestabilny kwas rybonukleinowy ujawniony przez znakowanie impulsowe Escherichia coli ” , Nature , tom. 190, 1961, s. 581-585 ( PMID 13708983 )
- (w) A. Claude , „ Konstytucja protoplazmy ” , Science , tom. 97, n o 2.5251943, s. 451–456 ( PMID 17789864 , DOI 10.1126 / nauka.97.2525.451 )
- (w) N. Ban , P. Nissen J. Hansen , PB Moore , TA Steitz , „ Pełna struktura atomowa podjednostki rybosomalnej szeroka przy rozdzielczości 2,4 A. » , Nauka , tom. 289, 2000, s. 905-920 ( PMID 10937989 )
- (w) F. Schluenzen , A. Tocilj R. Zarivach , J. Harms , Pan Gluehmann , D. Janell , A. Bashan , H. Bartels , I. Agmon , F. Franceschi i A. Yonath , " Struktura funkcjonalnie aktywowano małą podjednostkę rybosomalną w rozdzielczości 3,3 angstremów. ” , Komórka , tom. 102, 2000, s. 615-623 ( PMID 11007480 )
- (w) OF Brodersen , „ Struktura podjednostki rybosomalnej 30S. » , Przyroda , tom. 407,2000, s. 1143-1154 ( PMID 11014182 )
- (en) MM Jusupow , GZ Jusupowa , A. Baucom , K. Lieberman , TN Earnest , JH Cate i HF Noller , „ Struktura krystaliczna rybosomu przy rozdzielczości 5,5 A. » , Przyroda , tom. 292,2001, s. 883-896 ( PMID 11283358 )
- Polityka ekstazy, Timothy Leary, 1974, red. Fayard, Paryż, s. 115-120
- Bhavesh H. Patel, Claudia Percivalle, Dougal J. Ritson, Colm D. Duffy i John D. Sutherland (2015), Wspólne pochodzenie RNA, prekursorów białek i lipidów w protometabolizmie cyjanosiarczkowym ; Chemia przyrody ( podsumowanie )
Zobacz również
Powiązane artykuły
- Lista typów RNA
- Komunikatorowy kwas rybonukleinowy
- Rybosom
- Rybozym
- Dwuniciowy RNA
- mikroRNA
- Interferujący RNA
- Lista skrótów z biologii komórkowej i molekularnej
- transkrybowana nić
- sekwencja RNA
- Lista kwasów
Linki zewnętrzne
- Świat RNA w Fritz Lipman Institute Zbiór linków na temat „świata RNA” (struktury, sekwencje, narzędzia, publikacje)
