Ostra białaczka szpikowa
Ostra białaczka szpikowa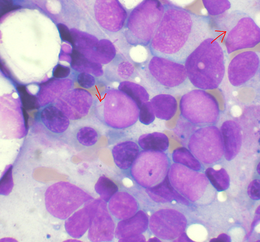 Ostra białaczka szpikowa, strzałki wskazują pałeczki Auera.
Ostra białaczka szpikowa, strzałki wskazują pałeczki Auera.
| Specjalność | Onkologia i hematologia |
|---|
| ICD - 10 | C92.0 |
|---|---|
| CIM - 9 | 205,0 |
| ICD-O | M 9861/3 |
| OMIM | 601626 |
| ChorobyDB | 203 |
| MedlinePlus | 000542 |
| eMedycyna | 197802 |
| eMedycyna | średni / 34 |
| Siatka | D015470 |
| Objawy | infekcje, krwawienie |
| Komplikacje | reakcja przeszczep przeciwko gospodarzowi (GvH) |
| Przyczyny | promieniowanie, benzen |
| Diagnostyczny | morfologia, mielogram, cytogenetyka |
| Leczenie | chemioterapia nowotworowa, terapia celowana, allogeniczny przeszczep szpiku kostnego |
| Lek | Idarubicyna , mitoksantron , etopozyd , cyklofosfamid , daunorubicyna , hydrat tioguaninę ( d ) , gemtuzumab , dasatinib monohydrat ( d ) , énasidénib , vénétoclax , doksorubicyna , hydroksymocznik , cytarabina , ewerolimus , azacytydyna , metotreksat , deferazyroks , tretinoina , nivolumab , klofarabinę , decitabinę , midostauryna , busulfan , sorafenib , ruksolitynib i 6-tioguanina |
| Pacjent z Wielkiej Brytanii | Ostra białaczka szpikowa pro |
Ostra białaczka szpikowa (AML), znany również jako białaczki ostrej białaczki jest rak typu hematologiczną złośliwość wpływu na krwiotwórcze komórki w szpiku kostnym . Komórki białaczki, zwane blastami , charakteryzują się niezdolnością do różnicowania się w dojrzałe komórki i niekontrolowaną proliferacją . Ta dysfunkcja szpiku kostnego uniemożliwia normalne wytwarzanie krwinek i powoduje różne objawy kliniczne, czasem bardzo poważne ( infekcje , krwotoki itp.). AML klasycznie występuje u osób dorosłych po 40. roku życia, w szczególności u osób starszych, nawet jeśli występują one również wśród nowotworów dziecięcych . Postępowanie zapewniają hematolodzy , głównie w szpitalach . Diagnoza wykorzystuje biologię molekularną do identyfikacji w szczególności mutacji genetycznych , co umożliwia określenie podtypu AML. Te elementy diagnostyczne są następnie brane pod uwagę w celu ustalenia rokowania choroby wraz z innymi elementami, takimi jak wiek lub odpowiedź na leczenie. Połączenie intensywnej chemioterapii i allogenicznego przeszczepu szpiku zapewnia całkowitą i trwałą remisję lub nawet wyleczenie u około 20-40% pacjentów.
Pole zainteresowań badań medycznych , w latach 2000 i 2010 dokonano znacznego postępu . Pojawienie się nowych, wysokowydajnych technik w hematologii komórkowej, biologii molekularnej i cytogenetyce zapewniło dostęp do lepszego zrozumienia mechanizmów zaangażowanych w rozwój AML. Identyfikacja nowych celów terapeutycznych umożliwia oferowanie terapii celowanych jako alternatywy dla chemioterapii cytotoksycznej. Tak więc w przypadku konkretnego podtypu, ostrej białaczki promielocytowej , konwencjonalna chemioterapia nie jest już oferowana jako pierwsza linia leczenia.
Epidemiologia
Wpływ
AML może wystąpić w każdym wieku, ale najczęściej dotyka dorosłych po 50. roku życia. W ciągu dekady 2010 mediana wieku diagnozy wynosiła od 64 do 72 lat, w zależności od kraju i roku.
| Epidemiologia AML | ||||
| Oprawa | Francja | Europa | Stany Zjednoczone | |
|---|---|---|---|---|
| Rozpowszechnienie (na 100 000 mieszkańców ) | 11 | |||
| Zapadalność (na 100 000 mieszk. ) | 2,3 (K) / 3,1 (M) (2018) | 2 - 3 | 3,5 (Ż) - 5,2 (M) (2012-2016) | |
| Stosunek płci (M/K) | 1,3 | 1.2 | 1,5 | |
| Odsetek hemopatii | 7,6% | |||
| Odsetek nowotworów | 0,9% | 1,2% | ||
Populacja pediatryczna (0-19 lat) jest w niewielkim stopniu dotknięta AML: zachorowalność jest niska, a w 2017 r. zachorowalność wyniosła 0,9%. Pacjenci ci są bardziej dotknięci innym podtypem białaczki: ostrą białaczką limfoblastyczną, która stanowi około 80% przypadków białaczki dziecięcej w porównaniu z 20% w przypadku AML.
Śmiertelność
Standaryzowany wskaźnik śmiertelności związany z AML szacuje się na 1,3 na 100 000 osób w 2017 roku przez Global Burden of Disease . W populacji pediatrycznej (0-19 lat) jest niższy i wynosi 0,4 na 100 000 osób.
Patogeneza, przyczyny, czynniki ryzyka
Patogeneza
Do układu krwiotwórczego , włączając AML strony, można ogólnie charakteryzują dwie cechy: do dojrzewania i proliferacji . W AML te dwie cechy ulegają zmianie: blasty utraciły zdolność różnicowania się w dojrzałe komórki krwi ( polimorfy , monocyty , płytki krwi , krwinki czerwone ), a podział komórek zachodzi bez kontroli z nadmierną proliferacją. To wadliwe dojrzewanie i proliferacja są powiązane z defektem cyklu komórkowego: ogólnie pewne geny odpowiedzialne za kontrolowanie tych funkcji przeszły mutacje, które zakłócają fizjologiczną kontrolę podziału komórek. Identyfikacja tych zmian służy jako podstawa do diagnozy, klasyfikacji i leczenia AML.
Przyczyny
Nowotwory i białaczki nie mają jednej znanej przyczyny, ale ich rozwój jest jednak związany z pewnymi czynnikami środowiskowymi i/lub nieprawidłowościami genetycznymi. Międzynarodowa Agencja Badań nad Rakiem , agencją WHO , odpowiedzialny jest w szczególności do oceny i klasyfikacji czynników fizycznych, chemicznych i biologicznych, zgodnie z ich rakotwórczego . Niektóre z nich szczególnie sprzyjają pojawieniu się białaczki, w tym AML. Ogólnie rzecz biorąc, każda ekspozycja, która może zmienić, zmodyfikować lub denaturować DNA komórek, jest potencjalnym czynnikiem ryzyka. Potrzebne są jednak dane epidemiologiczne i badania skutków komórkowych, aby ocenić, z rozsądnym stopniem pewności, ryzyko związane z takim narażeniem.
Promieniowanie jonizującePromieniowanie jonizujące są cząstki energetyczne wystarczającej do zerwania wiązania chemiczne między atomami, a tym samym zmienia się cząsteczek . Odkrycie promieniotwórczości i jej rosnące wykorzystanie w XX th century były szybko pokazać ryzyko ekspozycji na promieniowanie dla zdrowia. Rozwój radiobiologii umożliwił następnie ustalenie, że promieniowanie powoduje nieprawidłowości w DNA i zwiększa ryzyko rozwoju raka, a zwłaszcza białaczki. Marie Curie i Irène Joliot-Curie zmarły zatem na białaczkę prawdopodobnie wywołaną promieniowaniem z powodu ich pracy nad radioaktywnością .
Badanie INWORKS, opublikowane w Lancet Hematology w 2015 r., obejmujące kohortę nieco ponad 300 000 pracowników jądrowych w 3 krajach, wykazało, że ryzyko białaczki wzrosło nawet przy niskim narażeniu.
Środki chemiczneCzynniki chemiczne, w tym leki, aw szczególności chemioterapie cytotoksyczne, są identyfikowane jako źródła białaczki.
Narażenie na benzen jest znaną przyczyną rozwoju AML; w związku z tym został sklasyfikowany od 1979 r. jako czynnik rakotwórczy grupy 1 przez IARC (udowodniony czynnik rakotwórczy).
Glifosat klasyfikuje się jako prawdopodobnie rakotwórczy dla człowieka (grupa 2A), to nie ma w związku z AML z wysokim poziom wiarygodności ; chociaż dane są ograniczone, istnieje podejrzenie, że istnieje powiązanie.
Leki zidentyfikowane jako białaczkowe:
- że antracykliny ( doksorubicyna , daunorubicyna , itd. ) i pokrewne ( mitoksantronu ) są lekami przeciwnowotworowymi, znane jako białaczka;
- na środki alkilujące ( busulfan , etc. );
- antymetabolity (cytarabina);
- epidofilotoksyny: etopozyd .
- Leukemogenny środek chemiczny
-
Benzen
-
Doksorubicyna
-
Etopozyd
Początek ostrej białaczki szpikowej może następować po przekształceniu (lub zaostrzeniu ) innej choroby krwi , takiej jak zespół mielodysplastyczny lub zespół mieloproliferacyjny (przewlekła białaczka szpikowa itp .). Różne choroby wrodzone stanowią czynnik ryzyka ( trisomii 21 , zespół Klinefeltera , anemii Fanconiego , itd ).
Historia infekcji niektórymi wirusami lub bakteriami nie wydaje się być związana ze zwiększonym ryzykiem AML.
Objawy kliniczne
Gdy blasty nadmiernie się namnażają, atakują szpik kostny i/lub inne narządy ludzkiego ciała i zakłócają ich funkcję, powodując pojawienie się objawów klinicznych. Jednak obraz kliniczny na ogół nie jest bardzo specyficzny i nie można postawić diagnozy na podstawie samych objawów.
Niewydolność szpiku kostnego
Inwazja szpiku kostnego przez komórki białaczki zakłóca się krwinek, to znaczy fizjologiczny proces tworzenia się nowych komórek krwi. W szpiku zwykle wytwarzane są trzy typy komórek (lub linii): czerwone krwinki ( erytrocyty ), białe krwinki (zwłaszcza wielojądrzaste neutrofile ) i płytki krwi (trombocyty). Dysfunkcja szpiku kostnego może wahać się od cytopenii (pojedyncza dotknięta linia komórkowa) do anemii aplastycznej (całkowity niedobór krwinek ze wszystkich trzech linii). Towarzyszące objawy zależą od rodzaju cytopenii. Cytopenie można zdiagnozować przed wystąpieniem objawów klinicznych lub w rutynowej ocenie laboratoryjnej u osoby bezobjawowej.
Choroba czerwonej krwiIlościowy deficyt krwinek czerwonych objawia się całkowitym stężeniem hemoglobiny we krwi i nazywa się anemią . Tolerancja pacjenta na anemię jest na ogół powiązana z szybkością jej wystąpienia: w przypadku instalacji o niskim poziomie hałasu organizm dostosowuje się poprzez systemy kompensacyjne, objawy mogą być nieobecne. Szybkiemu wystąpieniu towarzyszyć będą natomiast następstwa kliniczne, w szczególności duszność , astenia , bladość.
Choroba białej liniiGłównym problemem jest spadek liczby neutrofili wielojądrzastych (PNN): komórki te należą do wrodzonego układu odpornościowego i tworzą pierwszą linię obrony przed infekcjami, głównie bakteryjnymi i grzybiczymi . W zależności od wielkości deficytu będziemy mówić o neutropenii lub agranulocytozie . Pacjent z neutropenią jest niezwykle podatny na infekcje . Wystąpienie gorączki w tym kontekście nazywa się gorączką neutropeniczną i stanowi nagły przypadek terapeutyczny najczęściej wymagający leczenia w środowisku szpitalnym z podaniem antybiotyku .
Obserwując neutropenię możemy mówić o białaczce „hiperleukocytowej” (to znaczy z nadmiarem białych krwinek): wysoki odsetek leukocytów w rzeczywistości odpowiada blastom krążącym we krwi przy jednoczesnym spadku ich liczby normalne komórki wielojądrzaste.
Zaangażowanie linii płytek krwiZmniejszenie liczby płytek krwi naraża Cię na ryzyko ciężkiego lub samoistnego krwawienia . Klinicznie objawy skórne, takie jak plamica , wybroczyny lub siniaki mogą odzwierciedlać nieskuteczną hemostazę.
Istotne zaburzenia krzepnięcia obserwuje się zwłaszcza w początkowej fazie ostrej białaczki promielocytowej . Spożycie płytek krwi i czynników krzepnięcia spowodowane rozsianym wykrzepianiem wewnątrznaczyniowym może pogorszyć małopłytkowość.
Zespół guza
Zespół guza wiąże się z rozprzestrzenianiem się blastów poza szpik kostny i akumulacją w narządach. Może to wynikać klinicznie przez:
- wzrost objętości niektórych narządów : śledziony , hepatomegalii ;
- ból stawu;
- uszkodzenie skóry (nocne pocenie się);
- uszkodzenie błony śluzowej, w tym przerost dziąseł (zwiększona objętość dziąseł);
- uszkodzenie nerwów i opon mózgowo-rdzeniowych w przypadku zajęcia ośrodkowego układu nerwowego , któremu mogą towarzyszyć objawy neurologiczne.
Gdy masa guza (tj. liczba blastów) jest bardzo duża, może rozpocząć się zespół rozpadu guza . Jest to związane z niszczeniem wybuchów, zarówno spontanicznych, jak i związanych z leczeniem. Zawartość wewnątrzkomórkowa jest następnie uwalniana do krwi, co powoduje zaburzenia stężenia jonów we krwi (potasu, fosforanów), widoczne na jonogramie. Może to prowadzić do hiperkaliemii , która jest szkodliwa dla rytmu serca lub wzrostu kwasu moczowego (hiperurykemia), co może prowadzić do uszkodzenia nerek poprzez tworzenie się kryształów moczanów. Leczenie zespołu lizy ma na celu przywrócenie prawidłowego jonogramu poprzez nawodnienie i podanie elektrolitów; Hiperurykemię można leczyć rasburykazą , enzymem rozkładającym kwas moczowy.
Zespół leukostazy obserwuje się w przypadku masywnego naciekania narządów przez komórki białaczkowe. Objawia się wysokim stężeniem blastów we krwi (blastoza), gorączką oraz objawami oddechowymi i/lub neurologicznymi. Zespół ten jest nagłym przypadkiem terapeutycznym, którego wynik może być śmiertelny z powodu niewydolności oddechowej .
Diagnostyczny
Badanie kliniczne pacjenta pozwala przede wszystkim wykryć oznaki złośliwej hemopatii. Diagnoza opiera się zasadniczo na rozszerzonej ocenie biologicznej obejmującej: morfologię krwi ( CBC ), biopsję mielogramu lub szpiku kostnego , immunofenotypowanie , kariotyp , cytogenetykę i sekwencjonowanie genów .
Badanie szpiku kostnego określa morfologiczny wygląd komórek i jest pierwszym krokiem w postawieniu diagnozy. Rozpoznanie ostrej białaczki stawia się w obecności ponad 20% niedojrzałych komórek, blastów. Badanie ekspresji różnych receptorów ( DC ) metodą immunofenotypowania umożliwia klasyfikację stadium i linii, do której należą komórki.
Kariotyp i badanie genomu pozwalają na identyfikację nieprawidłowości chromosomalnych (delecje, inwersje, translokacje); 50 do 60% AML ma nieprawidłowości kariotypu. Poszukiwane są również mutacje genetyczne . Analizy te mają decydujące znaczenie w ocenie rokowania i możliwości leczenia.
Przed opracowaniem technik fenotypowania i cytogenetyki diagnostyka AML opierała się głównie na morfologii komórki i opierała się na klasyfikacji francusko-amerykańsko-brytyjskiej (FAB). Nowe techniki badania DNA umożliwiły ustanowienie nowej klasyfikacji WHO, która zastąpiła FAB: jej kategoryzacja jest dokładniejsza i opiera się na anomaliach chromosomowych i/lub genetycznych.
Oprócz klasyfikacji możemy wyróżnić 3 rodzaje AML:
- AML de novo ;
- AML wtórna do zespołu mielodysplastycznego lub zespołu mieloproliferacyjnego ;
- AML indukowana przez cytotoksyczne i/lub promieniowanie.
Klasyfikacja
Ze względu na komórki dotknięte chorobą i zaangażowane mutacje, ostre białaczki szpikowe stanowią odmienny zestaw, który został poddany kategoryzacji. FAB (francusko-amerykańsko-brytyjska) jest najstarsza i została zastąpiona przez klasyfikację WHO opublikowaną w 2008 roku. Chociaż FAB jest przestarzały, nadal zwykle spełnia powiązane terminy diagnostyczne (LAM0, LAM3 itd .).
Światowa Organizacja ZdrowiaKlasyfikacja AML WHO jest obecnie stosowana w diagnostyce. Pierwotnie opublikowany w 2008 r., został zaktualizowany w 2016 r. i opublikowany w Blood (referencyjne czasopismo hematologiczne).
| Klasyfikacja WHO 2016 ostrej białaczki szpikowej i pokrewnych nowotworów | ||
| Nazwisko | Opis | ICD-O |
|---|---|---|
| AML z nawracającymi nieprawidłowościami cytogenetycznymi |
|
Wielokrotność |
| AML z nieprawidłowościami związanymi z mielodysplazjami | Obejmuje AML związane z MDS bez wyżej wymienionych nieprawidłowości molekularnych; są one na ogół związane z niekorzystnym rokowaniem.
|
M 9895/3 |
| AML . po leczeniu | Grupa obejmująca białaczki występujące po chemioterapii lub ekspozycji na promieniowanie. | M 9920/3 |
| LAM, bez dalszych wskazań | Grupa zawierająca podtypy, które nie pasują do innych kategorii.
|
|
| Mięsak szpikowy | ||
| Proliferacje szpiku związane z trisomią 21 |
|
M 9861/3 |
| Plazmacytoidalna białaczka dendrytyczna pochodzenia dendrytycznego | Dawniej znany jako białaczka / chłoniak z komórek NK
Nazywany również: Plasmocytoid Blast Dendrytic Cell Neoplasm (NCDPB) |
|
| Ostre białaczki o niejednoznacznym rodowodzie | ||
Klasyfikacja FAB (francusko-amerykańsko-brytyjska, 1976) jest starą klasyfikacją, obecnie porzuconą. Opiera się na morfologii i ilości komórek obserwowanych na mielogramie.
| Klasyfikacja FAB AML | ||
| CHŁOSTAĆ | Opis | Proporcja |
|---|---|---|
| LAM 0 | niezróżnicowany | 5% przypadków |
| LAM 1 | mieloblastyczny bez różnicowania | 15% przypadków |
| LAM 2 | mieloblastyczny z różnicowaniem | 25% przypadków |
| LAM 3 | promielocytowy | 10% przypadków |
| LAM 4 | mielomonocytowy | 20% przypadków |
| LAM 4Eo | mielomonocytowy z eozynofilią | 5% przypadków |
| LAM 5 | monoblastyczny (bez zróżnicowania: M5a, z zróżnicowaniem: M5b) | 10% przypadków |
| LAM 6 | erytroblastyczna lub erytroleukemia | 5% przypadków |
| LAM 7 | megakarioblastyczna | 5% przypadków |
W przeciwieństwie do analizy skupiającej się na badaniu zmutowanych genów, klasyfikacja ta nie ma wpływu na rokowanie lub leczenie, które ma zostać wdrożone.
Leczenie
Leczeniem leczniczym ostrej białaczki szpikowej jest chemioterapia intensywnie związana z allogenicznymi krwiotwórczymi komórkami macierzystymi (z wyjątkiem ostrej białaczki (" LA ") promielocytowej). Postępowanie zależy od wielu elementów związanych zarówno z chorym, jak i z białaczką. Szczególnie ważnymi czynnikami są wiek, stan ogólny, choroby współistniejące i życzenia pacjenta . Rodzaj ostrej białaczki, różne wykryte mutacje, a także reakcje kliniczne na poprzednie terapie określają opcje leczenia w całym postępowaniu. Decyzje dotyczące leczenia podejmowane są na zakończenie interdyscyplinarnych spotkań konsultacyjnych (RCP).
Klasyczne leczenie to następstwo cykli chemioterapii w kilku fazach: indukcja, konsolidacja, a następnie, jeśli pacjent się kwalifikuje, intensyfikacja terapii z allogenicznym przeszczepem szpiku. Promieniowanie nie jest standardem leczenia AML, ponieważ nie ma jedno miejsce choroby jak guza litego. Jest jednak stosowany w zapobieganiu lub leczeniu chorób nerwowo- oponowych, to znaczy, gdy komórki białaczki znajdują się w ośrodkowym układzie nerwowym ( mózgu , rdzeniu kręgowym ). Inne szczególne sytuacje mogą wymagać zastosowania radioterapii (lokalizacja jąder , mięsak szpikowy ).
Leczenie ostrej białaczki promielocytowej (APL) jest szczególnym przypadkiem: rola klasycznej chemioterapii cytotoksycznej jest mniej widoczna od czasu rozwoju połączenia kwaśnego kwasu all-trans retinowego ( ATRA ) i trójtlenku arsenu w celu uzyskania remisji powyżej 90% .
Zarządzanie białaczki i nowotworów jest związane z wieloma zasadniczego leczenia objawowego : zapobieganie i zarządzanie niekorzystnymi skutkami chemioterapii, wsparcie transfuzja złagodzić cytopenia , monitorowanie odżywczych , przesiewania dla objawów depresyjnych , leczeniu bólu i rozruch umieścić. Odpowiednią opiekę paliatywną Jeśli to konieczne.
Indukcja
Indukcja ma na celu wywołanie całkowitej remisji ( CR ) klinicznie i biologicznie za pomocą chemioterapii. Standardowo zalecany jest protokół 3+7 , oparty na cytarabinie i antracyklinie ( daunorubicyna lub idarubicyna ); to leczenie powoduje, że pacjent cierpi na głęboką anemię aplastyczną trwającą od trzech do czterech tygodni, podczas której ta ostatnia musi być ściśle monitorowana w specjalistycznym ośrodku hematologicznym, aby zapobiec ryzyku krwawienia i infekcji.
Jako alternatywę dla klasycznej indukcji można zastosować inne cząsteczki, takie jak decytabina .
Konsolidacja
Dalsze leczenie zależy w dużej mierze od rokowania AML, odpowiedzi na chemioterapię indukcyjną (osiągnięcie całkowitej remisji), od pacjenta (wiek, choroby współistniejące itp. ) oraz od życzeń terapeutycznych. Leczenie konsolidujące ma na celu wyeliminowanie resztkowych komórek białaczkowych, a tym samym zapobieganie nawrotom. Allogeniczny przeszczep szpiku kostnego jest leczeniem preferencyjnym, pozwalającym na osiągnięcie jak największej trwałej remisji, ale kosztem dość ciężkiego leczenia.
W przypadku odmowy lub niewłaściwego przeszczepu allogenicznego można kontynuować standardową chemioterapię, np. cytarabiną w dużych dawkach, azacytydyną lub klofarabiną . Inne opcje leczenia to terapie celowane. Autologicznego szpiku kostnego jest bardzo rzadki.
Alloprzeszczep
Allogeniczny przeszczep szpiku kostnego jest jedynym sposobem leczenia AML. Celem jest zniszczenie patologicznego szpiku kostnego pacjenta, a następnie odtworzenie z niego nowego szpiku za pomocą hematopoetycznych komórek macierzystych pobranych od zdrowego osobnika . Zarządzanie terapeutyczny jest złożony i wymaga odpowiedniego hematologii oferuje pokoje chronionych i innych obiektów szpitala ( jednostkowych terapii komórkowej , chemioterapia jednostce przetwórczej , itd. ).
Kwalifikowalność do przeszczepu jest oceniana kolegialnie i podejmowana w porozumieniu z pacjentem . Zabiegi wymagane do przeszczepu mają pewną toksyczność i wywołują długi okres aplazji i immunosupresji z wysokim ryzykiem powikłań i infekcji. Przeszczep alogeniczny jest zatem generalnie zarezerwowany dla osób „młodych” (poniżej 60 roku życia) i/lub w bardzo dobrym stanie ogólnym, którzy będą w stanie wesprzeć to leczenie i odnieść długofalowe korzyści z przeszczepu.
Z grubsza możemy wyróżnić 3 etapy. Po pierwsze, kondycjonowanie pacjenta polega na napromienianiu całego ciała , podaniu leków immunosupresyjnych i intensywnej chemioterapii. Jego celem jest eradykacja komórek białaczkowych, a także wywołanie znacznej immunosupresji umożliwiającej maksymalne ograniczenie odrzucenia przeszczepu . W heterologiczne komórki macierzyste są następnie wstrzykiwane. Kontynuacja postępowania polega na opanowaniu przedłużającej się niedokrwistości aplastycznej wywołanej kondycjonowaniem oraz możliwych powikłań i działań niepożądanych. W perspektywie średnioterminowej hematolog monitoruje stan przeszczepu i monitoruje skuteczne zanikanie komórek białaczkowych.
Na poziomie immunologicznym wprowadzenie do organizmu komórek obcych dla pacjenta (tzw. „ nie-własnych ”) może wywołać reakcję immunologiczną skierowaną przeciwko komórkom pacjenta lub przeciwko białaczce: skutki te są odpowiednio nazywane „ przeszczep przeciwko. gospodarz ”(GvH) i„ przeszczep vs. białaczka ”(GvL). Pierwszym jest mniej lub bardziej poważny niepożądany efekt, który może objawiać się w różnych miejscach (trawiennych, skórnych, itd. ) i odpowiada atakowi przeszczepionych komórek na narządy żywiciela; może być ostry lub przewlekły. Przeciwnie, efekt GvL jest korzystny, ponieważ komórki odpornościowe przeszczepu będą atakować komórki białaczki, a tym samym wywierać działanie przeciwnowotworowe. Oprócz GvH do powikłań po przeszczepie allogenicznym należą: zakażenia związane z immunosupresją i aplazją, zwiększone ryzyko nowotworów wtórnych, długotrwałe cytopenie wymagające transfuzji, choroba zarostowa żył wątrobowych oraz inne działania niepożądane chemioterapii.
W przypadku pacjentów wrażliwych lub starszych, którzy nie mogą wytrzymać standardowego przeszczepu allogenicznego, istnieją tak zwane protokoły „o zmniejszonej intensywności”, w których etap kondycjonowania (chemioterapia i radioterapia) obejmuje zmniejszone dawki: to rozwiązanie jest kompromisem, aby zachować korzyści z przeszczepu allogenicznego podczas przyjmowania uwzględnić niższą tolerancję pacjenta.
W 2016 roku we Francji wykonano nieco ponad 700 alloprzeszczepów w leczeniu AML. W roku 201 Europejskie Towarzystwo Przeszczepiania Krwi i Szpiku (EBMT) zidentyfikowało 6943 przeszczepy allogeniczne i 293 autoprzeszczepy z ostrą białaczką szpikową do wskazania.
Terapie celowane
Podczas diagnozy sekwencjonowanie genomu komórek białaczkowych umożliwia identyfikację wszelkich obecnych mutacji. Niektóre z nich uczestniczą w proliferacji i niedojrzałości blastów: mogą np. doprowadzić do syntezy nieprawidłowego białka, które trwale uruchomiłoby cykl komórkowy , prowadząc w ten sposób do niekontrolowanego podziału komórek. Zatrzymanie szkodliwego działania zmutowanych genów lub zmienionych białek stanowi zatem potencjalny cel terapeutyczny: tak opracowano w onkologii niektóre leki działające specyficznie na te nieprawidłowości . Są one pogrupowane razem pod nazwą terapie celowane w opozycji do klasycznej chemioterapii cytotoksycznej; określenie to obejmuje również inne leki o różnych mechanizmach działania, na przykład przeciwciała monoklonalne skierowane na receptory na powierzchni komórek ( klastry różnicowania ).
W 2016 roku przegląd literatury oszacował, że od 50% do 80% przypadków AML ma szkodliwe mutacje. Wśród najczęściej omawianych genów można wymienić FLT3 lub NPM1 (mutacje mogą współistnieć). W ramach opieki nad pacjentem znajomość zmutowanych genów pozwala nie tylko kategoryzować białaczkę, ustalać rokowanie, ale także przewidywać, jakie terapie celowane można przepisać pacjentowi. Chociaż nie ma jeszcze cząsteczki, która mogłaby przeciwdziałać każdemu genowi, kilka z nich zostało opracowanych w ciągu dekady 2010 r. i czasami uzyskało aprobatę od władz zajmujących się zdrowiem. Na przykład stwierdzono, że mutacje w dehydrogenazie izocytrynianowej (IDH), enzymie biorącym udział w metabolizmie energii komórkowej , mogą sprzyjać proliferacji komórek białaczkowych. W ten sposób opracowano inhibitory HDI: enasidenib (ukierunkowany na IDH2 ) i ivosidenib (ukierunkowany na IDH1 ). Różne inne terapie celowane mogą być przepisywane lub są przedmiotem badań klinicznych, takich jak glasdegib , wenetoklaks itp.
| Cel | Rodzaj | Przykład terapii celowanej |
|---|---|---|
| FLT3 | Białko | Midostauryna , gilteritynib (pl) kwizartinib (pl) |
| HDI | Białko | Iwosydenib (IDH1), enasydenib ( IDH2 ) |
| Bcl-2 | Białko | Wenetoklaks |
| CD33 | Receptor błonowy | Gemtuzumab ozogamycyna |
Stosowanie hormonów androgennych – które nie są ściśle ukierunkowanymi terapiami, ale raczej wchodzą w zakres terapii hormonalnej – było również przedmiotem badań klinicznych. W szczególności wydaje się, że norethandrolon poprawia przeżycie i remisję u pacjentów w podeszłym wieku.
Wreszcie, niektóre chemioterapie, mimo że posiadają klasyczny mechanizm ingerujący w syntezę DNA, mogą mieć również dodatkowe właściwości celowane. Azacytydyna ma na przykład działanie hipometylujące: może wywoływać wycofanie metylowych grup chemicznych (-CH 3 )nici DNA, a tym samym umożliwiają ponowną ekspresję pewnych genów kontrolujących podział komórkowy komórki.
Inne sytuacje
Nawracające lub oporne postacie AML leczy się według określonych protokołów, zazwyczaj chemioterapią (leczenie ratunkowe lub ratunkowe).
Jeśli chodzi o immunoterapię , gemtuzumab ozogamycyny jest jedynym przeciwciałem monoklonalnym zatwierdzonym do leczenia AML. Immunocheckpoint inhibitorów (takich jak ipilimumab , The nivolumab ) lub komórek T, CAR (limfocyty genetycznie modyfikowanych), nie są w 2020 roku, podano w leczeniu przypadków ostrej białaczki szpikowej, ale są przedmiotem badań dla badań klinicznych.
Przetrwanie
Rokowanie jest na ogół wyrażane przez całkowity czas przeżycia po 5 latach, to znaczy przez odsetka pacjentów wciąż Alive 5 lat po ich diagnozy, biorąc pod uwagę wszystkie przyczyny śmierci połączonej (czy związanej Lam, jego konsekwencje, do drugiego niepowiązane zdarzenie, takie jak wypadek drogowy). W onkologii do oceny rokowania w trakcie leczenia lub w badaniach klinicznych można stosować inne środki : możemy mówić o przeżyciach bez nawrotów, bez progresji lub w odpowiedzi na leczenie (odpowiedź całkowita, częściowa itp.).
U dorosłych przeżycie w wieku 5 lat szacuje się na około 25% i maleje wraz z wiekiem: wynosi 40% przed 65 rokiem życia, a następnie 5% po. W pediatrii prawdopodobieństwo całkowitego 5-letniego przeżycia wzrosło z 50% w latach 90. do około 60-70% w 2010 r. (w ostrej białaczce limfoblastycznej sięgało 90% w 2010 r.). Ponownie, szanse przeżycia małych dzieci są nieco wyższe niż w przypadku nastolatków.
Dane te nie mają zastosowania do ostrej białaczki promielocytowej (dawniej AML 3). Wcześniej kojarzone z ponurymi rokowaniami nowe terapie (kombinacja ATRA / ATO ) od 2000 roku umożliwiły uzyskanie długotrwałych remisji u 90% pacjentów.
Historia
Pierwszy opis w literaturze medycznej przypadku białaczki pochodzi z 1827 r. Alfred Velpeau opisał przypadek 63-letniego kwiaciarza cierpiącego na chorobę z gorączką, zmęczeniem, kamieniami nerkowymi oraz dużą powiększoną wątrobą i śledzioną . Zaobserwował, że krew pacjenta miała konsystencję owsianki i postulował, że ten wygląd może być spowodowany białymi cząsteczkami. W 1845 roku patolog JH Bennett doniósł o serii przypadków pacjentów, którzy zmarli z powodu poszerzenia śledziony i „zmiany koloru konsystencji ich krwi”. następnie używa terminu „leukocytemia”, aby opisać ten stan.
Słowa „białaczka” po raz pierwszy użył Rudolf Virchow , niemiecki patolog, w 1856 roku. Opisał on za pomocą mikroskopu nadmiar białych krwinek u osób wykazujących objawy opisane przez Velpeau i Benetta. Virchow, nie znając pochodzenia tej anomalii, nazwał ją czysto opisowym terminem białaczka (po grecku: biała krew ).
Uwagi i referencje
Uwagi
(fr) Ten artykuł jest częściowo lub w całości zaczerpnięty z artykułu w angielskiej Wikipedii zatytułowanego „ Ostra białaczka szpikowa ” ( patrz lista autorów ) .- Anglicyzm od ostrego do „ostrego”, co oznacza przejście od choroby przewlekłej do ostrego; powiązany czasownik to „acutiser”.
Bibliografia
- Grand Dictionnaire Terminologique , Office québécois de la langue française, „ ostra białaczka ” ,2019(dostęp 28 grudnia 2019 )
- MSD , Ashkan Emadi, Jennie York Law, „ Ostra białaczka szpikowa (AML) – Hematologia i Onkologia – Profesjonalne wydanie podręcznika MSD ” ,grudzień 2018(dostęp 29 grudnia 2019 )
- (en) National Cancer Institute , „ Leczenie dorosłych ostrej białaczki szpikowej (PDQ®) – wersja zawodowa w służbie zdrowia ” ,8 lutego 2019(dostęp 28 grudnia 2019 )
- Institut National Du Cancer, „ Podsumowanie - Krajowe szacunki dotyczące zachorowalności i umieralności na raka we Francji kontynentalnej w latach 1990–2018 - Ref: SYNINCNAT2019 ” , na www.e-cancer.fr ,lipiec 2019(dostęp 8 września 2019 )
- INSERM, „ Orphanet: ostra białaczka szpikowa ” , na orpha.net ,czerwiec 2014(dostęp 8 września 2019 )
- (w) D. Weber, E. Fromm, S. Erhardt, Pan Lübbert W. Fiedler, T. Kindler, J. Krauter, P. Brossart, A. Kündgen, HR Salih J. Westermann, G. Wulf , B Hertenstein, M. Wattad, K. Götze, D. Kraemer, T. Heinicke, M. Girschikofsky, HG Derigs, HA Horst, C. Rudolph, M. Heuser, G. Göhring, V. Teleanu, L. Bullinger, F. . Thol VI Gaidzik P. Paschka K. Döhner'a A. Ganser Hartmut Döhner'a RF Schlenka niemiecki-austriacki AML Study Group (AMLSG) Gabriele Nagel , „ epidemiologiczne genetyczny i charakterystyki klinicznej według wieku niedawno zdiagnozowano ostrą białaczka szpikowa na podstawie badania rejestrowego populacji akademickiej (AMLSG BiO) ” , Annals of Hematology , tom. 96 N O 12,31 października 2017 r., s. 1993 ( DOI 10.1007 / s00277-017-3150-3 , / pmc / artykuły / PMC5691091 / ? Raport = streszczenie, czytaj online )
- SEER, „ Ostra białaczka szpikowa – fakty dotyczące raka ” na stronie seer.cancer.gov (dostęp 8 września 2019 r. )
- Visser O i wsp., „ Zapadalność, przeżycie i występowanie nowotworów szpiku w Europie. » , na www.ncbi.nlm.nih.gov ,listopad 2012(dostęp 8 września 2019 )
- Global Burden of Disease Study, „ Globalne obciążenie raka dzieci i młodzieży w 2017 roku: analiza Global Burden of Disease Study 2017 ” , na stronie www.thelancet.com ,29 lipca 2019 r.(dostęp 14 września 2019 )
- Smith MA, Ries LA, Gurney JG i in., „ Częstość i przeżycie raka wśród dzieci i młodzieży: United States SEER Program 1975-1995 ” , na stronie seer.cancer.gov ,31 stycznia 2019(dostęp 15 września 2019 )
- Global Burden of Disease Study, „ Globalna, regionalna i krajowa śmiertelność ze względu na wiek i płeć dla 282 przyczyn zgonu w 195 krajach i terytoriach, 1980–2017: systematyczna analiza dla Global Burden of Disease Study 2017 ” , na stronie www .thelancet.com ,10 listopada 2018 r.(dostęp 14 września 2019 )
- VJ Cogliano , R. Baan , K. Straif , Y. Grosse , B. Lauby-Secretan , F. El Ghissassi , V. Bouvard , L. Benbrahim- Tallaa , N. Guha , C. Freeman , L. Galichet i CP Dzikie , „ Ekspozycje, którym można zapobiegać, związane z rakiem u ludzi ” , „ JNCI Journal of the National Cancer Institute” , tom. 103 n O 24,2011, s. 1827-1839 ( ISSN 0027-8874 , DOI 10.1093 / jnci / djr483 )
- " Klasyfikacja IARC według stron onkologicznych | Rak i środowisko ” (dostęp 24 listopada 2019 r. )
- Musée Curie , „ Biografia Marii Curie ” (dostęp 24 listopada 2019 r. )
- Musée Curie , „ Biography of Irene and Frédéric Joliot-Curie ” (dostęp 24 listopada 2019 r. )
- Klervi Leuraud David B Richardson , Elisabeth Cardis , Robert D Daniels , Michael Gillies , Jacqueline O'Hagan , Ghassan B Hamra , Richard Haylock Dominique Laurier , Monika Moissonnier , Mary K Schubauer-Berigan , Isabelle Thierry-Chef i Aušrelé Kesminiene , „ Promieniowanie jonizujące i ryzyko śmierci z powodu białaczki i chłoniaka u pracowników monitorowanych promieniowaniem (INWORKS): międzynarodowe badanie kohortowe ”, The Lancet Hematology , tom. 2, n O 7,2015, e276 – e281 ( ISSN 2352-3026 , DOI 10.1016 / S2352-3026 (15) 00094-0 )
- INRS, „ Benzen (FT 49). Patologia - Toksykologia - Karta toksykologiczna - INRS ” ,2011(dostęp 8 września 2019 )
- Loomis A., „ Carcinogenicity of benzene ” , na www.thelancet.com ,26 października 2017(dostęp 8 września 2019 )
- IARC, „ Monografie benzenu – IARC dotyczące oceny ryzyka rakotwórczego dla ludzi ” , na stronie iarc.fr ,2018(dostęp 8 września 2019 )
- Kathryn Z Guyton , Dana Loomis , Yann Grosse , Fatiha El Ghissassi Lamia Benbrahim-Tallaa , Neela Guha , Chiara Scoccianti Heidi Mattock i Kurt Straif " rakotwórcze z tetrachlorwinfos, paration, malation, diazynon, a glifosat ," The Lancet Oncology , vol . 16 N O 5,2015, s. 490–491 ( ISSN 1470-2045 , DOI 10.1016 / S1470-2045 (15) 70134-8 )
- Gabriella Andreotti , Stella Koutros , Jonathan N Hofmann , Dale P Sandler , Jay H Lubin , Charles F Lynch , Catherine C Lerro , Anneclaire J De Roos , Christine G Parks , Michael C Alavanja , Debra T Silverman i Laura E Beane Freeman ” Stosowanie glifosatu i występowanie raka w badaniu zdrowia w rolnictwie ”, JNCI: Journal of the National Cancer Institute , tom. 110 n O 5,2018, s. 509-516 ( ISSN 0027-8874 , DOI 10.1093 / jnci / djx233 )
- Centre Léon-Bérard , IARC, “ Klasyfikacja IARC według lokalizacji rakowych | Rak a środowisko ” ,29 listopada 2019 r.(dostęp 29 grudnia 2019 )
- Centre National Hospitalier d'Information sur le Médicament (CNHIM), „ Adverse response sheet ” , na theriaque.org (dostęp 15 września 2019 )
- (w) Sachiko Ezoe , „ Wtórna białaczka związana ze środkiem przeciwnowotworowym, etopozydem, inhibitorem topoizomerazy II ” , International Journal of Environmental Research and Public Health , tom. 9 N O 7,30 listopada 12, s. 2444 ( DOI 10.3390 / ijerph9072444 , / pmc / artykuły / PMC3407914 /? Raport = streszczenie, przeczytaj online )
- Barbara Deschler i Michael Lübbert , „ Ostra białaczka szpikowa: epidemiologia i etiologia ”, Rak , tom. 107 N O 9,2006, s. 2099-2107 ( ISSN 0008-543X , DOI 10.1002 / cncr.22233 )
- LLSCanada, " www.llscanada.org " (dostęp na 1 st marca 2020 )
- Hoffman, Ronald i in. (2005). Hematologia: podstawowe zasady i praktyka (wyd. 4). St. Louis, Mo .: Elsevier Churchill Livingstone. str. 1074–75
- Ostra białaczka szpikowa , N Engl J Med 1999; 341.
- Botton 2017 , s. 500-501
- Schmidt, Cornu, Angellilo-Scherrer i in. , „ Podstawy fizjopatologiczne w hematologii ogólnej: pomoc pamięciowa w hematologii ” [PDF] , na www.2bib.ch ,2015(dostęp 10.12.2019 ) , s. 149
- Ifrah 2018 , s. 68
- Francuskie Towarzystwo Hematologiczne, „ Ostra białaczka, 3 – Objawy biologiczne i diagnostyka ” [html] ,1 st kwiecień 2010(dostęp 15 grudnia 2019 )
- Botton 2017 , s. 500
- (w) James W. Vardiman , „ Rewizja 2016 klasyfikacji nowotworów szpiku i ostrej białaczki Światowej Organizacji Zdrowia ” , Blood , American Society of Hematology, tom. 127 n O 20,19 maja 2016, s. 2391-2405 ( ISSN 1528-0020 , DOI 10.1182 / krew-2016-03-643544 , streszczenie , czytaj online )
- (w) Karen Seiter, Emmanuel C. Besa i in. , „ Ostrej oceny zaawansowania białaczki szpikowej — klasyfikacje FAB i WHO dla ostrej białaczki szpikowej ” , na stronie emedicine.medscape.com ,30 grudnia 2015(dostęp 23 kwietnia 2016 r . ) .
- „Aktualizacja dotycząca ostrej białaczki szpikowej, wrzesień 2016, s. 3/16”
- " Wszystko o darowiznach | Don de Moelle Osseuse ” , na www.dondemoelleosseuse.fr (dostęp 11 listopada 2018 r. )
- Hartmut Döhner , Elihu Estey , David Grimwade , Sergio Amadori , Frederick R. Appelbaum , Thomas Büchner , Hervé Dombret , Benjamin L. Ebert , Pierre Fenaux , Richard A. Larson , Ross L. Levine , Francesco Lo-Coco , Tomoki Naoe , Dietger Niederwieser Gert J. Ossenkoppele Miguel Sanz , Jorge Sierra Martin S. Tallman , Hwei-Fang Tien , Andrew H. Wei , Bob Löwenberg i Clara D. Bloomfield „, diagnostyce i leczeniu AML u dorosłych: Rekomendacje ELN 2017 międzynarodowego panelu ekspertów ”, Krew , tom. 129 n O 4,2017, s. 424-447 ( ISSN 0006-4971 , DOI 10.1182 / krew-2016-08-733196 )
- Martin S. Tallman , Eunice S. Wang , Jessica K. Altman , Frederick R. Appelbaum , Vijaya Raj Bhatt , Dale Bixby , Steven E. Coutre , Marcos De Lima , Amir T. Fathi , Melanie Fiorella , James M. Foran , Aric C. Hall , Meagan Jacoby , Jeffrey Lancet , Thomas W. LeBlanc , Gabriel Mannis , Guido Marcucci , Michael G. Martin , Alice Mims , Margaret R. O'Donnell , Rebecca Olin , Deniz Peker , Alexander Perl , Daniel A. Pollyea , Keith Pratz , Thomas Prebet , Farhad Ravandi , Paul J. Shami , Richard M. Stone , Stephen A. Strickland , Matthew Wieduwilt , Kristina M. Gregory , Lydia Hammond i Ndiya Ogba , " Ostra białaczka szpikowa , wersja 3.2019 , NCCN Clinical Practice Guidelines in Oncology ”, Journal of the National Comprehensive Cancer Network , tom. 17 N O 6,2019, s. 721-749 ( ISSN 1540-1405 , DOI 10.6004 / jnccn.2019.0028 )
- (w) Cancer Research UK, „ Radioterapia mózgu – ostra białaczka szpikowa ” ,16 lipca 2019(dostęp 29 grudnia 2019 )
- (en + es) American Cancer Society, „ Terapia radiologiczna w ostrej białaczce szpikowej (AML) ” ,21 sierpnia 2018 r.(dostęp 29 grudnia 2019 )
- Miguel A. Sanz , Pierre FENAUX Martin S. Tallman , Elihu H. Estey Bob Löwenberg , Tomoki Naoe , Eva Lengfelder Hartmut Döhner'a , Alan K. Burnett , Sai-Juan Chen , Vikram Mathews , Harry iland Eduardo Rego , Hagop Kantarjian Lionel Ades , Giuseppe Avvisati Pau Montesinos , Uwe Platzbecker , Farhad Ravandi Nigel H. Russell i Francesco Lo-Coco „ Zarządzanie ostrą białaczką promielocytową: zaktualizowane zalecenia panelu ekspertów Europejskiego LeukemiaNet ” Krew , vol . 133 n O 15,2019, s. 1630-1643 ( ISSN 0006-4971 , DOI 10.1182 / krew-2019-01-894980 )
- Gustave Roussy , „ Opieka wspomagająca – Gustave Roussy ” (dostęp 18 marca 2020 r. )
- Institut Curie , „ Pomagamy podczas zabiegów Institut Curie ” (dostęp 18 marca 2020 )
- (w) Redakcja PDQ Adult Treatment, " Leczenie dorosłych ostrej białaczki szpikowej (PDQ®) - Cancer Information Summaries PDQ - NCBI Bookshelf " [html] , Bethesda (MD): National Cancer Institute (US)8 lutego 2019(dostęp 17 grudnia 2019 )
- Europejska Agencja Leków , " Dacogen " ,13 maja 2019 r.(dostęp 3 stycznia 2020 r. )
- Botton 2017 , s. 504
- Biomedycznych Agencji , " aktywność przeszczep Narodowy CSH (2016) " [PDF] , na www.agence-biomedecine.fr ,2017(dostęp 7 stycznia 2020 r. )
- Carreras 2019 , s. 27
- EMA , „ Bulsilvex (busulfan) – Charakterystyka Produktu Leczniczego ” [PDF] ,31 sierpnia 2017 r.(dostęp 23 czerwca 2020 r. )
- Canadian Cancer Society, „ Przeszczep komórek macierzystych w ostrej białaczce szpikowej ” (dostęp 23 czerwca 2020 r. )
- Ifrah 2018 , s. 77
- „ Hematologia. Onko-hematologia - Prezentacja - Konsultant EM » ,5 grudnia 11(dostęp 7 stycznia 2020 r. )
- (w) Cancer Research UK, „ Radioterapia całego ciała (TBI) Ostra białaczka szpikowa ” ,16 lipca 2019(dostęp 29 grudnia 2019 )
- The Leukemia & Lymphoma Society of Canada, „ Stem Cell Allogeneic Transplant ” (dostęp 7 stycznia 2020 r. )
- The Leukemia & Lymphoma Society of Canada, „ Alogeniczny przeszczep komórek macierzystych o zmniejszonej intensywności ” (dostęp 23 czerwca 2020 r. )
- (pl) Europejskie Towarzystwo Przeszczepu Krwi i Szpiku , „ Sprawozdanie roczne 2019 ” [2019]2019(dostęp 23 czerwca 2020 r. ) ,s. 68
- Jeanette Prada-Arismendy , Johanna C. Arroyave i Sarah Röthlisberger , „ Biomarkery molekularne w ostrej białaczce szpikowej ”, Blood Reviews , tom. 31, n o 1,2017, s. 63-76 ( ISSN 0268-960X , DOI 10.1016 / j.blre.2016.08.005 )
- (w) American Cancer Society, „ Co nowego w badaniach nad ostrą białaczką szpikową (AML)? " ,24 czerwca 2019 r.(dostęp 23 czerwca 2020 r. )
- Elihu Estey , Judith E. Karp , Ashkan Emadi , Megan Othus i Robert Peter Gale , „ Niedawne dopuszczenia leków na nowo zdiagnozowaną ostrą białaczkę szpikową: prezenty czy koń trojański? », Białaczka , tom. 34, n o 3,2020, s. 671-681 ( ISSN 0887-6924 , DOI 10.1038 / s41375-019-0704-5 )
- (w) " izocytrynianowej dehydrogenazy mutacji w białaczce nowotworów " (recenzja " białaczka " opublikowanym 11 listopada 2016), Nature (czasopismo) , n o 31,2017, s. 272–281 ( DOI 10.1038 / leu.2016.275 , czytaj online )
- „Ash, Clinicak News, 21 października 2016 r., Obietnica wyników klinicznych AG-221„ Rewolucyjne ”podejście do AML”
- Starr P, „ Midostauryna pierwsza terapia celowana w celu poprawy przeżycia w AML: potencjalna zmiana praktyki ”, Am Health Drug Benefits , tom. 9 N O Spec Issue,luty 2016, s. 1–21 ( PMID 27014400 , PMCID 4782225 )
- Alexander E. Perl , Giovanni Martinelli , Jorge E. Cortes , Andreas Neubauer , Ellin Berman , Stefania Paolini , Pau Montesinos , Maria R. Baer , Richard A. Larson , Celalettin Ustun , Francesco Fabbiano , Harry P. Erba , Antonio Di Stasi Robert Stuart , Rebecca Olin , Małgorzata Kasner , Fabio Ciceri , Wen-Chien Chou , Nikolai Podoltsev Christian Recher , Hisayuki Yokoyama , Naoko Hosono , Sung-Soo Yoon , I-Hwan Lee , Timothy Pardee , T. Amir Fathi , Chaofeng Liu , Nahla Hasabou , Xuan Liu , Erkut Bahceci i Mark J. Levis , „ Gilteritinib lub chemioterapia w przypadku nawrotu lub oporności na AML z mutacją FLT3 ”, New England Journal of Medicine , tom. 381 n O 182019, s. 1728-1740 ( ISSN 0028-4793 , DOI 10.1056/ NEJMoa1902688 )
- Arnaud Pigneux Marie C. bene , Philippe Guardiola , Christian Recherche , Jean-Francois Hamel , Mathieu Sauvezie , Jean-Luc Harousseau Olivier Tournilhac Francis Witz , Christian Berthou , Martine Escoffre-Barbe , Denis Guyotat , Nathalie Fegueux Chantal Himberlin , Mathilde Hunault , Martine Delain , Bruno Lioure Eric Jourdan , Frederic Bauduer Francois Dreyfus , Jean-Yves Cahn , Jean-Jacques Sotto i Norbert Ifrah " Dodawanie androgenów poprawia przeżycie u starszych pacjentów z ostrą białaczką szpikową: a GOELAMS Study " , Journal of Clinical Oncology , tom. 35, n o 4,2017, s. 387-393 ( ISSN 0732-183X , DOI 10.1200 / JCO.2016.67.6213 )
- Europejska Agencja Leków , " Vidaza - Charakterystyka Produktu Leczniczego " [PDF] , na www.ema.europa.eu ,9 lipca 2019(dostęp 25 czerwca 2020 r. )
- Europejska Agencja Leków , „ www.ema.europa.eu ” [PDF] ,25 października 2019 r.(dostęp 18 marca 2020 r. )
- Ceylad, „ Celiad zgłasza pierwszą całkowitą odpowiedź u pacjenta z oporną na leczenie i nawracającą AML w badaniu THINK ” , na stronie internetowej ,3 października 2017 r.(dostęp 18 marca 2020 r. )
- Yuxin Liu , Jan Philipp Bewersdorf , Maximilian Stahl i Amer M. Zeidan , „ Immunoterapia w ostrej białaczce szpikowej i zespołach mielodysplastycznych: początek nowej ery? ”, Recenzje krwi , tom. 34,2019, s. 67-83 ( ISSN 0268-960X , DOI 10.1016 / j.blre.2018.12.001 )
- (w) Amerykańskie Towarzystwo Onkologii Klinicznej , „ Białaczka - Ostra mieloida - AML: Statystyka | Cancer.Net ” , na www.cancer.net ,styczeń 2020(dostęp 27 czerwca 2020 r. )
- (en) National Cancer Institute , „ Leczenie dorosłych ostrej białaczki szpikowej (PDQ®) – wersja dla pracowników służby zdrowia ” na stronie www.cancer.gov ,22 stycznia 2020(dostęp 27 czerwca 2020 r. )
- (w) Cancer Research UK , " Survival | Ostra białaczka szpikowa | Cancer Research UK ” , na stronie www.cancerresearchuk.org ,19 lipca 2019(dostęp 27 czerwca 2020 r. )
- Mareike Rasche , Martin Zimmermann , Lisa Borschel , Jean-Pierre Bourquin , Michael Dworzak , Thomas Klingebiel , Thomas Lehrnbecher , Ursula Creutzig , Jan-Henning Klusmann i Dirk Reinhardt , „ Sukcesy i wyzwania w leczeniu retrospektywnej ostrej choroby szpikowej u dzieci analiza badań AML-BFM od 1987 do 2012 ”, Białaczka , tom. 32 N O 10,2018, s. 2167-2177 ( ISSN 0887-6924 , DOI 10.1038 / s41375-018-0071-7 )
- Fundacja ARC, „ Co to jest białaczka dziecięca?” | ARC Foundation for Cancer Research ” , na stronie internetowej ,14 lutego 2020 r.(dostęp 18 marca 2020 r. )
- American Cancer Society , „Wskaźniki odpowiedzi na leczenie w przypadku ostrej białaczki szpikowej (AML) ” na stronie www.cancer.org ,21 sierpnia 2018 r.(dostęp 27 czerwca 2020 r. )
- Hoffman i in. 2005, s. 1071.
- Bennett JH, „ Dwa przypadki przerostu śledziony i wątroby, w których nastąpiła śmierć z powodu ropienia krwi ”, Edinburgh Med Surg J , tom. 64,1845, s. 413
- (de) R Virchow , Gesammelte Abhandlungen zur Wissenschaftlichen Medizin , Frankfurt, Meidinger,1856( czytaj online ) , „Die Leukämie” , 190”
Bibliografia
![]() : dokument używany jako źródło tego artykułu.
: dokument używany jako źródło tego artykułu.
-
Norbert Ifrah ( dyrektor i koordynator), Marc Maynadié ( dyrektor i koordynator) i in. , Francuskie Towarzystwo Hematologiczne, Hematologiczne , Issy-les-Moulineaux, Elsevier Masson, coll. „Repozytoria Uczelni”,maj 2018, 3 e wyd. , 400 pkt. ( ISBN 978-2-294-75108-0 i 9782294752636 , EAN 9782294752636 , zawiadomienie BNF n O FRBNF45533912 ).

-
R. Costello, G. Venton, J. Colle, V. Ivanov, C. Mercier, L. Delassus i V. Baccini (art. 13-018-G-50), Ostra białaczka szpikowa u dorosłych , Elsevier Masson , coll. "EMC / Hematologia",2018, 13 pkt. ( ISBN 978-2-84299-505-8 , ISSN 1155-1984 , OCLC 726481102 , DOI 10.1016 / S1155-1984 (18) 83321-0 , czytaj online [html] ). .

-
Stéphane Vignot ( red. i redaktor), Jean-Charles Soria ( red. ) And Stéphane de Botton , Gustave Roussy & Université Paris Sud XI, Kurs chemioterapii przeciwnowotworowej i leczenia raka , Paryż,styczeń 2018, 32 th ed. , 534 s. ( ISBN 978-2-9555469-9-4 ) , rozdz. 83 ( „Ostra białaczka szpikowa”).

-
(en) Enric Carreras , Carlo Dufour , Mohamad Mohty i Nicolaus Kröger , Europejskie Towarzystwo Transplantacji Szpiku, Podręcznik EBMT: Transplantacja komórek macierzystych krwi i terapia komórkowa , Cham, Szwajcaria, Springer,2019, 688 s. ( ISBN 978-3-030-02277-8 (błędnie zredagowany) i 978-3-030-02278-5 , DOI 10.1007 / 978-3-030-02278-5 , czytaj online [PDF] ).

Zobacz również
Powiązane artykuły
Linki zewnętrzne
Ogółu społeczeństwa- Orphanet
- Przewodnik dla pacjentów opublikowany przez Europejskie Towarzystwo Onkologii Medycznej (ESMO)
- Francuskie Towarzystwo Hematologiczne
- rak.be
- rak.ca
- Fundacja ARC
- Laurette Fugain , stowarzyszenie zaangażowane w walkę z białaczką
- (en + es) Narodowy Instytut Raka
- Hématocell.fr (laboratorium hematologiczne Szpitala Uniwersyteckiego Angers)
- (pl) Europejska sieć białaczki
- (en + es) Narodowy Instytut Raka