Naftalen
| Naftalen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
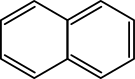  Struktura naftalenu. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nazwa IUPAC | naftalen | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nazwa systematyczna | bicyklo [4.4.0] deka-1,3,5,7,9-penten | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonimy |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O ECHA | 100,001,863 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O WE | 202-049-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 931 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| UŚMIECHY |
C1 = C2C (= CC = C1) C = CC = C2 , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1S / C10H8 / c1-2-6-10-8-4-3-7-9 (10) 5-1 / h1-8H InChIKey: UFWIBTONFRDIAS-UHFFFAOYSA-N |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd | Bezbarwne romboedryczne kryształy w postaci łusek. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości chemiczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formula |
C 10 H 8 [Izomery] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa cząsteczkowa | 128,1705 ± 0,0086 g / mol C 93,71%, H 6,29%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Podatność magnetyczna | 91,9 × 10-6 cm 3 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości fizyczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuzja | 80,2 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| * Temperatura wrzenia | 217,96 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozpuszczalność |
32 mg · L -1 wody w 20 ° C . Miele w etanolu , eterze , benzenie , chloroformie , kwas octowy , kwas chlorowodorowy , i oleje |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametr rozpuszczalności δ | 20,3 MPa 1/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa objętościowa |
1,162 g · cm -3 ( 20 ° C )
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura samozapłonu | 567 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura zapłonu | 79 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Granice wybuchowości w powietrzu | 0,9 - 5,9 % obj | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nasycenie prężności par | przy 25 ° C : 11 Pa
równanie:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punkt krytyczny |
475,2 ° C ,
40,0 atm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Potrójny punkt | 80,28 ° C , 999,6 Pa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochemia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
równanie:
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SZT | 5 156,3 kJ · mol -1 ( 25 ° C , ciało stałe) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalografia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| System kryształów | Jednoskośny | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klasa kryształu lub grupa kosmiczna | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parametry siatki | a = 8,24 Å b = 6,00 A |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości optyczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Współczynnik załamania światła | 1.5822 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Środki ostrożności | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   Ostrzeżenie H302, H351, H410, P273, P281, P501, H302 : Działa szkodliwie po połknięciu H351 : Podejrzewa się, że powoduje raka (wskazać drogę narażenia, jeżeli definitywnie udowodniono, że żadna inna droga narażenia nie powoduje takiego samego zagrożenia) H410 : Działa bardzo toksycznie na organizmy wodne, powoduje długotrwałe skutki P273 : Unikać uwolnienia do środowisko. P281 : Stosować wymagane środki ochrony indywidualnej. P501 : Zawartość / pojemnik usuwać do ... |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  B4, D2A, B4 : Substancja stała łatwopalna Transport towarów niebezpiecznych: klasa 4.1 D2A : Materiał bardzo toksyczny powodujący inne skutki toksyczne Rakotwórczość: IARC grupa 2B Ujawnienie na poziomie 0,1% zgodnie z kryteriami klasyfikacji |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 2 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
40 : materiał stały łatwopalny, materiał samoreaktywny lub samonagrzewający się Numer UN : 1334 : NAFTALEN SUROWY; lub RAFINOWANY NAFTALEN Klasa: 4.1 Etykieta: 4.1 : Substancje stałe łatwopalne, substancje samoreaktywne i materiały wybuchowe odczulone 
44 : łatwopalne ciało stałe, które w podwyższonej temperaturze znajduje się w stanie stopionym Numer UN : 2304 : STOPIONY NAFTALEN |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klasyfikacja IARC | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupa 2B: prawdopodobnie rakotwórczy dla ludzi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoksykologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 3.3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Próg zapachu | niska: 0,0095 ppm wysoka: 0,64 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Związki pokrewne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izomery | Azulen | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednostki SI i STP, chyba że określono inaczej. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Naftalenu lub naftalenu lub kamfora smoła jest policykliczne węglowodory aromatyczne , konkretnie aceny ma dwa pierścienie o wzór empiryczny C 10 H 8. Jego charakterystyczny zapach jest wyczuwalny przez ludzki zapach już od 0,04 ppm . Był powszechnie stosowany jako środek odstraszający mole . Stwierdzono, monitorując choroby pracowników przemysłu chemicznego, że jest on prawdopodobnie rakotwórczy.
Pochodzenie i produkcja
Naftalen został wyizolowany w 1820 roku przez Garden. Jego obecna reprezentacja w postaci dwóch jąder aromatycznych została zaproponowana przez Erlenmeyera w 1868 roku.
W Niemczech surowcem używanym do produkcji naftalenu jest smoła węglowa , która zawiera około 10%. Ponieważ produkcja koksu spada, coraz więcej produktów pochodzących z ropy naftowej (benzyna pirolityczna , pozostałości olejów pirolitycznych) jest używanych; produkcja metodą destylacji frakcyjnej.
Zawartość naftalenu w produkcie technicznym wynosi co najmniej 95%, pozostałość składa się z zanieczyszczeń, takich jak benzo (b) tiofen ( tionaften ), aw przypadku naftalenów otrzymywanych z ropy naftowej wyłącznie metyloindeny .
Używa
Naftalen był wcześniej używany głównie jako środek odstraszający mole ( w tym celu zastosowano również paradichlorobenzen ). Według INERIS , obecnie 60% wyprodukowanego naftalenu jest sprzedawane jako półprodukt do produkcji bezwodnika ftalowego . Ten bezwodnik ftalowy służy do syntezy ftalanów i różnych plastyfikatorów , żywic , barwników , insektycydów lub repelentów itp. Jest on również stosowany jako środek opalania na skórę i pewnych środków powierzchniowo czynnych ( sulfoniany naftalenu i pochodnych mających działanie dyspergujące i zwilżające w farby , barwniki, formowania papieru do pakowania w procesie wytwarzania betonu i okładziny tynkowej).
Napalmowy zasadniczo stosowane w Wietnamie , pierwotnie otrzymano z naftalenu (stąd „NA”) i kwas palmitynowy (stąd „Palm”). Naftalen jest również używany do uzyskania efektów pirotechnicznych, podczas eksplozji powstaje bardzo czarny dym.
Może być używany do produkcji niektórych tworzyw sztucznych (w szczególności poprzez syntezę ftalanów), barwników ... ale także do innych, bardziej marginalnych zastosowań: antyseptyki, środki bakteriobójcze, dielektryczne, perfumy ...
W środowisku
Gatunek amerykańskiego termita Coptotermes formosanus wydziela niewielkie ilości naftalenu do walki z pasożytami i ich głównym drapieżnikiem, mrówką Solenopsis invicta , ale większość naftalenu występującego w naturze (około 89% według INERIS) pochodzi z niekompletnych procesów spalania ( pirolizy ) ( ogrzewanie domowe drewnem) oraz sublimacja naftalenu stosowanego jako środek owadobójczy. Około 10% emisji do powietrza pochodziłoby z destylacji węgla. Dym tytoniowy zawiera go w niewielkich ilościach.
Naftalen będąc lotnym (przez sublimację ) szybko się rozprasza. Średnia szybkość w powietrzu wyniosłaby 1 µg m- 3 , czyli znacznie więcej niż w wodzie morskiej, gdzie jest słabo rozpuszczalna ( 10 ng l- 1 ) i skąd może odgazować w powietrzu ( podobnie jak w wodzie słodkiej ). Gleby ( średnio 2 µg kg –1 ) słabo go zatrzymują (odgazowanie, średnia adsorpcja). Zwykle nie występuje w osadach (2 µg kg –1 ). Testy adsorpcji / desorpcji wymienione przez INERIS dają wartości Koc od 378 do 3200 L kg- 1 . Komisja Europejska (WE, 1996) przyjęła wartość 1320 L kg- 1 .
Bioakumulacja
Jego ekotoksykologiczne skutki nie są dobrze znane, ale wykazano, że wykazuje bioakumulację u kilku gatunków ryb (np. Cyprinus carpio , Pimephales promelas ), omułków ( Mytilus edulis ) i ostryg ( Ostrea edulis ) .
Wydaje się, że naftalen może być wchłaniany przez korzenie i liście roślin, ale INERIS w 2005 r. Nie znalazł żadnych badań dotyczących jego skutków ani możliwych czynników biokoncentracji.
Degradacja
Ze względu na swoją strukturę chemiczną uważa się, że naftalen jest bardzo stabilny.
Wydaje się, że w normalnych warunkach bardzo słabo ulega biodegradacji. Standardowy test wykazał jedynie 2% degradacji po 28 dniach, ale testy (nie znormalizowane) sugerują, że może on ulec szybkiej biodegradacji w warunkach tlenowych i denitryfikacyjnych po kontakcie z niektórymi mikroorganizmami, które prawie to robią. Znikają w ciągu 8 do 12 dni w najlepsze przypadki.
Komisja Europejska (WE, 1996) przyjęła okres półtrwania wynoszący 150 dni w wodach powierzchniowych. Kilka (niestandaryzowanych) testów biodegradacji w warunkach beztlenowych , w szczególności w osadach, sugeruje, że jest on stabilny w tych warunkach.
Toksykologia
Różne raporty z ATSDR (1995) oraz Agencji Ochrony Środowiska w Stanach Zjednoczonych ( 1998 ) podkreśliły kilka właściwości toksykologicznych tego produktu (patrz także raport INERIS " wielopierścieniowych węglowodorów aromatycznych (WWA): Ocena zależności dawka-odpowiedź dla działanie rakotwórcze - Podejście według substancji Uważają, że naftalen może być wchłaniany, aw niektórych przypadkach może powodować zatrucie przez drogi oddechowe i pokarmowe, a także przez skórę w kontakcie z prześcieradłami lub ubraniami poddanymi działaniu antymoli, zwłaszcza u noworodków W ludzkim organizmie znane są co najmniej dwa stabilne metabolity naftalenu: 1-naftol i 1,2-dihydro-naftalenodiol. Według INERIS naftalen może ulegać metylacji do 1-metylonaftalenu (prawdopodobnie mniej toksycznego niż naftalen) lub 2- metylonafatlen i jest wydalany głównie w postaci metabolitów z moczem.
Dzieci są bardziej wrażliwe na tę cząsteczkę. Osoby pochodzenia afrykańskiego i azjatyckiego są na nią bardziej podatne ze względu na częstszy niedobór enzymu G6PD.
Źródła narażenia organizmów żywych
- Produkty petrochemiczne ;
- pożary budynków;
- dym tytoniowy ;
- wydech z silnika spalinowego ;
- emisje z ogrzewania ;
- opary z plastyfikatorów ;
- emanacje żywic;
- opary z barwników ;
- opary z niektórych opakowań ;
- Opary z owadobójczych repelentów (np mole odstraszające );
- emisje z zanieczyszczonych gleb (czasami o wysokim poziomie);
- ...
Efekt zdrowotny
Inhalacja jest głównym źródłem narażenia zgodnie AFSSET który zauważył w 2010 roku, że ma tylko dane kilku ekspozycji (np 7% mieszkań 555 niemiecki studiował od 2003 do 2006 roku miał powietrze poziomy naftalenu przekroczenia limitu kwantyfikacji ( 1 mcg · m - 3 ), nie przekraczać 4,9 mcg · m -3 ).
- Naftalen jest klasyfikowany jako czynnik rakotwórczy kategorii 3 przez Unię Europejską, aw grupie 2B przez Międzynarodową Agencję Badań nad Rakiem (IARC). Zespół AFSSET nie znalazł informacji na temat zależności dawka-skutek i uważa, że „ dane dotyczące ludzi nie są wystarczające do ustalenia związku przyczynowego między narażeniem na naftalen a występowaniem raka ”, ale u „zwierząt częstość występowania gruczolaków nabłonka dróg oddechowych” a neuroblastoma nabłonka węchowego (bardzo rzadki guz) zwiększa się po ekspozycji na ten gaz, jednak dane te „ nie są takie, jakie są. przenoszone na ludzi ”.
- Zgodnie z doświadczeniami in vivo i in vitro naftalen nie jest genotoksyczny
Możliwe objawy;
- niedokrwistość , niezależnie od dróg narażenia (oraz z udokumentowanymi przypadkami niedokrwistości hemolitycznej prowadzącej do zgonu, z towarzyszącą żółtaczką u noworodka, w tym zakażonym w macicy, łożysko nie stanowi bariery dla tej cząsteczki)
- krwotoki,
- koagulat
- zaćma (narażenie zawodowe)
- nawet halucynacje.
Wartości progowe, wartość orientacyjna
Według AFSSET, przed 2010 rokiem nie było żadnych wartości referencyjnych (VG i VTR)
- Brak VG (wartość orientacyjna) lub TRV (toksykologiczna wartość odniesienia) dla naftalenu w przypadku ostrego narażenia;
- Brak danych toksykologicznych dla ludzi dotyczących narażenia pośredniego;
- wartość orientacyjną INDEKSU 10 μg · m -3 ustalono na podstawie progu drażniącego działania produktu na błony śluzowe nosa.
W Francji , to IAGVs dłuższą metę został ustawiony przez AFSSET (wartość na rok 2010, w wyniku samodzielnego skierowania 2004 2010) do: 10 mcg · m -3 dla ekspozycji powyżej roku
Uwagi i odniesienia
- (w) Hyp Daubensee J., Jr., James D. Wilson and John L. Laity, „ diamagnetic Susceptibility Exaltation in Hydrocarbons ” , Journal of the American Chemical Society , tom. 91 N O 8,9 kwietnia 1968, s. 1991-1998
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- " Naphthalene " , w Hazardous Substances Data Bank (dostęp: 17 marca 2010 ) .
- (w) Iwona Owczarek i Krystyna Błażej, „ Zalecane temperatury krytyczne. Część druga. Aromatic and Cyclic Hydrocarbons ” , J. Phys. Chem. Nr ref. Dane , vol. 33 N O 230 kwietnia 2004, s. 541 ( DOI 10.1063 / 1.1647147 )
- (w) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 II wyd. , 1076, s. ( ISBN 978-0-387-69002-5 i 0-387-69002-6 , czytaj online ) , str. 294
- (en) Robert H. Perry i Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , str. 2-50
- NAPHTALEN , karta (y) bezpieczeństwa Międzynarodowego Programu Bezpieczeństwa Substancji Chemicznych , konsultacja 9 maja 2009
- (w) David R. Lide , CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 s. , twarda oprawa ( ISBN 978-1-4200-9084-0 ) , s. 6-53
- (w) Carl L. Yaws , Handbook of Thermodynamic Diagrams: Organie Compounds C8 do C28 , vol. 3, Huston, Teksas, Gulf Pub. Współ.,1996, 396, str. ( ISBN 0-88415-859-4 )
- (w) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18 czerwca 2002, 83 th ed. , 2664 s. ( ISBN 0849304830 , prezentacja online ) , str. 5-89
- (en) R. B. Campbell , J. M. Robertson i J. Trotter , „ The crystal structure of hexacene, and a revision of the crystallographic data for tetracene ” , Acta Crystallographica , vol. 15 N O 5,Marzec 1962, s. 289-290
- (w) JG Speight i Norbert Adolph Lange , Lange's Handbook of Chemistry , McGraw-Hill,2005, 16 th ed. , 1623 s. ( ISBN 0-07-143220-5 ) , str. 2,289
- Grupa robocza IARC ds. Oceny ryzyka rakotwórczego dla ludzi, „ Evaluations Globales de la Carcinogenicité pour l'Homme, Groupe 2B: potencjalnie rakotwórcze dla ludzi ” , na http://monographs.iarc.fr , IARC,16 stycznia 2009(dostęp 22 sierpnia 2009 ) .
- Numer indeksu w tabeli 3.1 załącznika VI do rozporządzenia WE nr 1272/2008 (16 grudnia 2008)
- SIGMA-ALDRICH
- „ Naphthalene ” w bazie danych produktów chemicznych Reptox of the CSST (organizacja Quebec odpowiedzialna za bezpieczeństwo i higienę pracy), dostęp 25 kwietnia 2009
- " naftalen, " na hazmap.nlm.nih.gov (dostęp 14 listopada 2009 ) .
- Verschueren K. (1996) - Naphtalene. Podręcznik danych środowiskowych dotyczących chemikaliów organicznych. New York, Van Nostrand Reinhold Co. 3rd Ed, str. 1756-1762.
- Wolf O. (1976) - Nowotwory u pracowników chemicznych w byłej oczyszczalni naftalenu. Dt Gesundh Wesen, 31, 996–999
- Wolf O. (1978) - Rak krtani w oczyszczaczach naftalenu. Z Ges Hyg., 24, 737–739
- Artykuł Anne Gallus w „Le Monde” z 12 kwietnia 1998 r
- Źródło: INERIS, po ATSDR (1995) i HSDB (2000)
- Rippen G., Ilgenstein M., Klöpffer W. and Poremski H. (1982) - Screening of the adsorption Behavior of new chemical: natural soils and model adsorbents. Ecotoxicol Environ Saf, 6, 236
- Bouchard D. C., Mravik S. C. and Smith G. B. (1990) - Benzene and naphthalene sorption on soil contaminated with high molecular weight residual hydrocarbons from bezołowiowej benzyny. Chemosphere, 21, 975
- Løkke H. (1984) - Sorpcja wybranych zanieczyszczeń organicznych w glebach duńskich. Ecotox Toxicol Environ Saf, 8, 395.
- Veith G. D., De Foe D. L. i Bergstedt B. V. (1979) - Pomiar i oszacowanie czynników biokoncentracji chemikaliów w rybach. J Fish Res Board Can, 36, 1040-1048.
- Riley R. T., Mix M. C., Schaffer R. L. and Bunting D. L. (1981) - Uptake and accumulation of naphthalene by the oyster Ostrea edulis , in a flow-through system. Marine Biol, 61, 267-276
- Dane dotyczące biodegradacji i bioakumulacji istniejących chemikaliów na podstawie CSCL. Instytut Kontroli i Badań Chemikaliów. Japonia. (metoda OECD 302 C, ISIC, 1992)
- Delfino J. J. and Miles C. J. (1985) - Tlenowa i beztlenowa degradacja zanieczyszczeń organicznych w wodach podziemnych Florydy. Proc Soil Crop Sci Soc Fla, 44, 9–14.
- Nielsen P. H. and Christensen T. H. (1994) - Variability of biodegradation of aromatic hydrocarbons in aerobic aquifer specified by Laboratory Batch Experiments. J Contam Hydrol, 15, 305-320.
- Bauer J. E. and Capone D. G. (1985), Effects of four aromatic organic pollutants on microbial glycolism and thymidine incor- tion in marine sediments. Appl Environ Microbiol, 49, 828–835
- Delaune R. D., Hambrick G. A. and Patrick W. H. (1980) - Degradation of hydrocarbons in oksydowane i zredukowane sedymenty. Mar Pollut Bull, 11, 103–106
- „ Wielopierścieniowe węglowodory aromatyczne (WWA): ocena zależności dawka-odpowiedź w przypadku skutków rakotwórczych - podejście według substancji według substancji (współczynniki równoważności toksycznej - FET) i podejście oparte na mieszaninie; ocena zależności dawka-odpowiedź dla skutków nierakotwórczych: Toksykologiczne wartości odniesienia (TRV) »z INERIS ( patrz )
- Dawson J., Thayer W. i Desforges J. (1958) - Ostra niedokrwistość hemolityczna u noworodka z powodu zatrucia naftalenem : Raport dwóch 2 przypadków, wraz z badaniami mechanizmu choroby. Blood, 13, 1113-1125
- Tingle M., Pirmohmed M. and Templeton E. (1993) - Badanie tworzenia cytotoksycznych, genotoksycznych, reaktywnych i stabilnych metabolitów z naftalenu przez mikrosomy ludzkiej wątroby . Biochem Pharmacol, 46 (9), 1529–1538.
- Calabrese E. J. ( 1986 ) - Ekogenetyka: podstawy historyczne i stan obecny. J Occup Med, 28, 10, 1096–1102.
- /gesundheit/survey/publikationen/KUS-VOC-Innenraumluft-2008.pdf GerES (2008). Vergleichswerte für flüchtige organische Verbindungen (VOC und Aldehyde) in der Innenraumluft von Haushalten in Deutschland, Ergebnisse des repräsentativen Kinder-Umwelt- Surveys (KUS) des Umweltbundesamtes, Bundesgesundheitsblatteses - 11schundsschunds- 51schundsschunds
- OPINIĘ z Francuskiej Agencji Środowiska oraz bezpieczeństwem i higieną pracy odnoszące się do jakości powietrza w pomieszczeniach wartości przypomnienie propozycja dla naftalenu; samodzielne skierowanie Afsset (2004)]
- „ Referencyjna wartość toksykologiczna ” , w Anses - Krajowa Agencja ds. Bezpieczeństwa Żywności, Środowiska i Bezpieczeństwa Pracy ,październik 2014(dostęp w październiku 2014 )
- Wartość orientacyjna dla jakości powietrza w pomieszczeniach, zaproponowana w ramach projektu finansowanego przez Komisję Europejską











