Ksantotoksyna
| Ksantotoksyna | |
| Identyfikacja | |
|---|---|
| Nazwa IUPAC | 9-m "thoksy-7H-furo [3,2-g] chromen-7-on |
| Synonimy |
ksantotoksyna, metoksalen, 8-metoksypsoralen |
| N O CAS | |
| N O ECHA | 100,005,516 |
| N O WE | 206-066-9 |
| N O RTECS | LV1400000 |
| Kod ATC |
D05 D05 |
| DrugBank | DB00553 |
| PubChem | 3971 |
| UŚMIECHY |
COc1c2c (ccc (= O) o2) cc3c1occ3 , |
| InChI |
InChI: InChI = 1 / C12H8O4 / c1-14-12-10-8 (4-5-15-10) 6-7-2-3-9 (13) 16-11 (7) 12 / h2- 6H, 1H3 InChIKey: QXKHYNVANLEOEG-UHFFFAOYAV Std. InChI: InChI = 1S / C12H8O4 / c1-14-12-10-8 (4-5-15-10) 6-7-2-3-9 (13) 16-11 (7) 12 / h2- 6H, 1H3 Std. InChIKey: QXKHYNVANLEOEG-UHFFFAOYSA-N |
| Właściwości chemiczne | |
| Brute formula |
C 12 H 8 O 4 [Izomery] |
| Masa cząsteczkowa | 216,1895 ± 0,0114 g / mol C 66,67%, H 3,73%, O 29,6%, |
| Właściwości fizyczne | |
| T ° fuzja | Od 148 do 150 ° C |
| Rozpuszczalność | 47,6 mg · l -1 (woda, 30 ° C ) |
| Środki ostrożności | |
| SGH | |
  H302, H334, P261, P342 + P311,
H302 : Działa szkodliwie po połknięciu
H302, H334, P261, P342 + P311,
H302 : Działa szkodliwie po połknięciu H334 : Może powodować objawy alergii lub astmy lub trudności w oddychaniu w następstwie wdychania P261 : Unikać wdychania pyłu / dymu / gazu / mgły / par / rozpylonej cieczy. P342 + P311 : W przypadku wystąpienia objawów ze strony układu oddechowego: wezwać OŚRODEK ZATRUĆ lub lekarza. |
|
| Ekotoksykologia | |
| DL 50 |
423 mg · kg -1 (mysz, doustnie ) 860 mg · kg -1 (mysz, sc ) 250 mg · kg -1 (myszy, ip ) |
| LogP | 2.140 |
| Dane farmakokinetyczne | |
| Okres półtrwania eliminacji. | ~ 2 godziny |
| Jednostki SI i STP, chyba że określono inaczej. | |
Xanthotoxin lub metoksalen (sprzedawany pod nazwą Oxsoralène , Deltasoralène , Meladinine , UVADEX ) jest organiczny związek z rodziny furocoumarins . Jest to 8-metoksylowana pochodna psoralenu . Stosowany jest w leczeniu niektórych chorób skóry.
Występowanie naturalne
Ksantotoksyna występuje naturalnie w afrykańskiej roślinie leczniczej, fagarierze ( Fagara xanthoxyloïdes ), a także w wielu roślinach z rodziny baldaszkowatych , w szczególności w wysokiej ammi ( Ammi majus ), z której jest pozyskiwana, dzięgielu , pasternaku , Giant barszcz , albo z Rutaceae rodziny , takie jak bergamotki .
Biosynteza
Ksantotoksyna jest wytwarzana specyficzną drogą, drogą liniowych furokumaryn, która umożliwia tworzenie furokumaryn, takich jak psoralen i jego pochodne z umbeliferonu , który sam jest biosyntetyzowany na drodze fenylopropanoidowej , oraz z pirofosforanu dimetyloallilu , otrzymywanego z mewalonianu .
Synteza umbelliferonu
Umbelliferon jest kumaryną , jedną z wielu podrodzin fenylopropanoidów , a zatem jest biosyntetyzowany, podobnie jak ten ostatni, z L-fenyloalaniny zgodnie ze szlakiem fenylopropanoidów (lub szlakiem szikimatu ). Fenyloalanina jest najpierw przekształcana w kwas cynamonowy przez działanie liazy amoniakalnej fenyloalaniny (PAL), która jest następnie hydroksylowana do kwasu parakumarowego przez działanie 4-hydroksylazy cynamonowej (C4H). Ten ostatni jest ponownie hydroksylowany przez działanie 2-hydroksylazy cynamonianowej / kumaranowej (C2H) z wytworzeniem kwasu 2,4-dihydroksycynamonowego , a następnie przez obrót nienasyconego wiązania sąsiadującego z grupą karboksylową tego ostatniego. Reakcja kończy się wewnątrzcząsteczkową estryfikacją , w której grupa hydroksylowa C2 'jest atakowana przez grupę karboksylową, tworząc pierścień laktonowy .
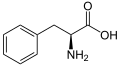
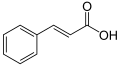


Synteza ksantotoksyny
Następnie biosynteza przebiega dalej poprzez aktywację pirofosforanu dimetyloallilu (DMAPP), wytwarzanego na szlaku mewalonianu, tworząc karbokation przez rozszczepienie difosforanu. Po aktywacji, enzym 6-prenylotransferaza umbeliferonu katalizuje C-alkilację pomiędzy DMAPP i umbelliferonem do pozycji aktywowanej, orto do fenolu, prowadząc do powstania demetylosuberozyny. Po tej reakcji następuje hydroksylacja katalizowana przez enzym syntazę marmezyny tworzącą marmesynę , po której następuje druga hydroksylacja z odejściem acetonu katalizowana przez syntazę psoralenu tworzącą psoralen . Psoralen jest następnie przekształcany przez działanie 8-monooksygenazy psoralenu tworzącej ksantotoksol . Ten ostatni widzi metylację swojej grupy fenolowej w reakcji z S-adenozylometioniną , reakcji katalizowanej przez O-metylotransferazę ksantotoksolu tworzącą ksantotoksynę.
Leczenie chorób skóry
Ze względu na swoje właściwości fotouczulające skóry (które dzieli z innymi furokumarynami) ksantotoksyna jest stosowana wraz z ekspozycją skóry na słońce jako lek w leczeniu chorób skóry, takich jak łuszczyca , egzema czy bielactwo nabyte oraz przeciw niektóre chłoniaki skóry. Ksantotoksyna zmienia sposób, w jaki komórki skóry otrzymują promieniowanie UV-A , co tłumi chorobę. Na ogół przepisuje się dawkę 10 mg ksantotoksyny przed leczeniem PUVA ( psoralen + UV-A) w dawce 30 mg / 75 minut.
Ryzyka
Osoby z wysokim ciśnieniem krwi lub chorobami wątroby w wywiadzie są narażone na zapalenie i nieodwracalne uszkodzenie wątroby i skóry. Efekty uboczne obejmują nudności , bóle głowy , zawroty głowy , aw rzadkich przypadkach bezsenność .
Ksantotoksyna jest toksyczna dla zwierząt zimnokrwistych .
Uwagi i odniesienia
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- Arkusz Sigma Aldrich , przeglądany 15 czerwca 2011 r
- (in) „ Xanthotoxin ” on ChemIDplus , dostęp 15 czerwca 2011
- Toksykologia lekowa i chemiczna. Lot. 2, str. 309, 1979
- Narkotyki w Japonii, tom. 6, str. 837, 1982
- Alfa Aesar 15 czerwca 2011 r. , Konsultowano
- liniowa biosynteza furanokumaryny
- PM Dewick , Naturalne produkty lecznicze: podejście biosyntetyczne , John Wiley & Sons ,2009, 3 e ed. , s. 161, 164-165
- (fr) Ten artykuł jest częściowo lub w całości zaczerpnięty z artykułu z angielskiej Wikipedii zatytułowanego „ Methoxsalen ” ( zobacz listę autorów ) .



