Chlorek glinu
| chlorek glinu (III) | |||||
  
|
|||||
| Identyfikacja | |||||
|---|---|---|---|---|---|
| Nazwa IUPAC | trichloroaluman | ||||
| Synonimy |
trichlorek glinu |
||||
| N O CAS | |||||
| N O ECHA | 100,028,371 | ||||
| N O WE | 231-208-1 | ||||
| N O RTECS | BD0525000 | ||||
| Kod ATC | D10 | ||||
| PubChem | 24012 | ||||
| InChI |
InChIKey: VSCWAEJMTAWNJL-UHFFFAOYSA-K |
||||
| Wygląd | bladożółte ciało stałe | ||||
| Właściwości chemiczne | |||||
| Brute formula |
Al Cl 3 [Izomery] |
||||
| Masa cząsteczkowa | 133,341 ± 0,006 g / mol Al 20,23%, Cl 79,76%, |
||||
| Właściwości fizyczne | |||||
| T ° fuzja | 463 K ( 190 ° C ) przy ciśnieniu 2,5 atm |
||||
| * Temperatura wrzenia | 182,7 ° C przy 752 mmHg (sublimacja) | ||||
| Rozpuszczalność | w wodzie : 439 g · l -1 ( 0 ° C ), 449 g · l -1 ( 10 ° C ), 458 g · l -1 ( 20 ° C ) 466 g · l -1 ( 30 ° C ) 473 g · l -1 ( 40 ° C ) 481 g · l -1 ( 60 ° C ) 486 g · l -1 ( 80 ° C ) 490 g · l -1 ( 100 ° C ). etanol : 1000 g · l -1 ( 12,5 ° C ). chloroform : 0,7 g · l -1 ( 20 ° C ). CCl 4 : rozpuszczalny. eter : rozpuszczalny |
||||
| Masa objętościowa | 2,44 do 2,48 g / cm 3 | ||||
| Punkt krytyczny | 26,3 bar , 346,85 ° C | ||||
| Krystalografia | |||||
| System kryształów | Jednoskośny | ||||
| Sieć Bravais | mC | ||||
| Symbol Pearsona | |||||
| Klasa kryształu lub grupa kosmiczna | C2 / m ( N O 12) | ||||
| Strukturbericht | D0 15 | ||||
| Środki ostrożności | |||||
| SGH | |||||
 Niebezpieczeństwo H314, H314 : Powoduje poważne oparzenia skóry i uszkodzenia oczu |
|||||
| NFPA 704 | |||||
| 0 3 2 W. | |||||
| Transport | |||||
80 : substancja żrąca lub substancja o niewielkim stopniu korozyjności Numer UN : 1726 : BEZWODNY CHLOREK ALUMINIUM Klasa: 8 Kod klasyfikacyjny: C2 : Substancje żrące bez ryzyka dodatkowego; Substancje kwasowe: nieorganiczne, stałe; Etykieta: 8 : Substancje żrące Pakowanie: Grupa pakowania II : substancje średnio niebezpieczne; 
80 : substancja żrąca lub substancja wykazująca niewielki stopień korozyjności Numer UN : 2581 : CHLOREK ALUMINIUM W ROZTWORZE Klasa: 8 Kod klasyfikacyjny: C1 : Substancje żrące bez ryzyka dodatkowego; Substancje kwasowe: nieorganiczne, ciekłe; Etykieta: 8 : Substancje żrące Pakowanie: Grupa pakowania III : substancje niskiego zagrożenia.  |
|||||
| Ekotoksykologia | |||||
| DL 50 | 3450 mg · kg -1 | ||||
| Jednostki SI i STP, chyba że określono inaczej. | |||||
Chlorek glinu (AlCl 3 ), znane również jako trichlorek glinu albo chlorku glinu (III) jest sól z aluminium i chloru . Bezwodna postać ma szczególną strukturę: mimo, że jest halogenek o bardzo elektrododatni metalu , to wiązania chemiczne są głównie kowalencyjne i nie jonowe , jak można by się spodziewać. Konsekwencją tego jest to, że AlCl 3 ma niską temperaturę topnienia i temperaturę sublimacji ( 178 ° C, do drugiego), a w ciekłym stanie , to przewodzi elektryczność słabo, w przeciwieństwie do jonowego halogenkami takimi jak chlor. Sodu . Związek ten istnieje w stanie stałym w postaci sieci sześcio-współrzędnych. Że topi się , tworząc tetracoordinated dimer, Al 2 Cl 6, który może parować , ale który dysocjuje w podwyższonej temperaturze z wytworzeniem AlCl 3 gatunków typu BF 3 .
Chlorek glinu jest bardzo rozpuszczalny i może eksplodować w kontakcie z wodą pod wpływem hydratacji . Jest częściowo hydrolizuje się w obecności wody na postać roztworu chlorowodoru ( kwasu solnego ). W roztworze wodnym AlCl 3 jest całkowicie zjonizowany, a roztwór dobrze przewodzi prąd elektryczny . Ten roztwór jest kwaśny . W uproszczeniu kation powstały w wyniku reakcji chlorku glinu z wodą zapisujemy:
AlCl 3 jest prawdopodobnie najpowszechniej stosowanym i silnym kwasem Lewisa . Związek ten ma wiele zastosowań w chemicznej przemysłu , w szczególności jako katalizator dla Friedela i Craftsa reakcji , zarówno alkilowanie i acylowanie . Jest on również stosowany do reakcji polimeryzacji i izomeryzacji w związkach organicznych .
Istnieje również chlorek glinu (I) (AlCl), ale jest on bardzo niestabilny i znany jest tylko w stanie gazowym .
Właściwości fizykochemiczne
W stanie stałym chlorek glinu krystalizuje zgodnie ze strukturą typu YCl 3 , z jonami Al 3+ tworzącymi regularną sieć centrowaną na powierzchni.
Chlorek glinu jest silnym kwasem Lewisa , zdolnym do reagowania zgodnie z reakcjami kwas-zasada Lewisa nawet ze słabymi zasadami Lewisa, takimi jak benzofenon lub mezytylen . W obecności jonu chlorkowego reaguje tworząc AlCl 4 - .
Hydrolizy częściowo w obecności wody , jak chlorowodór i / lub kwas solny . Wodne roztwory chlorku glinu zachowują się analogicznie do roztworów innych soli zawierających uwodnione jony Al 3+ . Np. Umieszczony w obecności odpowiedniej ilości sody tworzy galaretowaty osad wodorotlenku glinu :
AlCl 3 (aq) + 3 NaOH (aq) → Al (OH) 3 (s) + 3 NaCl (aq)
Struktura krystaliczna
W stanie stałym chlorek glinu krystalizuje w strukturze jednoskośnej , takiej jak RhCl 3 , grupy przestrzennej C 2 / m. Jego parametry siatki to a = 5,914 A , b = 10,234 A ic = 6,148 A przy β = 108,25 ° . W siatce aluminium zajmuje pozycję Wyckoffa 4g (y = 0,166), a chlor w pozycjach 4i (x = 0,215 iz = 0,226) i 8j (x = 0,252, y = 0,321, z = 0,225). Uzyskana struktura jest strukturą z arkuszy w płaszczyźnie (a, c), aluminium jest umieszczone w środku ośmiościanów aluminium, aw płaszczyźnie o strukturze plastra miodu (a, b).
Przygotowanie
Chlorek glinu jest produkowany przemysłowo w wyniku bezpośredniej reakcji pierwiastków glinu i chloru :
2 Al + 3 Cl 2 → 2 AlCl 3Lub z glinu i kwasu solnego :
2 Al + 6 HCl → 2 AlCl 3 + 3 H 2Ta reakcja jest egzotermiczna.
Używa
- Główne zastosowanie chlorku glinu dotyczy wytwarzania związków w reakcji Friedela i Craftsa, których jest on katalizatorem , np. Produkcja antrachinonu (dla przemysłu farbiarskiego ) z benzenu i fosgenu . Podczas reakcji Friedela i Craftsa chlorek acylu lub halogenek alkilu reaguje z następującym związkiem aromatycznym :
W przypadku pochodnych benzenu głównym produktem reakcji jest izomer para. Ponieważ reakcja alkilowania stwarza wiele problemów, jest mniej rozpowszechniona niż reakcja acylowania. W obu przypadkach chlorek glinu (lub zastosowana aparatura) nie może być całkowicie bezwodny, ponieważ do przeprowadzenia reakcji konieczne są ślady wilgoci. Jednym z problemów związanych z reakcją Friedela i Craftsa jest to, że katalizator (chlorek glinu) musi być obecny w ilości stechiometrycznej, aby reakcja była zakończona, ponieważ tworzy trwały kompleks z produktem. Ta cecha sprawia, że recykling jest bardzo trudny , dlatego po użyciu muszą zostać zniszczone, co powoduje powstanie dużej ilości żrących ścieków. Z tego powodu chemicy badają możliwość zastosowania bardziej obojętnych dla środowiska katalizatorów, takich jak trifluorometanosulfonian iterbu (III) lub trifluorometanosulfonian dysprozu (III), które są droższe, ale można je poddać recyklingowi.
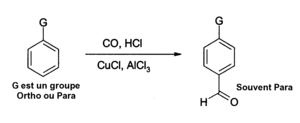
- Chlorek glinu można również stosować w funkcjach reakcji insercji aldehydów w pierścieniu aromatycznym , na przykład w wyniku reakcji Gattermana-Kocha, w której wykorzystuje się tlenek węgla , chlorowodór i chlorek miedzi (I) jako kokatalizator:
- Chlorek glinu ma wiele innych zastosowań w chemii organicznej :
- AlCl 3 stosuje się w reakcji na polimeryzacji lub izomeryzacji w związkach organicznych . Ważnymi zastosowaniami są produkcja etylobenzenu (używanego do produkcji styrenu, a następnie polistyrenu ) oraz produkcja dodecylobenzenu (używanego do produkcji detergentów );
- AlCl 3 katalizuje w szczególności w reakcji Dielsa-Aldera ;
- AlCl 3 również katalizuje dodanie 3-buten-2-onu do karwonu :
- Wreszcie jest to nieorganiczny koagulant, szeroko stosowany w niektórych procesach oczyszczania wody, w postaci polichlorku glinu (PAC). W tym kontekście może również usuwać nadmiar fluoru z wody. Aby uniknąć zanieczyszczenia wody pitnej aluminium i zapewnić dobrą koagulację, należy dobrze kontrolować pH procesu koagulacji, a także stosowane dawki. Mieszanie wody musi być odpowiednie, podobnie jak system filtracji (który musi usuwać aglomeraty glinu). Chitozan i bentonitu użyteczne dodatki.
bezpieczeństwo
AlCl 3 może spowodować wybuch w przypadku kontaktu z zasadą lub wodą . Jest to odczynnik, z którym należy obchodzić się ostrożnie, używając rękawic i okularów ochronnych. Należy go obsługiwać pod wyciągiem. W wilgotnym powietrzu chlorek glinu szybko wchłania wilgoć, stając się silnie kwaśnym i szybko atakuje różne materiały, w tym stal nierdzewną i gumę .
Sześciowodzian chlorku glinu
Wzór chemiczny: AlCl 3 (H 2 O) 6
Ten stabilny produkt nie jest agresywny dla skóry; wchodzi nawet w skład miejscowych preparatów skórnych w dermatologii (patrz nadmierna potliwość ).
Główne synonimy:
- Nazwa francuska = heksahydrat trichlorku glinu,
- Angielska nazwa = sześciowodny trójchlorek glinu.
Zobacz też
- Polichlorek glinu
Bibliografia
- NN Greenwood, A. Earnshaw, Chemistry of the Elements , Pergamon Press, Oxford, Wielka Brytania, 1984.
- Handbook of Chemistry and Physics , 71 wydanie, CRC Press, Ann Arbor, Michigan, 1990.
- GA Olah (red.), Friedel-Crafts and Related Reactions , tom. 1, Interscience, Nowy Jork, 1963.
- LG Wade, Organic Chemistry , 5th edition, Prentice Hall, Upper Saddle River, New Jersey, USA, 2003.
- P. Galatsis, w: Handbook of Reagents for Organie Synthesis: Acidic and Basic Reagents , (HJ Reich, JH Rigby, red.), P. 12-15 , Wiley, Nowy Jork, 1999.
- BB Snider, Accounts of Chemical Research 13 , 426 (1980).
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- PubChem
- „ Properties of Various Gases ” na stronie flexwareinc.com (dostęp 12 kwietnia 2010 )
- " The AlCl3 (D015) Structure " , na http://cst-www.nrl.navy.mil/ (dostęp 17 grudnia 2009 )
- Numer indeksowy w tabeli 3.1 załącznika VI do rozporządzenia WE n O 1272/2008 (16 grudnia 2008)
- SI Troyanov, Zhurnal Neorganicheskoi Khimii 37 , 266 (1992)
- Sohrabi Y Shokoohizadeh MJ Tabar FR, Mirzaei N Bagheri A Ghadiri SK, ... i Charganeh SS (2018) Przyglądając się wykorzystanie chlorku glinu w uzdatnianiu wody . Zaawansowane badania naukowe ( streszczenie ).