Flawan-3-ol
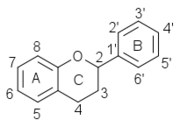
W flawan-3-oli i flawanole lub katechiny stanowią podrodzinę flawonoidów , których konstrukcja oparta jest na 2-fenylo-3-chromanol.
Flav zawiera fenole nie powinny być mylone z flav ö fenoli , które zawiera ponadto w pozycji 4 grupę karbonylową C = O.
Struktury oligomeryczne i polimerowe flawanoli stanowią klasę proantocyjanidoli lub garbników skondensowanych.
Definicja
|

|
|
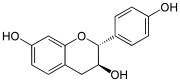
| Flawonoidy ponumerowały szkielet | (+) - katechina | guibourtinol |
Flawanole są scharakteryzowane w klasie flawanoidów przez ich centralny heterocykl C zawierający tylko jedną substytucję w 3 przez grupę hydroksylową OH. Są one zanikane w szeregu związków po podstawieniu przez fenolowe grupy hydroksylowe w pierścieniach A i B. Te grupy hydroksylowe mogą być wolne lub eteryfikowane lub być zaangażowane w wiązania heterozydowe . Wszystkie związki mają 4 stereomery ze względu na obecność asymetrycznych 2 i 3 węgli (z 4 różnymi podstawnikami).
Najliczniejszą klasę w przyrodzie stanowią katechiny lub katechiny i ich pochodne, które zawierają hydroksylowe grupy OH w pozycjach 5 i 7 na pierścieniu A oraz 4 'i 5' na pierścieniu B. Katechina występuje w 4 formach stereoizomerycznych ze względu na obecność węgle asymetryczne 2 i 3.
Termin katechina jest niejednoznaczny:
- może oznaczać związek (+) - katechinę lub (-) - katechinę
- klasa flawanoli pochodzących od katechiny i jej zestryfikowanych pochodnych.
Istnieją również związki, takie jak guibourtinidol, które mają tylko jeden hydroksyl na każdym pierścieniu A i B. Znajduje się on w Cassia abbreviata .
Cztery stereoizomeryczne formy katechiny
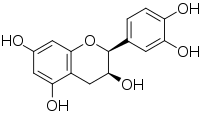
Katechina występuje w postaci kilku stereoizomerów pochodzących z dwóch asymetrycznych atomów węgla. Formy enancjomeryczne (w odbiciu lustrzanym) w pozycjach 2 i 3 centralnego heterocyklu, zwane konfiguracją R / S, dają następujące cztery struktury:
| Struktury enancjomerów katechiny / epikatechiny | ||
| Nazwisko | Konfiguracja | Formuła |
|---|---|---|
| (+) - katechina | 2R, 3S |

|
| (-) - epikatechina | 2R, 3R |

|
| (-) - katechina | 2S, 3R |

|
| (+) - epikatechina | 2S, 3S |
|
W naturze najpowszechniejszymi izomerami są (+) - katechina i (-) - epikatechina. Pozostałe dwa stereoizomery są znacznie rzadsze, a ich obecność wydaje się być związana z reakcjami enzymatycznymi lub obróbką cieplną.
Niektóre powszechne katechiny
Typowe katechiny herbaty i wina z konfiguracją a -cis w pozycjach 2, 3:
| 2,3- cis struktury katechinowe | |||
| Związki | R3 | R5 ” | Struktury |
|---|---|---|---|
| (-) - epikatechina EC | O | H. |

|
| (-) - epigallokatechina EGC | O | O | |
| (-) - EKG galusanu epikatechiny | sol | H. | |
| (-) - galusan epigallokatechiny EGCG | sol | O | |
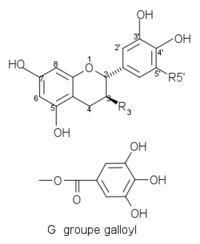
Niektóre typowe katechiny z konfiguracją a -trans na pozycjach 2, 3:
| Struktury 2,3- trans katechiny | |||
| Związki | R3 | R5 ” | Struktury |
|---|---|---|---|
| (+) - katechina C | O | H. |
|
| (+) - galokatechina GC | O | O | |
| (+) - galusan galokatechiny GCG | sol | O | |
Te skondensowane taniny są oligomery lub polimery pochodzące z monomerów flawanoli. Zatem procyjanidole są zbudowane na katecholu / epikatecholu, a prodelfinidole na gallokatecholu / epigallokatecholu.
Inne flawanole
| Flawan-3-ols | |||
| Obrazek | Nazwisko | Formuła | Oligomer |
|---|---|---|---|

|
Afzelechol , Epiafzelechol |
C15H14O5 | Propelargonidyny |
|
|
Fisetinidol Epifisetinidol |
C15H14O5 | Profisetynydyny |
|
|
Guibourtinidol Epiguibourtinidol |
C15H14O4 | Proguibourtynidyny |

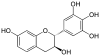
|
Mesquitol Epimesquitol |
C15H14O6 | Promelacinidins i Proteracinidins |
|
Robinetinidol Epirobinetidol |
C15H14O6 | Prorobinetynydyny |
Rośliny bogate we flawanole
- roślin herbaty ( Camellia sinensis ), flawonoidy w liściach herbaty są utworzone w 80% flawanole, czyli (+) - katechiny C, (-) - epikatechina WE (+) - gallokatechiny GC i ich estry galusowy
| Przeciętny skład świeżych liści herbaty we flawanolach | |
| Flawanole | Wyniki wg / kg sm |
|---|---|
| (-) - galusan epigallokatechiny EGCG | 90-130 |
| (-) - epigallokatechina EGC | 30-60 |
| (-) - EKG galusanu epikatechiny | 30-60 |
| (+) - galokatechina GC | 30-40 |
| (-) - epikatechina EC | 10-30 |
| (+) - katechina C | 10-20 |
W herbata zielona, oolong i czarnej jest zróżnicowana w zależności od znaczenia enzymatycznej poddawany jest procesowi utleniania przez liście, gdy niewłaściwie proces zwany „fermentacja”. Flawonoidy w zielonej herbacie, podobnie jak te w świeżych liściach, to 80% flawanoli, ale po utlenieniu tylko 20 do 30% pozostaje w czarnej herbacie.
Skład flawanolu w herbatach znajdujących się w handlu różni się znacznie w zależności od różnych parametrów związanych z uprawą krzewów herbacianych, a następnie z procesem produkcyjnym. Oto kilka wartości zaczerpniętych od Chen i współpracowników dla zielonej herbaty z Chin oraz od Kurody i Hary dla czarnej herbaty z Darjeeling.
|
Skład herbat nadających się do sprzedaży we flawanolach (wyniki wg / kg sm) | |||||
| Flawanole | Zielona herbata | Czarna herbata | |||
|---|---|---|---|---|---|
| Maxi | Mini | Średni | |||
| EGCG | 106.2 | 58,67 | 93.03 | 40.2 | |
| EGC | 47,94 | 28.13 | 33,59 | . | |
| EKG | 40,60 | 13,37 | 34,68 | 39.20 | |
| WE | 13.38 | 7.20 | 9,79 | 6.7 | |
| Całkowity | 171.09 | 86.10 | |||
.
Zaparzając 20 g zielonej herbaty w litrze wody o temperaturze 90 ° C przez 5 minut, uzyskuje się następujący skład flawanolu:
|
Skład flawanolu w naparze z zielonej herbaty (wyniki w mg / l) | |||||
| EGCG | EGC | EKG | WE | VS | Całkowity |
| 489,6 | 705,9 | 48.1 | 84.9 | 7.8 | 1336,3 |
W tych optymalnych warunkach filiżanka zielonej herbaty o pojemności 150 ml zawiera zatem około 200 mg flawanoli. W przypadku Rains i in. (2011), typowa filiżanka zielonej herbaty (250 ml) zawiera 50-100 mg katechin (lub 30-60 mg na 150 ml) i 30-40 mg kofeiny. Jednak ze względu na wiele parametrów zmienności, od kultury, czasu zbioru, produkcji po infuzję, według autorów wartości te są bardzo różne. Bronner i Beecher stwierdzają znacznie niższe wartości, zaparzając 3 g liści przez 3 minuty w litrze wrzącej wody, szacują, że filiżanka (150 ml) zielonej herbaty zawiera 18 mg flawanoli, a filiżanka czarnej herbaty zawiera 49,5 mg .
W przypadku czarnej herbaty Arts i wsp. Szacują, że kubek o pojemności 150 ml zawiera 20 mg flawanoli (monomerów).
- winorośli ( Vitis vinifera ) winogron jest bogaty w (+) - katechiny, (-) - epikatechiny i jego ester galusowy, epikatechiny, 3-galusan. Te flawanole są skoncentrowane w nasionach w różnych dawkach w zależności od odmiany winogron, gleby, rocznika i dojrzałości fenolowej. Wysokie stężenia znajdują się w pestkach winogron Merlot i Cabernet Sauvignon:
|
Skład pestek winogron we flawanolach zebranych w Toskanii (Włochy) Wyniki w mg / kg sm | ||
| Odmiany winogron | (+) - Katechina | (-) - Epikatechina |
|---|---|---|
| Merlot | 1388 | 1318 |
| Cabernet Sauvignon | 1418 | 1276 |
Podczas winiarstwa różne techniki maceracji pozwalają na wydobycie większej lub mniejszej ilości flawonoidów ze skórki i nasion. Dlatego te związki znajdują się w winach czerwonych w wciąż dość wysokich stężeniach:
|
Średni skład win czerwonych we flawanolach Wyniki w mg / l | |||
| Flawanole | Maxi | Mini | Średni |
|---|---|---|---|
| (+) - katechina | 300 | 20 | 130 |
| (-) - epikatechina | 120 | 5 | 60 |
| (+) - galokatechina | 80 | 7 | 35 |
| (-) - epigallokatechina | 35 | 2 | 13 |
To znaczy średnio łącznie 238 mg · l -1 flawanoli, co daje szklankę 12 cl o wartości 28,5 mg .
- kakaowca ( Theobroma cacao ) ziarna kakaowego zawiera od 12 do 18% polifenoli (w% suchej masy) z około 35% z nich w postaci chlorowodorku (-) - epikatechina (z niefermentowanego Forastero fasola ). Aby stać się kakao, ziarna muszą przejść fermentację, suszenie i prażenie. Podczas tych licznych operacji większość katechin i procyjanidoli przekształca się w chinony . W kakao jednak w większości wśród polifenoli pozostają flawanole, przy czym najpierw (-) - epikatechina, następnie (+) - katechina, (+) - galokatechina i (-) - epigalokatechina oraz proantocyjanidole składające się z 2 lub 3 jednostek (+) - katecholu i / lub (-) - epikatechiny, czyli procyjanidoli B1, B2, B3, B4, B5, C1 i D.Wysokie temperatury prażenia przekształcają część (-) - epikatechiny w jej epimer (-) - katechina. Handlowe kakao z Wybrzeża Kości Słoniowej zawiera od 2,2 do 4,8 g · kg -1 epikatechiny.
Katechiny znajdują się w czekoladzie , w ilości 53,5 mg / 100 gw ciemnej czekoladzie i 15,9 mg / 100 gw białej czekoladzie.
Aby zorientować się w rzędzie wielkości, możemy powiedzieć, że 4 kwadraty ciemnej czekolady (40 g ), filiżanka herbaty i kieliszek czerwonego wina dostarczają mniej więcej taką samą ilość flawanoli.
- te ziarna są bogate w katechiny, ale nie fasoli lub kapusty. Wiele owoców jest również bogatych w katechiny: najpierw jeżyny , oczywiście winogrona , potem wiśnie , morele , maliny , jabłka , śliwki , truskawki , gruszki i brzoskwinie :
|
Skład flawanoli z owoców i warzyw, surowych (wyniki w mg / kg świeżej masy) | |||
| (-) - epikatechina | (+) - katechina | Całkowity | |
|---|---|---|---|
| Bób (Vicia faba), surowe nasiona | 225,1 | 128,3 | 353,4 |
| Jeżyna (Rubus sp.) | 180,8 | 6.6 | 187,4 |
| Czarny Grappe | 86.4 | 89.4 | 175,8 |
| wiśnia | 95.3 | 21.7 | 117,0 |
| Morela | 60.6 | 49.5 | 110.1 |
| Malina | 82.6 | 9.7 | 92.3 |
| Jabłko ze skórką | 81.4 | 9.5 | 90.9 |
| Śliwka | 28.4 | 33.5 | 61.9 |
| Truskawki | 0 | 44.7 | 44.7 |
Wchłanianie i biodostępność katechin
Po spożyciu herbaty, wina czy czekolady katechiny tych produktów ulegają znacznym przemianom w układzie pokarmowym. Większość z nich jest metabolizowana przez bakterie jelitowe i enterocyty . Po przejściu przez ścianę jelita katechina i epikatechina znajdują się w 45% w postaci glukuronidowej, 30% w postaci o-metylowanej i 20% w postaci o-metyloglukuronidowanej (zgodnie z badaniami na gradzie szczura w jelicie z Kuhnle i in.). Wiadomo również, że u ludzi tylko 1,68% spożytej katechiny znajduje się w osoczu krwi, moczu i kale. EGCG prawie nie przedostaje się do krwi, a wchłonięta część jest wydalana głównie z żółcią w okrężnicy. EGC i EC są nieco bardziej biodostępne. Niemniej jednak EGC jest wykrywany głównie w postaci glukuronidowanej (57-71%) lub siarczanowanej (23-36%), a tylko niewielka część znajduje się w stanie wolnym (3-13%). 2/3 EC jest wykrywane w postaci siarczanowanej i 1/3 glukuronidowanej.
Metabolity pojawiają się w krwiobiegu dość szybko, ponieważ maksymalne stężenie obserwuje się 2,5 godziny po spożyciu pokarmu bogatego we flawanol. Następnie są szybko wydalane z żółcią i moczem.
Działalność biologiczna
Działania przeciwutleniające
Nadmierna produkcja wolnych rodników w organizmie może spowodować znaczne uszkodzenie makrocząsteczek i komórek w tym organizmie. Degradacja lipidów pod wpływem stresu oksydacyjnego powoduje odkładanie się utlenionych lipidów w naczyniach powodując powstawanie blaszek miażdżycowych , zaburza funkcjonowanie błon komórkowych i generuje rakotwórcze pochodne.
Katechiny, podobnie jak wszystkie polifenole, posiadają fenolowe grupy hydroksylowe Ar-OH, które mogą dostarczać H rodnikom nadtlenowym L-OO • i tym samym neutralizować je w postaci wodorotlenków L-OOH:
Ar-OH + L-OO • → Ar-O • + L-OOH
Rodnik Ar-O • jest dość stabilny i mniej reaktywny, przerywa łańcuch.
Ponieważ nie ma absolutnej miary do oceny potencjału przeciwutleniającego związku, należy zastosować oceny porównawcze z innymi związkami. Ponadto porównania te będą zależeć od metody oceny, a zwłaszcza od zastosowanego wolnego rodnika nadtlenkowego.
- Porównując zdolność in vitro do wychwytywania wolnych rodników DPPH • (2,2-difenylo 1-pikrylhydrazyl) przez katechiny, Nanjo i wsp. Wykazali, że nie ma znaczącej różnicy między (+) - C, (-) - EC, (-) - EGC, (-) - EGCG iz drugiej strony ich odpowiednie epimery la (+) - EC, (-) - C, (-) - GC, (-) - CG, (-) - GCG. Zatem zdolność wychwytywania katechin nie zależy od ich stereoizomerii. Z drugiej strony galoilowane pochodne katechin są silniejszymi zmiataczami niż nie-stopowe. W ten sposób uzyskuje się następującą malejącą kolejność aktywności przeciwutleniającej:
- Chociaż siła przeciwutleniająca flawanoli jest dobrze potwierdzona w badaniach in vitro , nie jest taka sama in vivo ze względu na ich niską biodostępność . Badania in vivo koncentrowały się na napojach lub żywności bogatej we flawanole, ale zawierającej także inne polifenole i witaminy, które również posiadają bardzo silny potencjał antyoksydacyjny.
Istnieje pół tuzina metod oceny potencjału antyoksydacyjnego osocza krwi po spożyciu pokarmów bogatych we flawonoidy. Wiele badań wykazało, że istnieje znacząca korelacja pomiędzy zmierzonym potencjałem przeciwutleniającym a całkowitą zawartością polifenoli w badanym produkcie spożywczym, chociaż osocze może zawierać znaczne stężenia przeciwutleniaczy witamin (witamin C i E) oraz moczu, co wiąże się z bardzo niskim stężeniem flawonoidów.
W kilku badaniach oceniano zdolność przeciwutleniającą osocza osobników przed i po spożyciu herbaty i we wszystkich zaobserwowano znaczny wzrost zdolności przeciwutleniającej osocza w około godzinę po spożyciu (z korzyścią dla zielonej herbaty).
Podobne obserwacje in vivo przeprowadzono dla wina i czekolady. Wszystkie badania potwierdzają znaczny wzrost zdolności antyoksydacyjnej osocza po około godzinie od spożycia czerwonego wina.
Po spożyciu czekolady stężenie (-) - epikatechiny w osoczu gwałtownie wzrasta, osiągając maksimum po 2 godzinach, a następnie powoli spada. Po regularnym spożywaniu czekolady przez długi czas zaobserwowano lepszą odporność cząsteczek LDL na stres oksydacyjny oraz wzrost całkowitej zdolności antyoksydacyjnej serum. Z drugiej strony, tego samego rodzaju badania dotyczące regularnego spożywania herbaty czy wina przez długi czas nie przyniosły spójnych rezultatów.
Niedawne odkrycie w analizie osocza po spożyciu produktów bogatych we flawonoidy rzuciło światło na rozbieżności, które mogą czasami pojawiać się między pomiarami in vitro i in vivo . Lolito i wsp. Zaobserwowali zaskakujące pojawienie się szczytu stężenia kwasu moczowego w osoczu krwi (po spożyciu jabłek) dokładnie po szczycie zdolności antyoksydacyjnej osocza. Kwas moczowy jest przeciwutleniaczem, którego nie ma w jabłkach, ale którego pojawienie się we krwi wynikałoby ze spożycia fruktozy zawartej w jabłkach. Rola moczanu została potwierdzona przez badanie Moduna i wsp. Na czerwonym winie. Poprzez sukcesywne spożywanie czerwonego wina, czerwonego wina bezalkoholowego, czerwonego wina pozbawionego polifenoli, etanolu i wody, autorzy ci byli w stanie jasno ustalić, że wzrost zdolności antyoksydacyjnej osocza można wytłumaczyć zarówno szczytem cetachin (i polifenoli). ) w osoczu i szczytowe stężenie moczanów.
..............
Cząsteczki te pozwalają również na zahamowanie kiełkowania nasion podczas rywalizacji między roślinami, co powoduje zmniejszenie rekrutacji gatunków sąsiednich, a tym samym wpływa na dynamikę populacji, z którymi konkurują.
Badanie przeprowadzone w listopadzie 2020 roku przez University of North Carolina sugeruje, że określone polifenole (flawanole i proantocyjanidyny ) zawarte w Vitis rotundifolia (muskadyna winogronowa), zielonej herbacie , kakao i ciemnej czekoladzie mogą wpływać na zdolność wiązania wirusa SARS-CoV-2 do komórek ludzkich, zmniejszając wskaźniki infekcji i przenoszenia wirusa, który powoduje Covid-19 .
Uwagi i odniesienia
- (en) Michael Kofink, Menelaos Papagiannopoulos i Rudolf Galensa , „ (-) - Catechin in Cocoa and Chocolate: Occurrence and Analysis of an Atypical Flavan-3-ol Enantiomer ” , Molecules , vol. 12,2007, s. 1274-1288
- (en) Fereidoon Shahidi, Marian Naczk, Phenolics in Food and Nutraceuticals , CRC Press,2004( ISBN 1-58716-138-9 )
- P. Sarni-Manchado, V. Cheynier, Polyphenols in the food industry , Lavoisier, Editions Tec & Doc,2006, 398, str. ( ISBN 2-7430-0805-9 )
- (w) Bauer E Sumpio Alfredo Cordova C, W David Berke-Schlessel, Feng Qin Quan Hai Chen , „ Zielona herbata,„ azjatycki paradoks ”oraz choroby układu krążenia i choroby układu krążenia ” , J Am Coll Surg. , vol. 202 n O 5,2006
- (w) Quansheng Chen Zhiming Guo Jiewen Zhao , „ Identyfikacja poziomu jakości zielonej herbaty (Camellia sinensis (L.)), pomiar selonu w ręcznych katechinach i zawartości kofeiny metodą HPLC oraz wspomaganie rozpoznawania wzorca klasyfikacji wektorów ” , Journal of Pharmaceutical and Biomedical Analysis , vol. 48,2008, s. 1321-1325
- (w) Yukiaki Kuroda (red.), Yukihiko Hara (red.), Health Effects of Tea Catechins and Its: Mystery of Tea Catechins Springer2004
- (w) David Labbe, Angelo Tremblay, Laurent Bazinet , „ Wpływ temperatury i czasu parzenia na solubilizację katechin zielonej herbaty: Podstawa produkcji frakcji wzbogaconych w EGC i EGCG ” , Separation and Purification Technology , Vol. 49,2006, s. 1-9
- Tia M. Rains, Sanjiv Agarwal, Kevin C. Maki , „ Anti-otesity effects of green tea catechins: a mechanistic review ”, Journal of Nutritional Biochemistry , tom. 22,2011, s. 1-7
- (in) WE Bronner, GR Beecher , „ Metoda określania zawartości katechin w naparach herbaty metodą wysokosprawnej chromatografii cieczowej ” , Journal of Chromatography A , vol. 805,1998, s. 137-142
- (w) Ilja CW Arts, Peter CH Hollman, Daan Kromhout , „ Czekolada jako źródło flawonoidów herbaty ” , The Lancet , vol. 354,1999
- (in) P. Iacopini, Mr. Baldi, P. Storchi L. Sebastiani , " Katechina, epikatechina, kwercetyna, rutyna i resweratrol w czerwonych winogronach: zawartość, aktywność przeciwutleniająca in vitro i interakcje " , Journal of Food Composition and Analysis , vol. 21,2008, s. 589–598 (doi: 10.1016 / j.jfca.2008.03.011)
- Nicolas Vivas, Związki fenolowe i produkcja win czerwonych , Bordeaux, Editions Féret, 2007
- (w) J. Pontillon (koordynator), Cacao et Chocolat, produkcja, zastosowania, charakterystyka , Lavoisier TEC & DOC1997
- (w) IC Arts PCH Hollman D. Kromhout , " czekolady jako źródło flawonoidów herbaty " , The Lancet , N O 354 1999
- US Department of Agriculture, „ USDA bazy danych dla flawonoidów zawartości wybranych Foods, ” na http://www.nal.usda.gov , Biblioteka Narodowa Rolnicza,2003(dostęp 31 października 2008 ) , s. 1-78 [PDF]
- (w) Gunter Kuhnle, Jeremy Spencer PE Hagen Schroeter, Baskar Shenoy, Edward S. Debnam, S. Kaila S. Srai Catherine Rice-Evans i Ulrich Hahn , „ epikatechina i katechina są O-metylowane i glukuronidowane w jelicie cienkim ” , Biochemical and Biophysical Research Communications , vol. 277, 2000, s. 507-512
- (w) Beverly A. Warden, Lametta S. Smith, Gary R. Beecher, Douglas A. Balentine i Beverly A. Clevidence , „ Katechiny są biologicznie dostępne u mężczyzn i kobiet pijących czarną herbatę przez cały dzień ” , The Journal of Nutrition , lot. 131,2001, s. 1731-1737
- (w) Mao-Jung Lee, Pius Maliakal, Laishun Chen Xiaofeng Meng, Flordeliza Y. Bondoc, Saileta Prabhu George Lambert, Sandra Mohr i Chung S. Yang3 , „ Farmakokinetyka katechin herbaty po spożyciu zielonej herbaty i (- ) - 3-galusan epigallokatechiny przez ludzi: tworzenie różnych metabolitów i zmienność indywidualna ” , Cancer Epidemiology, Biomarkers & Prevention , vol. 11,2002, s. 1025-1032
- (w) Joshua D. Lambert, Chung S. Yang , „ Cancer chemopreventive activity and bioavailability of tea and tea polifhenols ” , Mutation Research , tom. 523-524, 2003, s. 201-208
- (w) Wang JF, Schramm DD, Holt RR Ensunsa JL Fraga CG, Schmitz HH, Keen CL , „ Efekt odpowiedzi na dawkę ze spożycia czekolady to epikatechina w osoczu i uszkodzenia oksydacyjne ” , J Nutr , Vol. 130,2000
- gdy do DPPH dodany zostanie środek przeciwrodnikowy • wolny elektron jest sparowany, a purpurowy kolor zmienia się na żółty
- (en) Nanjo F, Goto K, Seto R, Suzuki M, Sakai M, Hara Y. , „ Efekty wychwytujące katechiny herbaty i ich pochodne to rodnik 1,1-difenylo-2-pikrylohydrazyl. » , Wolny Radic Biol Med. , vol. 21, n o 6,1996, s. 895-902
- (w) Jessica Tabart Claire Kevers Joel Pincemail , Jean-Olivier Defraigne i Jacques Dommes , „ Porównawcze zdolności przeciwutleniające związków fenolowych mierzone różnymi testami ” , Food Chemistry , tom. 113,2009, s. 1226-1233
- (i) Silvina B. Lotito, Balz Frei , „ spożycie żywności bogatej flawonoidy i zwiększonej zdolności przeciwutleniającej osoczu u ludzi: Bo, skutkiem lub epifenomenem? » , Free Radical Biology & Medicine , vol. 41,2006, s. 1727-1746
- (w) Janice F. Wang, Derek D. Schramm, Roberta R. Holt, Jodi L. Ensunsa, Cesar G. Fraga, Harold H. Schmitz i Carl L. Keen , „ Efektem reakcji na dawkę z konsumpcji czekolady jest plazma Epikatechina i uszkodzenia oksydacyjne ” , The Journal of Nutrition , vol. 130,2000
- (w) Ying Wan, Joe A Vinson, Terry D Etherton, John Proch, Sheryl A Lazarus i Penny M Kris-Etherton , „ Wpływ proszku kakaowego i ciemnej czekolady na podatność na utlenianie LDL i stężenia prostaglandyn u ludzi ” , Am J Clin Nutr. , vol. 74 N O 5,2001, s. 596-602
- (w) Darko Modun Ivana Music, Jonatan Vukovic, Ivica Brizic, Visnja Katalinic Ante Obad Ivan Palada Zeljko Dujic Mladen Boban , " Wzrost zdolności antyoksydacyjnej ludzkiego osocza po spożyciu czerwonego wina jest spowodowany zarówno moczanem osocza, jak i polifenolami wina " , Miażdżyca , vol. 197,2008, s. 250-256
- (in) Yue Zhu De and Yu Xie, " Docking Characterization and in vitro Inhibitory Activity of Flavan-3-ols and Proanthocyanidins dimeric Against the Main Protease Activity of SARS-Cov-2 " , Frontiers in Plant Science ,30 listopada 2020 r( DOI 10.3389 / fpls.2020.601316 , czytaj online , dostęp: 4 stycznia 2021 ).
Linki zewnętrzne
Oszacowanie spożycia katechin i procyjanidyn w stosunku do umiarkowanego i regularnego spożycia win we Francji , Carando S., Teissedre PL i Cabanis JC z Centrum Szkoleń i Badań Enologicznych Wydziału Farmaceutycznego w Montpellier.