Cysteina
| Cysteina | |
 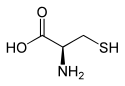 L lub R (+) - cysteina i D lub S (-) - cysteina |
|
| Identyfikacja | |
|---|---|
| Nazwa IUPAC | kwas 2-amino-3-merkaptopropanowy |
| Synonimy |
C, Cys |
| N O CAS |
(racemiczny) L lubR(+) D lubS(-) |
| N O ECHA | 100 000 145 |
| N O WE | 200-158-2 L 213-062-0 D |
| N O E | E920 L |
| FEMA | 3263 L |
| Właściwości chemiczne | |
| Formuła |
C 3 H 7 N O 2 S [Izomery] |
| Masa cząsteczkowa | 121,158 ± 0,009 g / mol C 29,74%, H 5,82%, N 11,56%, O 26,41%, S 26,47%, |
| pKa | 1,91 8,14 10,28 |
| Właściwości fizyczne | |
| T ° fuzja | 240 °C |
| Rozpuszczalność | 280 g · L -1 w wodzie ( 25 °C ) |
| Właściwości biochemiczne | |
| Kodony | UGU , UGC |
| izoelektryczne pH | 5.07 |
| Niezbędny aminokwas | Zgodnie ze sprawą |
| Występowanie u kręgowców | 3,3% |
| Środki ostrożności | |
| WHMIS | |
|
Produkt niekontrolowanyTen produkt nie jest kontrolowany zgodnie z kryteriami klasyfikacji WHMIS. |
|
| Dyrektywa 67/548/EWG | |
 Xn Symbole : Xn : Szkodliwy Zwroty R : R22 : Działa szkodliwie po połknięciu. Zwroty R : 22, |
|
| Jednostki SI i STP, chyba że zaznaczono inaczej. | |
Cysteiny (Skróty IUPAC - IUBMB : Cys i C ) z starożytnego greckiego κύστις ( „ pęcherz ”) jest kwaśny α-aminokwas, którego enancjomer L jest jednym z 22 tworzących białka aminokwasów , kodowany na RNA przez Ugu i UGC kodony . Nie jest uważana za niezbędną dla człowieka, ale może być wytwarzana w niewystarczających ilościach przez organizm w zależności od stanu zdrowia jednostek – zwłaszcza w przypadku niektórych chorób metabolicznych i zespołów złego wchłaniania – a także u pacjentów, dzieci i osób starszych.
Jest to naturalne α-aminokwas, charakteryzujący się obecnością sulfhydrylową -SH grupy tworzącej tiol ; selenocysteina i tellurocystéine są jak których atom siarki zastępuje się odpowiednio atom selenu i telluru .
Cysteina występuje w niewielkich ilościach w większości białek . Jego obecność w białkach jest bardzo ważna, w szczególności dlatego, że umożliwia tworzenie mostków dwusiarczkowych . Grupa tiolowa jest bardzo delikatna, ponieważ łatwo się utlenia. Jej utlenianie prowadzi do powstania cystyny , która składa się z dwóch cząsteczek cysteiny połączonych mostkiem dwusiarczkowym. Silniejszy utleniacz może utlenić cysteinę na jej siarkę, dając kwas cysteinowy HO 3 S – CH 2 – CH (NH 2 ) COOH, z której pochodzi tauryna , produkt dekarboksylacji obecny w żółci w postaci taurocholanu .
W celu „ochrony” tioli przed cysteinami lub redukcji mostków dwusiarczkowych stosuje się różne reakcje, w szczególności:
- Przemieszczenie przez duży nadmiar wolnych tioli:
- przez monotiole typu R-SH. Najczęściej stosowanym jest 2-merkaptoetanol : HS H 2 C – CH 2 OH,
- przez cyklizowane ditiole, np. ditiotreitol : HS H 2 C – CHOH – CHOH – CH 2 SH ;
- Alkilacja wolnych tioli.
Blokowanie alkilacji jest powszechnie stosowane podczas badania białek. Wykorzystuje w szczególności jodoacetamid prowadzący do karboksyamidometylacji:
Cys – SH + IH 2 C – CONH 2→ Cys – S – CH 2 – CONH 2.Cysteinę można przyjmować jako suplement diety w postaci N- acetylocysteiny (NAC).
Mogła odegrać ważną rolę w rozwoju życia na ziemi.
Podanie
Cysteina jest dopuszczona jako dodatek do żywności i nosi numer E920 .
Produkcja
Kwas L- cysteinowy i L- cysteinę można wytwarzać w ilościach przemysłowych z niektórych GMO , w szczególności Escherichia coli z glukozy i soli mineralnych , z piór rozpuszczonych w kwasie solnym, a także z włosów ludzkich , które zawierają więcej. Ten ostatni sposób produkcji został zakazany we Francji w opinii Wyższej Rady Higieny Publicznej Francji w opinii z dnia 8 czerwca 1999 r . „podającej ogólne zalecenie Komitetu Naukowego ds. Żywności dla Ludzi sprzeciwiające się recyklingowi wewnętrznemu. decyzja ta jest jednak trudna do zastosowania, ponieważ pochodzenie dystrybuowanej cysteiny nie może być łatwo określone.
Europejski Urząd Bezpieczeństwa Żywności (EFSA) wydał zezwolenie, przez dyrektywy opaździernik 2010, Stosowanie L- cysteiny w herbatnikach dla niemowląt i małych dzieci w celu zapobiegania zadławieniu przez fragmentację tłuszczu o niskiej zawartości ciastek . Mówiąc bardziej ogólnie, cysteina pozwala makaronowi lepiej zatrzymywać gaz i przez długi czas zachować obszerne kształty, co sprzyja przepływowi tych produktów do cukierników .
Żywność będąca źródłem cysteiny
- Drożdże
- kiełki pszenicy
- Czosnek
- Cebula
- brukselki
- Konopie
- brokuły
- Nabiał
- Orzechy
- Posiew
- Fonio
- Owoce morza
- Ryba
- Jajka
- Mięso
Działanie w ludzkim ciele
Cysteina bierze udział w syntezie melaniny , naturalnego barwnika skóry i włosów .
Bierze również udział w syntezie koenzymu A, który odgrywa ważną rolę w metabolizmie człowieka.
A ponieważ jej pozostałości ustalić metali kationy , wydaje się brać udział w niektórych procesach zanieczyszczenia , biokoncentacji i naturalne detoksykacji korpusu ( chelatacji z metali ciężkich lub toksycznych niemetali ).
Uwagi i referencje
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- (w) Francis A. Carey, „ Tabela PK i wartościach pH ” , w Wydziału Chemii na Uniwersytecie w Calgary , 2014(dostęp 26 lipca 2015 )
- (w) Pan Beals, L. Gross, S. Harrell, „ Częstotliwość aminokwasów ” w Instytucie Modelowania Środowiskowego (ITSH) na Uniwersytecie Tennessee (dostęp 26 lipca 2015 r. )
- „ cysteina (l) ” w bazie danych chemikaliów Reptox z CSST (Quebec organizacji odpowiedzialnej za bezpieczeństwo i higienę pracy), dostęp 25 kwietnia 2009
- Streszczenie słownika grecko-francuskiego A. Bailly, s. 520 .
- Terminologia medyczna autorstwa Georgesa Dolisi
- (w) Yannick Vallee , Ibrahim Shalayel , Dung Kieu- Ly i K. Raghavendra Rao , „ Na samym początku życia na Ziemi: światowa hipoteza peptydu bogatego w tiole (TRP) ” , International Journal of Developmental Biology , tom. 61, n kość 8-9,8 listopada 2017 r.( ISSN 0214-6282 i 1696-3547 , przeczytane online , skonsultowane 16 kwietnia 2018 r. )
- Cysteina na stronie GMO Compass.
- http://www.economie.gouv.fr/files/files/directions_services/dgccrf/boccrf/00_01/a0010016.htm Opinia Wyższej Rady Higieny Publicznej Francji dotycząca wniosku o zezwolenie na stosowanie L Cysteiny z ludzkich włosów w ludzkiej żywności].
- Dyrektywa Komisji 2010/69/UE z dnia 22 października 2010 r. zmieniająca załączniki do Dyrektywy 95/2/WE Parlamentu Europejskiego i Rady w sprawie dodatków do żywności innych niż barwniki i substancje słodzące .
- HMCOF SEABIRDS " Zanieczyszczenie metalami ciężkimi ptaków morskich i morświnów w Morzu Północnym ;" Biuletyn Królewskiego Towarzystwa Nauk Liège 61 (1992): 163.)
- MOENNE, Alejandry. „Eukariotyczne metalotioneiny: białka, regulacja genów i homeostaza miedzi”. Zeszyty biologii morskiej 42.1-2 (2001): 125-135.
Zobacz również
Powiązane artykuły
Linki zewnętrzne
- (en) http://www.chemie.fu-berlin.de/chemistry/bio/aminoacid/cystein_en.html
- (w) hydrofobowy charakter cysteiny.
- Badanie pilotażowe nad tolerancją spożycia izolatu białka bogatego w cysteinę (Immunocal) u osób z autyzmem
Bibliografia
- Brattström, L., et al. „ Homocysteina i cysteina: wyznaczniki poziomu w osoczu u osób w średnim i starszym wieku ”. Journal of Internal Medicine 236,6 (1994): 633-641 ( streszczenie ).
- Quig, David. „Metabolizm cysteiny i toksyczność metali”. Przegląd medycyny alternatywnej 3 (1998): 262-270.
- Rhee, Sue Goo, et al. „Nadtlenek wodoru: kluczowy przekaźnik, który moduluje fosforylację białek poprzez utlenianie cysteiny”. Sygnalizacja naukowa 2000.53 (2000): pe1-pe1 ( streszczenie ).
- Turk, Vito i Wolfram Bode. „ Cystatyny: białkowe inhibitory proteinaz cysteinowych ”. Listy FEBS 285,2 (1991): 213-219.
- Turk, Vito, Boris Turk i Dušan Turk. „Lizosomalne proteazy cysteinowe: fakty i możliwości”. Czasopismo EMBO 20.17 (2001): 4629-4633 ( streszczenie ).
- Van Wart, Harold E. i Henning Birkedal-Hansen. „ Przełącznik cysteinowy: zasada regulacji aktywności metaloproteinazy z możliwością zastosowania do całej rodziny genów metaloproteinaz macierzy. ” Proceedings of the National Academy of Sciences 87.14 (1990): 5578-5582 streszczenie .