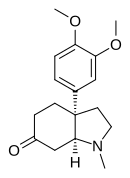
Mesembrine
| Mesembrine | |
|
|
| Identyfikacja | |
|---|---|
| Nazwa IUPAC | (3a S , 7a S ) -3a- (3,4-dimetoksyfenylo) -1-metylooktahydro-6H-indol-6-on |
| N O CAS |
[(+) - (3aR, 7aR)] [(-) - (3aS, 7aS)] |
| PubChem | 193296 |
| UŚMIECHY |
COc1ccc (cc1OC) [C @@] 23CCC (= O) C [C @ H] 3N (C) CC2 , |
| InChI |
InChI: InChI = 1 / C17H23NO3 / c1-18-9-8-17 (7-6-13 (19) 11-16 (17) 18) 12-4-5-14 (20-2) 15 ( 10-12) 21-3 / h4-5,10,16H, 6-9,11H2,1-3H3 / t16-, 17- / m1 / s1 |
| Właściwości chemiczne | |
| Brute formula |
C 17 H 23 N O 3 [Izomery] |
| Masa cząsteczkowa | 289,3694 ± 0,0163 g / mol C 70,56%, H 8,01%, N 4,84%, O 16,59%, |
| Jednostki SI i STP, chyba że określono inaczej. | |
Mesembrine jest alkaloidem indol obecny w wielu roślinach z rodziny Aizoaceae jako Mesembryanthemum crystallinum i nazwie Sceletium tortuosum (Kanna), oba pochodzące z Republiki Południowej Afryki .
Stereochemia
Mesembrine został po raz pierwszy wyizolowany i scharakteryzowany przez K. Bodendorf i W. Krieger w 1957 Mesembrine jest cząsteczka bicyklicznego ma dwa węgla z węgla chiralnego głowicy pomostu między pięcioczłonowy pierścień i sześcio-członowy pierścień. Ograniczenia steryczne nie pozwalają na istnienie pary enancjomerów : (+) - (3a R , 7a R ) -mésembrine i (-) - (3a S , 7a S ) -mésembrine. Chiralności deskryptorów z R i S w tej cząsteczce nie znajduje się w osiowym chiralności jednak odpowiednie dla systemu numeracji atomu, który wyznacza „a” z atomami pierścienia indolowego części cząsteczki, jak pokazano przez liczbę gałęzi - 3a Grupa 3,4-dimetoksyfenylowa w tej części. Lewoskrętny izomer (-) - mesembrin stanowi naturalną formę. W rzeczywistości stwierdzono, 1970, rozwiązując strukturę krystaliczną metylojodki pochodną 6-epimésembranol który jest jednoskośna , grupa przestrzenna P 2 1 ( N O 4).
własność
W medycynie tradycyjnej alkaloidowi przypisuje się właściwości przeciwdepresyjne . U szczurów obserwuje się zahamowanie wychwytu zwrotnego serotoniny z towarzyszącą ataksją : ten drugi efekt może ograniczyć jej potencjał terapeutyczny, chociaż alkaloid wydaje się wykazywać niską toksyczność in vivo . Mesembrin jest również inhibitorem fosfodiesterazy .
Całkowita synteza
Ze względu na swoją strukturę i aktywność biologiczną mesembrin jest celem w drodze całkowitej syntezy od lat 70. XX w. Opisano ponad czterdzieści całkowitych syntez mezembryny, z których większość skupia się na różnych podejściach i strategiach budowy komórki, układu bicyklicznego i czwartorzędowego atomu węgla .
Pierwsza całkowita synteza mesembriny została opisana przez Maurice'a Shammę i Hermana R. Rodrigueza w 1965 roku. Ta syntetyczna droga składa się z dwudziestu jeden kroków, co plasuje ją wśród najdłuższych dla mesembryny. Główne etapy obejmują budowę sześcioczłonowego pierścienia z ketonem w reakcji Dielsa-Aldera , α - allilację do syntezy czwartorzędowego węgla oraz reakcję addycji sprzężonej w celu ostatecznego zamknięcia pięcioczłonowego pierścienia. Produktem końcowym tej drogi syntezy jest mieszanina racemiczna (+) - i (-) - mesembryny:
W 1971 roku Shun-ichi Yamada opisał pierwszą całkowitą asymetryczną syntezę (+) - mesembriny. Czwartorzędowy węgiel jest wprowadzany przez asymetryczną anelację Robinsona wspomaganą przez pochodną L-proliny .
Źródła
- (en) / (de) Ten artykuł jest częściowo lub w całości z artykułów zatytułowanych w języku angielskim „ Mesembrine ” ( zobacz listę autorów ) i niemieckim „ Mesembrin ” ( zobacz listę autorów ) .
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- JS Glasby, ((Directory Of Plants Containing Secondary Metabolites , Taylor & Francis, Londyn, Nowy Jork, 1991, str. 780. ( ISBN 978-0-85066-423-2 ) .
- MT Smith, NR Crouch, N. Gericke, M. Hirst, Psychoactive constituents of the genus Sceletium NEBr. i inne Mesembryanthemaceae: A Review , Journal of Ethnopharmacology, 1996, vol. 50 ust. 3, str. 119–130. DOI : 10.1016 / 0378-8741 (95) 01342-3 , .
- K. Bodendorf, W. Krieger ,, Arch. Pharm., 1957, t. 290, s. 441-448
- P. Coggon, DS Farrier, PW Jeffs, AT McPhail, Absolute configuration of mesembrine and related alkaloidids: X-ray analysis of 6-epimesembranol methiodide. , J. Chem. Soc. B, 1970, s. 1267-1271. DOI : 10.1039 / J29700001267 .
- Peter W. Jeffs, Richard L. Hawks, DS Farrier, Struktura mesembranoli i absolutna konfiguracja mesembryny i pokrewnych alkaloidów , J. Am. Chem. Soc. , 1969, t. 91 (14), str. 3831–3839. DOI : 10.1021 / ja01042a025 .
- GI Stafford, ME Pedersen, J. van Staden, AK Jäger, Review on plants with CNS-effects used in tradycyjnej południowoafrykańskiej medycynie przeciwko chorobom psychicznym , Journal of Ethnopharmacology, 2008, vol. 119 ust. 3, s. 513–537. DOI : 10.1016 / j.jep.2008.08.010 , .
- MJ Loria, Z. Ali i wsp., Effects of Sceletium tortuosum in rats , J Ethnopharmacol., 2014, vol. 155, s. 731–735. DOI : 10.1016 / j.jep.2014.06.007 ,
- Ocena bezpieczeństwa toksykologicznego standaryzowanego ekstraktu ze Sceletium tortuosum (Zembrin (®)) u szczurów , Food Chem Toxicol., 2014, vol. 74, s. 190–199. DOI : 10.1016 / j.fct.2014.09.017 , .
- AL Harvey, LC Young, AM Viljoen, NP Gericke, Farmakologiczne działania południowoafrykańskiej rośliny leczniczej i żywności funkcjonalnej Sceletium tortuosum i jego głównych alkaloidów , Journal of Ethnopharmacology, 2011, vol. 137 ust. 3, s. 1124–1129. DOI : 10.1016 / j.jep.2011.07.035 , .
- Maurice Shamma, Herman R. Rodriguez, The total synthesis of (±) -mesembrine , Tetrahedron Lett., 1965, vol. 6 (52), s. 4847-4851. DOI : 10.1016 / S0040-4039 (01) 89046-8 .
- Shun-ichi Yamada, Całkowita synteza (+) - mesembryny przez asymetryczną syntezę z aminokwasem , Tetrahedron Lett., 1971, vol. 12 (16), str. 1133-1136. DOI : 10.1016 / S0040-4039 (01) 96647-X .