Asparagina
| Asparagina | |
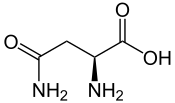 L lub S (-) - asparagina D lub R (+) - asparagina 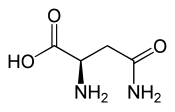 |
|
| Identyfikacja | |
|---|---|
| Nazwa IUPAC | Kwas 2,4-diamino-4-oksobutanowy |
| Synonimy |
Kwas N, Asn, ( 2S ) -2-amino-3-karbamoilo-propanowy |
| N O CAS |
(racemiczny) (D) lubR(+) (L) lubS(-) |
| N O ECHA | 100,019,565 |
| N O WE | 200-735-9 (L) |
| UŚMIECHY |
NC (= O) CC (N) C (= O) O , |
| InChI |
InChI: InChI = 1 / C4H8N2O3 / c5-2 (4 (8) 9) 1-3 (6) 7 / h2H, 1,5H2, (H2,6,7) (H, 8,9) |
| Właściwości chemiczne | |
| Brute formula |
C 4 H 8 N 2 O 3 [Izomery] |
| Masa cząsteczkowa | 132,1179 ± 0,0051 g / mol C 36,36%, H 6,1%, N 21,2%, O 36,33%, |
| pKa | l-asparagina: p K a 1 = 2,16 , p K a 2 = 8,73 w 25 ° C |
| Właściwości fizyczne | |
| T ° fuzja | 235 ° C |
| Rozpuszczalność | 25,1 g · kg -1 |
| Masa objętościowa | 1 g · cm -3 |
| Właściwości biochemiczne | |
| Kodony | AAU, AAC |
| izoelektryczne pH | 5.41 |
| Niezbędny aminokwas | Nie |
| Występowanie u kręgowców | 4,4% |
| Środki ostrożności | |
| WHMIS | |
|
Produkt niekontrolowanyTen produkt nie jest objęty kontrolą zgodnie z kryteriami klasyfikacji WHMIS. |
|
| Jednostki SI i STP, chyba że określono inaczej. | |
Asparagina (Skróty IUPAC - IUBMB : Asn i N ) jest kwaśny α-aminokwas, którego enancjomer L jest jednym z 22 tworzących białka aminokwasów , kodowany z mRNA przez kodon AAU i AAC. Jego promień van der Waalsa wynosi 96 Å . Wynika to z amidowania z terminala karboksylowej z asparaginianu . Daje polarne reszty, które są elektrycznie obojętne i mają tendencję do tworzenia wiązań wodorowych poprzez swoją grupę amidową .
Biosynteza i degradacja
Prekursor do asparaginy szczawiooctan. Szczawiooctan jest przekształcany do asparaginianu przy użyciu enzymu transaminazy. Enzym przenosi grupę aminową z glutaminianu do szczawiooctanu, wytwarzając α-ketoglutaran i asparaginian. Enzym syntetaza asparaginy wytwarza asparaginę, AMP, glutaminian i pirofosforan z asparaginianu, glutaminy i ATP. W reakcji syntetazy asparaginy ATP jest używany do aktywacji asparaginianu, tworząc β-aspartylo-AMP. Glutamina tworzy grupę amonową, która reaguje z β-aspartylo-AMP, tworząc asparaginę i wolny AMP.
Funkcje strukturalne
Oligosacharydy są połączone z asparaginą podczas N-glikozylacji .
Rodnik tego aminokwasu jest ponadto w dużej mierze odpowiedzialny za selektywność akwaporyny . Rzeczywiście, tworząc słabe wiązania z wodą w akwaporynie, zapobiega ruchowi protonów H + wzdłuż cząsteczek wody.
Anegdoty
- Asparagina była pierwszym aminokwasem odkrytym w 1806 roku przez Louisa-Nicolasa Vauquelina, który następnie badał szparagi , stąd jej nazwa.
- Asparagina jest często kojarzona z charakterystycznym zapachem moczu po spożyciu szparagów, ale niektórzy naukowcy nie zgadzają się i sugerują inne substancje, takie jak kwas szparagowy .
Uwagi i odniesienia
- "Properties of Amino Acids", w CRC Handbook of Chemistry and Physics , 91 th Edition (Internet wersja 2011), WM Haynes, red., CRC Press / Taylor i Francis, Boca Raton, Floryda. P. 7-1
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- (w) Mr. Beals, L. Gross, S. Harrell, " Amino Acid Frequency " on The Institute for Environmental Modeling (ITSH) to the University of Tennessee (dostęp: 26 lipca 2015 )
- „ asparaginowy (l) ” w bazie danych chemikaliów Reptox z CSST (Quebec organizacji odpowiedzialnej za bezpieczeństwo i higienę pracy), dostęp 25 kwietnia 2009
- (w) SC Mitchell , " Idiosynkrazje żywnościowe: buraki i szparagi " , Metabolizm i usposobienie leków , t. 29 N O 4,1 st kwiecień 2001, s. 539-543 ( ISSN 0090-9556 i 1521-009X , PMID 11259347 , czytaj online , dostęp 20 stycznia 2017 )
- (w) ML Pelchat , C. Bykowski , FF Duke i Dr Reed , „ Wydalanie i postrzeganie charakterystycznego zapachu w moczu po spożyciu szparagów: badanie psychofizyczne i genetyczne ” , Chemical Senses , Vol. 36, n o 1,1 st styczeń 2011, s. 9–17 ( ISSN 0379-864X , PMID 20876394 , PMCID PMC3002398 , DOI 10.1093 / chemse / bjq081 , czytaj online , dostęp 20 stycznia 2017 )