Agregacja białek
Agregacja białek (lub agregacji / aglomeracja białka ) jest zjawiskiem biologicznym, w którym białka słabo zagięte agregat (to znaczy, kumulują się i są zgrupowane) tak wewnątrz- jako zewnątrzkomórkowa. Te agregaty białek są często skorelowane z chorobą . W rzeczywistości agregaty białek odgrywają rolę w wielu różnych chorobach, które nazwano amyloidozą , w tym ALS , chorobach Alzheimera i Parkinsona oraz chorobach prionowych .
Białka po ich syntezie mają zwyczaj fałdowania się do określonej konformacji trójwymiarowej, która jest dla nich najbardziej korzystna termodynamicznie : stan naturalny . Proces składania jest napędzany przez działanie hydrofobowe , co jest tendencja części hydrofobowe białek próby zabezpieczenia się z hydrofilowego środowiska w komórce przez wiercenie otworów wewnątrz białka. Zatem strona zewnętrzna białka jest typowo hydrofilowa, podczas gdy jego wnętrze jest typowo hydrofobowe.
Struktury białek są stabilizowane przez wiązania niekowalencyjne i wiązania dwusiarczkowe łączące dwie reszty cysteiny . Oddziaływania niekowalencyjne obejmują wiązania jonowe i słabe oddziaływania van der Waalsa . Oddziaływania jonowe powstają między anionem a kationem i tworzą mostki solne, które pomagają stabilizować białko. Oddziaływania Van der Waalsa obejmują oddziaływania niepolarne ( siły Londynu ) i polarne ( wiązania wodorowe , siły międzycząsteczkowe ). Odgrywają one ważną rolę w strukturze drugorzędowej białek, takich jak tworzenie alfa helisy lub arkusza beta , a także w ich strukturze trzeciorzędowej . Oddziaływania między resztami aminokwasów w danym białku są bardzo ważne dla ostatecznej struktury tego białka.
Kiedy zachodzą zmiany w interakcjach niekowalencyjnych, co może wynikać ze zmiany sekwencji aminokwasów, białko prawdopodobnie źle się zwija lub wcale. W tego typu sytuacji, jeśli komórka nie pomaga białkom w naprawieniu tego fałdującego defektu lub ich zniszczeniu, mogą się one zlepiać, aw tym procesie odsłonięte hydrofobowe części białek mogą wchodzić w interakcje z odsłoniętymi częściami hydrofobowymi. białka. Istnieją trzy główne typy agregatów białek, które mogą tworzyć: agregaty amorficzne, oligomery i włókienka amyloidowe.
Przyczyny
Agregacja białek może mieć kilka przyczyn. Istnieją cztery klasy, do których można podzielić te przyczyny, które opisano szczegółowo poniżej.
Mutacje
Te mutacje występujące w sekwencji z DNA może być lub może nie mieć wpływu na sekwencję aminokwasową białka. Jeśli ma to wpływ na sekwencję, inny aminokwas może zmienić interakcje między łańcuchami bocznymi , co wpływa na fałdowanie białka. Może to prowadzić do odsłonięcia hydrofobowych regionów białka, które agregują z tym samym źle sfałdowanym lub nie sfałdowanym białkiem lub z innym białkiem.
Oprócz mutacji wpływających na same białka agregację białek można również wywołać pośrednio przez mutacje występujące w białkach na szlakach regulatorowych, takich jak szlak fałdowania ( chaperony ) lub szlak ubikwityna-proteasom ( ligazy ubikwityny ). Chaperony pomagają białkom fałdować się, zapewniając im bezpieczne środowisko do fałdowania. Ligazy ubikwityny celują w białka, które ulegają degradacji poprzez modyfikację ubikwityny .
Defekty podczas syntezy białek
Agregacja białek może być spowodowana problemami występującymi podczas transkrypcji lub translacji . Podczas transkrypcji DNA jest kopiowane do mRNA , tworząc nić pre-mRNA, która podlega potranskrypcyjnym modyfikacjom w celu utworzenia mRNA. Podczas translacji rybosomy i RNA pomagają w translacji sekwencji mRNA na sekwencję aminokwasów. Jeśli defekty wystąpią podczas któregokolwiek z tych dwóch etapów, wytwarzając nieprawidłową nić mRNA lub sekwencję aminokwasów, powoduje to nieprawidłowe fałdowanie białka, co prowadzi do agregacji białka.
Stres środowiskowy
Stresy środowiskowe, takie jak ekstremalne temperatury lub pH lub stres oksydacyjny, mogą również prowadzić do agregacji białek. Przykładem choroby wywołanej tego typu stresem jest krioglobulinemia .
Ekstremalne temperatury mogą osłabiać i destabilizować niekowalencyjne wiązania między resztami aminokwasów. PH poza zakresem pH danego białka mogą zmieniać stan protonowania aminokwasów, co może zwiększać lub zmniejszać interakcje niekowalencyjne. Może również prowadzić do mniej stabilnego wiązania, a zatem nie fałdowania białka.
Stres oksydacyjny może być spowodowany przez rodniki, takie jak RFT . Te niestabilne rodniki mogą atakować reszty aminokwasowe, prowadząc do utleniania łańcuchów bocznych (takich jak aromatyczne łańcuchy boczne lub metioninowe łańcuchy boczne) i / lub rozszczepienia wiązań polipeptydowych. Może to wpływać na wiązania niekowalencyjne, które utrzymują białko w prawidłowym kształcie, co może powodować destabilizację białka, a tym samym zapobiegać fałdowaniu się białka.
Starzenie się
Komórki mają mechanizmy, które mogą ponownie fałdować lub rozkładać agregaty białek. Jednak wraz ze starzeniem się komórek te mechanizmy kontrolne są mniej wydajne i komórka jest mniej zdolna do przejęcia kontroli nad tymi agregatami.
Hipoteza, zgodnie z którą agregacja białek jest konsekwencją procesu starzenia, jest obecnie możliwa do przetestowania, ponieważ opracowywane są pewne modele opóźnionego starzenia. Gdyby rozwój agregatów białkowych był procesem niezależnym od starzenia, spowolnienie tego starzenia nie miałoby wpływu na tempo proteotoksyczności w czasie. Gdyby jednak starzenie się wiązało ze spadkiem aktywności mechanizmów ochronnych przed proteotoksycznością, modele spowolnionego starzenia wykazywałyby zmniejszenie agregacji i proteotoksyczności. Aby rozwiązać ten problem, przeprowadzono kilka testów toksyczności na nicieniu C. elegans . Badania te wykazały, że zmniejszenie aktywności sygnalizacyjnej insuliny / IGF, dobrze znanego szlaku regulacji starzenia, chroni przed agregacją toksycznych białek związaną z neurodegeneracją. Trafność tego podejścia została przetestowana i potwierdzona na ssakach , ponieważ zmniejszenie aktywności szlaku sygnalizacji IGF-1 uchroniło badane myszy z chorobą Alzheimera przed zachowaniem i upośledzeniami związanymi z tą chorobą.
Lokalizacja kruszyw
Kilka badań wykazało, że odpowiedzi komórkowe na agregację białek są dobrze regulowane i zorganizowane. Agregaty białek są zlokalizowane w określonych obszarach komórki i badania skupiły się na tych obszarach u prokariontów ( E. coli ) i eukariontów ( drożdże , komórki ssaków).
W bakteriach
Agregaty bakterii znajdują się asymetrycznie na jednym z biegunów komórki, „ starszym biegunie ”. Po podziale komórki komórka potomna zawierająca bardziej przedni biegun uzyskuje agregat białka i rośnie wolniej niż komórka potomna bez agregatu. Stanowi to mechanizm naturalnej selekcji w celu redukcji agregatów białek w populacji bakterii.
W drożdżach
Większość agregatów białkowych w komórkach drożdży ma defekt fałdowania korygowany przez chaperony. Jednak niektóre agregaty mogą nie mieć skorygowanego defektu fałdowania, na przykład białka uszkodzone przez stres oksydacyjny lub białka przeznaczone do degradacji. Zamiast tego można je przekierować do jednego z dwóch przedziałów: przedziału kontroli jakości JUxtaNuclear ( JUNQ ) w pobliżu błony jądrowej i do nierozpuszczalnego depozytu białkowego lub IPOD w języku angielskim) w pobliżu wakuoli w komórkach drożdży. Agregaty białkowe trafiają do JUNQ, gdy są wszechobecne i przeznaczone do degradacji, podczas gdy zbite i nierozpuszczalne białka trafiają do IPOD w celu dłuższego przechowywania. Wyniki pokazały, że białka w tym miejscu można usunąć na drodze autofagii . Te dwie możliwości działają razem w taki sposób, że białka mają tendencję do przechodzenia do IPOD, gdy szlak proteasomowy jest przeciążony.
W komórkach ssaków
W komórkach ssaków te agregaty białkowe nazywane są „agresomami” i powstają, gdy komórka jest chora. Dzieje się tak, ponieważ agregaty mają tendencję do tworzenia się, gdy w komórce obecne są białka heterologiczne, co może wystąpić, gdy komórka jest zmutowana. Ligaza ubikwityny E3 jest zdolna do rozpoznawania nieprawidłowo sfałdowanych białek i ich ubikwitynacji. HDAC6 może następnie powiązać ubikwityny i białka motoryczne dyneiny aby przetransportować „znakowany” agregaty w centrosomie . Tam gromadzą się razem w kuli otaczającej centrosom. Dostarczają białek opiekuńczych i proteasomów oraz aktywują autofagię.
Usuwanie kruszyw
Istnieją dwa główne systemy „kontroli jakości” w komórce odpowiedzialne za usuwanie agregatów białkowych. Błędnie sfałdowane białka mogą zostać ponownie sfałdowane przez system bi-opiekuńczy lub zdegradowane przez układ ubikwityna-proteasom lub przez autofagię.
Neo-składane
Układ dwu opiekuńcze wykorzystuje szaperony Hsp70 (DnaK-DnaJ-GrpE w E. coli i Ssa1-Ydj1 / SIS 1-Sse1 / Fe1 w drożdżach) i Hsp100 (ClpB w E. coli i w drożdżach Hsp104) do dezagregacji i neo zwiń białka.
Hsp70 oddziałuje z agregatami białek i rekrutuje Hsp100. Hsp70 stabilizuje aktywowany Hsp100. Hsp100 mają aromatyczne pętle porów stosowanych do gwintowania aktywność oddzielić pojedyncze polipeptydy. To gwintowanie działanie może być inicjowane w N-końcu , C-końcu , albo w środku polipeptydu . Polipeptyd podlega translokacji przez Hsp100 w szeregu etapów, z których każdy zużywa ATP . Polipeptyd nie fałduje się, a następnie nie fałduje się samoczynnie lub za pomocą białek szoku cieplnego ( białka szoku cieplnego ).
Degradacja
Błędnie sfałdowane białka mogą zostać usunięte przez układ ubikwityna-proteasom. Obejmuje szlak E1-E2-E3, który ubikwitynuje białka w celu ich degradacji. U eukariontów białka są degradowane przez proteasom 26S. W komórkach ssaków ligaza E3 i białko na końcu karboksylowym oddziałujące z Hsp70 celują w białka związane z Hsp70. U drożdży ligazy E3 Doa10 i Hrd1 mają podobne funkcje na białkach retikulum endoplazmatycznego :

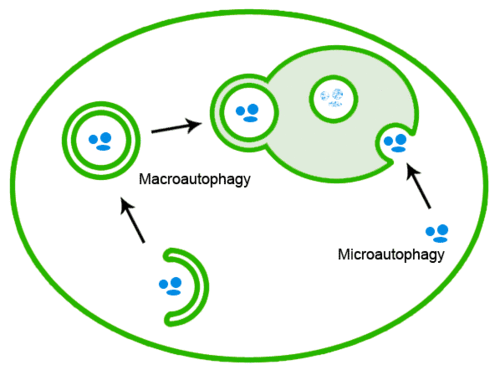
Błędnie sfałdowane białka można również usunąć przez autofagię, w której agregaty białek są transportowane do lizosomu :
Toksyczność
Chociaż uważano, że dojrzałe agregaty białek są toksyczne, ostatnie wyniki sugerują, że w rzeczywistości niedojrzałe agregaty białkowe są najbardziej toksyczne. Grupy hydrofobowe w tych agregatach mogą wchodzić w interakcje z innymi składnikami komórki i uszkadzać je. Hipotezy są takie, że toksyczność agregatów białkowych jest związana z mechanizmami sekwestracji składników komórkowych, z wytwarzaniem RFT, z wiązaniem się z określonymi receptorami w błonie lub z rozerwaniem błon. Test genetyczny wykazał, że gatunki o wyższej masie cząsteczkowej są odpowiedzialne za przepuszczalność błony. Wiadomo, że agregaty białek mogą destabilizować in vitro sztuczne dwuwarstwy lipidowe, co prowadzi do przepuszczalności błony.
Zobacz też
Uwagi
- (fr) Ten artykuł jest częściowo lub w całości zaczerpnięty z artykułu w angielskiej Wikipedii zatytułowanego „ Agregacja białek ” ( zobacz listę autorów ) .
Bibliografia
- Adriano Aguzzi i Tracy O'Connor , „ Choroby agregacji białek: patogeniczność i perspektywy terapeutyczne ”, Nature Reviews. Drug Discovery , tom. 9 N O 3,marzec 2010, s. 237-248 ( ISSN 1474-1784 , PMID 20190788 , DOI 10.1038 / nrd3050 , czytaj online , dostęp 30 października 2017 )
- Fernanda G. De Felice , Marcelo NN Vieira , M. Nazareth L. Meirelles i Ludmilla A. Morozova-Roche , „ Tworzenie agregatów amyloidu z ludzkiego lizozymu i jego wariantów związanych z chorobą przy użyciu ciśnienia hydrostatycznego ”, czasopismo FASEB: oficjalna publikacja Federacja Amerykańskich Towarzystw Biologii Eksperymentalnej , vol. 18 N O 10,Lipiec 2004, s. 1099–1101 ( ISSN 1530-6860 , PMID 15155566 , DOI 10.1096 / fj.03-1072fje , czytaj online , dostęp 30 października 2017 )
- Rudolph E. Tanzi i Lars Bertram , „ Dwadzieścia lat choroby Alzheimera, hipoteza amyloidowa: perspektywa genetyczna ”, Celi , tom. 120 n O 4,25 lutego 2005, s. 545–555 ( ISSN 0092-8674 , PMID 15734686 , DOI 10.1016 / j.cell.2005.02.008 , czytaj online , dostęp 30 października 2017 )
- MJ Gething i J. Sambrook , „ Protein folding in the cell ”, Nature , vol. 355 n O 635502 stycznia 1992, s. 33–45 ( ISSN 0028-0836 , PMID 1731198 , DOI 10.1038 / 355033a0 , czytaj online , dostęp 30 października 2017 )
- (w) David L. Cox i Michael Nelson , Lehninger Principles of Biochemistry , Nowy Jork, WH Freeman,2013( ISBN 978-1-4292-3414-6 ) , str. 143
- Sarah J Shoesmith Berke i Henry L Paulson , „ Agregacja białek i szlak ubikwitynowo-proteasomowy: zdobywanie ręki UPPer na neurodegenerację ”, Current Opinion in Genetics & Development , vol. 13 N O 3,1 st czerwiec 2003, s. 253–261 ( DOI 10.1016 / S0959-437X (03) 00053-4 , czytaj online , dostęp: 30 października 2017 )
- (w) Robert F. Weaver, Molecular Biology , Nowy Jork, McGraw-Hill,2012( ISBN 978-0-07-352532-7 ) , str. 122-156; 523-600
- Jens Tyedmers , Axel Mogk i Bernd Bukau , „ Cellular strategy for controllers protein ”, Nature Reviews. Molecular Cell Biology , tom. 11 N O 11listopad 2010, s. 777–788 ( ISSN 1471-0080 , PMID 20944667 , DOI 10.1038 / nrm2993 , czytaj online , dostęp 30 października 2017 )
- (in) ER Stadtman i RL Levine , „ Utlenianie wolnych rodników za pośrednictwem wolnych aminokwasów i reszt aminokwasowych w białkach ” , Amino Acids , vol. 25 Bez kości 3-4,1 st grudzień 2003, s. 207–218 ( ISSN 0939-4451 i 1438-2199 , DOI 10.1007 / s00726-003-0011-2 , odczyt online , dostęp: 30 października 2017 )
- James F. Morley , Heather R. Brignull , Jill J. Weyers i Richard I. Morimoto , „ Próg agregacji białek ekspansji poliglutaminy i toksyczności komórkowej jest dynamiczny i podlega wpływowi starzenia w Caenorhabditis elegans ”, Proceedings of the National Academy of Sciences of the United States of America , vol. 99 N O 166 sierpnia 2002, s. 10417–10422 ( ISSN 0027-8424 , PMID 12122205 , DOI 10.1073 / pnas.152161099 , czytaj online , dostęp 30 października 2017 )
- Natalia G. Bednarska , Joost Schymkowitz , Frederic Rousseau i Johan Van Eldere , „ Agregacja białek w bakteriach: cienka granica między funkcjonalnością a toksycznością ”, Microbiology (Reading, England) , vol. 159 n O Pt 9wrzesień 2013, s. 1795-1806 ( ISSN 1465-2080 , PMID 23894132 , DOI 10.1099 / mic.0.069575-0 , czytaj online , dostęp 30 października 2017 )
- Mari Takalo , Antero Salminen , Hilkka Soininen i Mikko Hiltunen , „ Białka agregacji i mechanizmy degradacji w chorobach neurodegeneracyjnych ”, American Journal of Neurodegenerative Disease , tom. 2 n o 1,2013, s. 1-14 ( ISSN 2165-591X , PMID 23516262 , PMCID PMC3601466 , czytaj online , dostęp 30 października 2017 )
- (w) Rafael Garcia-Mata , Ya-Sheng Gao i Elizabeth Sztul , „ Hassles with Taking Out the Garbage: Aggravating Aggresomes ” , Traffic , vol. 3 N O 6,1 st czerwiec 2002, s. 388–396 ( ISSN 1600-0854 , DOI 10.1034 / j.1600-0854.2002.30602.x , czytaj online , dostęp: 30 października 2017 )
- (w) Niels Gregersen Lars Bolund i Peter Bross , „ Niewłaściwe fałdowanie białek, agregacja i pogorszenie stanu chorobowego ” , Molecular Biotechnology , vol. 31 N O 21 st październik 2005, s. 141–150 ( ISSN 1073-6085 i 1559-0305 , DOI 10.1385 / MB: 31: 2: 141 , czytaj online , dostęp 30 października 2017 )
- Axel Mogk , Eva Kummer i Bernd Bukau , „ Współpraca maszyn opiekuńczych Hsp70 i Hsp100 w dezagregacji białek ”, Frontiers in Molecular Biosciences , tom. 2,2015, s. 22 ( ISSN 2296-889X , PMID 26042222 , PMCID PMC4436881 , DOI 10.3389 / fmolb.2015.00022 , czytaj online , dostęp 30 października 2017 )
- Krzysztof Liberek , Agnieszka Lewandowska i Szymon Zietkiewicz , „ Chaperones in control of protein disaggregation ”, The EMBO journal , vol. 27 N O 223 stycznia 2008, s. 328–335 ( ISSN 1460-2075 , PMID 18216875 , PMCID PMC2234349 , DOI 10.1038 / sj.emboj.7601970 , czytaj online , dostęp 30 października 2017 )
- Bryan Chen , Marco Retzlaff , Thomas Roos i Judith Frydman , „ Komórkowe strategie kontroli jakości białka ”, Cold Spring Harbor Perspectives in Biology , tom. 3 N O 8,1 st sierpień 2011, a004374 ( ISSN 1943-0264 , PMID 21746797 , PMCID PMC3140689 , DOI 10.1101 / cshperspect.a004374 , odczyt online , dostęp 30 października 2017 )
- YJ Zhu , H. Lin i R. Lal , „ Świeże i niefibrylarne białko amyloidu beta (1-40) indukuje szybkie zwyrodnienie komórkowe u starszych ludzkich fibroblastów: dowody na toksyczność komórkową, w której pośredniczy kanał AbetaP ”, czasopismo FASEB: oficjalna publikacja Federacja Amerykańskich Towarzystw Biologii Eksperymentalnej , vol. 14 N O 9,Czerwiec 2000, s. 1244-1254 ( ISSN 0892-6638 , PMID 10834946 , czytaj online , dostęp 30 października 2017 )
- C. Nilsberth , A. Westlind-Danielsson , CB Eckman i MM Condron , „ Arktyczna” mutacja APP (E693G) powoduje chorobę Alzheimera poprzez zwiększone tworzenie protofibryli Abeta ”, Nature Neuroscience , tom. 4, n O 9,Wrzesień 2001, s. 887-893 ( ISSN 1097-6256 , PMID 11528419 , DOI 10.1038 / nn0901-887 , odczyt online , dostęp 30 października 2017 )
- (w) Claudio Soto , „ Odkrywanie roli nieprawidłowego fałdowania białek w chorobach neurodegeneracyjnych ” , Nature Reviews Neuroscience , vol. 4, N O 1,styczeń 2003, s. 49–60 ( ISSN 1471-003X , DOI 10.1038 / nrn1007 , czytaj online , dostęp: 30 października 2017 )
- Patrick Flagmeier , Suman De , David C. Wirthensohn i Steven F. Lee , „ Ultrasensitive Measurement of Ca (2+) Influx into Lipid Vesicles Induced by Protein Aggregates ”, Angewandte Chemie (wyd. Międzynarodowe w języku angielskim) , vol. 56 N O 2726 czerwca 2017 r, s. 7750–7754 ( ISSN 1521-3773 , PMID 28474754 , PMCID PMC5615231 , DOI 10.1002 / anie.201700966 , czytaj online , dostęp 30 października 2017 )
Linki zewnętrzne
- (pl) Folding @ Home Pomoc w dekodowaniu fałdowania białek.
- (en) Rosetta @ Home Pomaga w przewidywaniu struktur białkowych i kompleksów.