Salicyline
| Salicyline | ||
| ||
 | ||
| Identyfikacja | ||
|---|---|---|
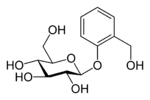
| Nazwa IUPAC | (2R, 3S, 4S, 5R, 6S) -2- (hydroksymetylo) -6- [2- (hydroksymetylo) fenoksy] oksano-3,4,5-triol | |
| Synonimy |
salicyna, D - (-) - salicyna, salicozyd, 2- (hydroksymetylo) fenylo-β-D-glukopiranozyd |
|
| N O CAS | ||
| N O ECHA | 100,004,847 | |
| N O WE | 205-331-6 | |
| PubChem | ||
| UŚMIECHY |
C1 = CC = C (C (= C1) CO) OC2C (C (C (C (O2) CO) O) O) O , |
|
| InChI |
InChI: InChI = 1 / C13H18O7 / c14-5-7-3-1-2-4-8 (7) 19-13-12 (18) 11 (17) 10 (16) 9 (6-15) 20-13 / godz.1-4.9-18H, 5-6H2 / t9-, 10-, 11 +, 12-, 13- / m1 / s1 |
|
| Właściwości chemiczne | ||
| Brute formula |
C 13 H 18 O 7 [Izomery] |
|
| Masa cząsteczkowa | 286,2778 ± 0,0138 g / mol C 54,54%, H 6,34%, O 39,12%, |
|
| Właściwości fizyczne | ||
| T ° fuzja | 197 do 200 ° C | |
| Rozpuszczalność | 40 g · L -1 (woda, 25 ° C ) | |
| Właściwości optyczne | ||
| Współczynnik załamania światła | 1.638 | |
| Ekotoksykologia | ||
| DL 50 | > 500 mg · kg -1 (mysz, dootrzewnowo) | |
| Względy terapeutyczne | ||
| Klasa terapeutyczna | przeciwbólowy | |
| Jednostki SI i STP, chyba że określono inaczej. | ||
Salicyny jest przeciwzapalne produkt z kory z wierzby białej (rodzaj Salix ).
Ten naturalny heterozyd D- glukozy ma budowę chemiczną bardzo podobną do aspiryny i ma taki sam wpływ na organizm . Po spożyciu tworzy metabolit : kwas salicylowy .
W 1825 roku włoski farmaceuta Francesco Fontana wyodrębnił substancję czynną z wierzby białej i nazwał ją salicyną.
W 1828 roku w Monachium Johann Buchner wydobył z kory wierzby białej, żółte kryształki ułożone w igły: salicylinę, o gorzkim smaku.
Rok później, w 1829 roku , francuski farmaceuta Pierre-Joseph Leroux ulepszył ten proces. Gotuje proszek z kory wierzby białej w wodzie i zagęszcza swój preparat. Otrzymuje białe kryształy, które ochrzcił salicyliną (od Salix = wierzba). Leroux mówi Akademii Nauk, że salicylina leczy gorączkę.
Salicyline, podobnie jak chinina, ma gorzki smak .
Uwagi i odniesienia
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- (w) S Daniells, „ Symrise odkrył tańsze alternatywy w bitter- maskers ” , www.foodnavigator.com, 9 października 2006(dostęp 13 grudnia 2007 )
Powiązane artykuły
- Kwas salicylowy
- Kwas acetylosalicylowy (aspiryna)