Wielościan koordynacyjny
Pojęcie wielościanu koordynacyjnego jest używane w krystalografii i chemii do opisania środowiska substancji chemicznej za pomocą jej ligandów w krysztale lub kompleksie . Jest to wielościan utworzony przez ligandy wokół centralnych form chemicznych. Liczba koordynacyjna , to znaczy liczba ligandów, nie jest wystarczająca do opisania środowiska substancji chemicznej, ponieważ dla danej liczby koordynacyjnej może występować wiele wielościanów koordynacyjnych. Na przykład, w stanie stałej, miedź ma liczbę koordynacyjną 4 z tlenu w krzemian z baru oraz miedzi BaCuSi 2 O 6a także koordynacja 4 siarki w stannicie Cu 2 FeSnS 4, ale jego wielościan koordynacyjny to kwadrat CuO 4 w BaCuSi 2 O 6i czworościan CuS 4 w stannicie.
W rozwiązaniu pojęcie koordynacji często sprowadza się do koordynacji kationów ( aniony są koordynowane ze słabą energią wiązania, która nie zapewnia dobrej stabilności struktury). Koordynacja jest określona, podobnie jak w stanie stałym, przez środowisko kationu w jego pierwszej sferze koordynacyjnej . Jest to definiowane przez ligandy (opcjonalnie rozpuszczalnik ), które są bezpośrednio związane z kationem. Te ligandy są zorientowane geometrycznie, a ich wiązanie jest dość silne, tak że wymiany z bytami drugiej sfery koordynacji są powolne. Ta druga sfera składa się głównie z cząsteczek rozpuszczalnika, ale nie wyłącznie, które są zorientowane przez obecność kationu, ale które wymieniają się (1) szybko z cząsteczkami rozpuszczalnika znajdującymi się na zewnątrz i (2) powoli z ligandami które są dla niego wewnętrzne. Geometria koordynacji kationu w roztworze jest mniej zróżnicowana niż w stanie stałym. W przypadku zwykłych ligandów większość kationów metali przyjmuje koordynację oktaedryczną, niewielka część przyjmuje koordynację czworościenną lub w płaszczyźnie kwadratowej, a metale w kolumnie miedzi na I stopniu utlenienia mają koordynację dwa (liniową). Spośród nich jon srebra diaminowego Ag (NH 3 ) 2+ (zwany także odczynnikiem Tollensa ) jest najbardziej znanym. Inne współrzędne wynikiem obecności konkretnych ligandów (na przykład o dużej objętości) lub dużych kationów metali ( Ta , W , etc. )
Ewentualne wielościany koordynacyjne dla danego związku chemicznego i jego ligandów zależą od stopnia utlenienia związków chemicznych i zaangażowanych promieni jonowych , a dokładniej od stosunku, gdzie jest promieniem jonowym centralnego związku chemicznego i promieniem jego ligandów.
Wielościany koordynacyjne na ogół nie są regularne. Na przykład w przypadku kompleksów mogą one wykazywać deformację spowodowaną elektronową konfiguracją kationu metalu w polu krystalicznym utworzonym przez ligandy. Tak jest w przypadku Cu (H 2 O) 62+, który przedstawia zniekształcenie osiowe, które można wyjaśnić efektem Jahna-Tellera . Innym przypadkiem nieregularności jest inny charakter chemiczny ligandów, jak w przypadku Cu (NH 3 ) 4 (H 2 O) 22+ . Jednak we wszystkich przypadkach jest zwyczajowo używać nazwy regularnych wielościanów do opisania koordynacji gatunków chemicznych.
Różne wielościany koordynacyjne
Wielościany koordynacyjne zwykle składają się z równobocznych trójkątnych ścian , takich jak czworościan , ośmiościan , dwupiramida trygonalna lub dwudziestościan . My też często spotkać twarze kwadratowych, jak w tetragonalnej piramidy , kostki lub sześcio-ośmiościan . Rzadziej można znaleźć wielościany koordynacyjne, których twarze mają dużą liczbę wierzchołków .
Poniższa tabela przedstawia wielościany koordynacyjne występujące w kompleksach w roztworze i kryształach:
| Koordynacja | Wielościan | Reprezentacja | Przykłady: struktura molekularna | Przykłady: stan stały |
|---|---|---|---|---|
| 2 | liniowy | Cu w jonie dimetylomerupranu (I) (CH 3 ) 2 Cu- | Ag w dicyjanargentacie potasu (I) KAg (CN) 2 |
|
| 3 | trójkąt |  |
B w trifluorku boru BF 3 | NO 3 w saletry KNO 3 , BO 3 , CO 3 w kalcycie CaCO 3 |
| 4 | czworościan | 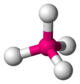 |
Ni w tetrakarbonylnickelu (0) Ni (CO) 4 | SiO 4 w kwarcu SiO 2 , BO 4 |
| kwadrat | 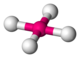 |
Ni w jonie tetracyjanonikielanowym (II) Ni (CN) 42− | Cu w CuO | |
| 5 | bipiramidy trygonalne |
 |
Fe w pentakarbonylferze (0) Fe (CO) 5 | K w K 3 Sb |
|
piramida czterokątna |
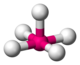 |
Brak prostej struktury prądu, ale jest to klasyczna struktura pośrednia w substytucji na kompleksie płasko-kwadratowym (przez dodanie nadchodzącego liganda) lub w podstawieniu na kompleksie oktaedrycznym (po odejściu wychodzącego liganda) | V w CaV 4 O 9, Ti w fresnoicie Ba 2 (TiO) Si 2 O 7 |
|
| 6 | oktaedr | 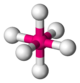 |
Ti w jonie heksaakwatytanu (II) Ti (H 2 O) 62+ | Na i Cl w NaCl, Ti w BaTiO 3 (struktura perowskitu ), Ni w breithauptite NiSb |
|
trójkątny lub trygonalny pryzmat |
 |
Sb in breithauptite | ||
| 7 |
pięciokątna dwupiramida |
 |
U w jonie UO 2 (H 2 O) 5 2+ | Pa w PaCl 5 |
ograniczona twarz ośmiościan |
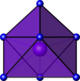 |
La w A-La 2 O 3 | ||
| zamknięty pryzmat o kwadratowej powierzchni |
||||
| 8 | sześcian | 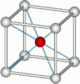 |
Cs i Cl w CsCl | |
|
kwadratowy lub czworokątny antypryzmat |
 |
|||
|
sześciokątna dwupiramida |
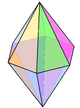 |
N w Li 3 N | ||
zmiękczony disphenoid |
 |
Zr w K 2 ZrF 6 | ||
| trygonalny pryzmat z dwoma zamkniętymi trójkątnymi ścianami |
||||
| trygonalny pryzmat z dwoma zakrytymi kwadratowymi powierzchniami |
 |
Ca w CaFe 2 O 4 | ||
| 9 | trygonalny pryzmat z trzema zakrytymi kwadratowymi powierzchniami |
 |
Pr w PrZr 3 F 15, Sr w SrCl 2 6H 2 O |
|
kwadratowy antypryzmat z zakrytą kwadratową twarzą |
 |
La w LaTe 2 | ||
| 10 | kwadratowy antypryzmat z zakrytymi twarzami |
|||
| 11 | ||||
| 12 | dwudziestościan |  |
Cr w Mg 3 Cr 2 Al 18 | |
| sześciokąt |  |
Atomy w strukturze metalowej typu ściśnięte ścianki sześcienne wyśrodkowane |
||
|
sześciokątny orthobicupola lub anticuboctahedron |
 |
Atomy w metalach o sześciokątnej zwartej strukturze typu stacking |
||
sześciokątny pryzmat |
 |
Rb w Rb 2 (VO) 2 [Si 8 O 19 ] |
Wyznaczanie wielościanu koordynacyjnego
W praktyce wielościany koordynacyjne w materiałach krystalicznych są często określane na podstawie eksperymentów z dyfrakcją promieni rentgenowskich , neutronów lub elektronów . Metody spektroskopowe , takie jak rentgenowska spektrometria absorpcyjna, mogą również dostarczyć informacji o środowisku związków chemicznych, zwłaszcza gdy znajdują się one w roztworze ciekłym lub w materiale amorficznym .
W przypadku kompleksów metali syntetyzowanych w roztworze koordynacja nie jest w pełni ustalona do czasu ustalenia struktury krystalograficznej. Warto więc przeanalizować różnice między kątami podstawowego wielościanu (na przykład ośmiościanu) a kątami faktycznie obserwowanymi. Często wynikają z ograniczeń sterycznych. To samo dotyczy odległości kationowo-ligandowych. Zniekształcenie odległości dla ligandów o porównywalnej wielkości można zinterpretować za pomocą efektu Jahna Tellera. Tak jest często w przypadku miedzi (II). Najbardziej symetryczna geometria w roztworze, która jest ogólnie akceptowana w dobrej zgodności z danymi NMR, jest tylko średnią między różnymi kształtami, które są wymieniane między sobą przez wibracje sfery kompleksowania.
Wielościany koordynacyjne są ogólnie opisywane w publikacjach naukowych przez długość wiązań chemicznych między centralnym kationem M i jego ligandami X oraz przez kąty między tymi wiązaniami. Długość wiązań zależy od rozpatrywanych związków chemicznych: w czworościanie SiO 4 wiązania Si-O mają zazwyczaj długość 1,60 Å , podczas gdy średnie wiązania BO w czworościanie BO 4 wahają się od 1,44 Å do 1, 53 Å . Z tego powodu najpierw używamy kątów wiązania do określenia wielościanu koordynacyjnego. Długości wiązań są najbardziej przydatne do obliczania efektywnej liczby koordynacyjnej atomu lub do uwzględnienia krotności wiązania między kationem metalu a ligandem.
W przypadku odkształcenia wielościanu koordynacyjnego, to znaczy, gdy obserwowane kąty wiązań znacznie odbiegają od wartości oczekiwanych dla wielościanu regularnego, nie zawsze łatwo jest od razu rozpoznać wielościan koordynacja atomu. Na przykład wielościan koordynacyjny miedzi CuO 5 może być tetragonalną piramidą w nadprzewodniku YBa 2 Cu 3 O 7lub bipiramidy trygonalnej w olivenicie Cu 4 (AsO 4 ) 2 (O), ale jest tak zniekształcona w Cu 2 P 2 O 7że jest w połowie drogi między nimi. Obliczenie dwuściennych kątów wielościanu koordynacyjnego między normalnymi z dwoma sąsiednimi ścianami pozwala w pewnych trudnych przypadkach usunąć wątpliwości. Każda krawędź wielościanu koordynacyjnego odpowiada kątowi dwuściennemu. Poniższa tabela podaje kąty wiązania i kąty dwuścienne dla niektórych wyidealizowanych wielościanów koordynacyjnych, dla których wszystkie długości wiązań MX są równe (wielościany koordynacyjne niekoniecznie są regularne, patrz przypadek dwupiramidy trygonalnej).
| Wielościan | Kąty wiązania XMX | Kąty dwuścienne |
|---|---|---|
| kwadrat | 90 ° (× 4) | 0 ° (× 4) |
| czworościan | 109,5 ° (× 4) | 109,5 ° (x 6) |
| piramida czterokątna | 90 ° (× 8) | 0 ° (× 1), 75,7 ° (× 4), 119,8 ° (× 4) |
| bipiramidy trygonalne | 120 ° (× 3), 90 ° (× 6) | 53,1 ° (× 3), 101,5 (× 6) |
| sześcian | 70,5 ° (x 12) | 90 ° (× 12) |
| oktaedr | 90 ° (× 12) | 70,5 ° (x 12) |
Czynniki determinujące wielościany koordynacyjne
W przypadku centralnej substancji chemicznej i jej określonych ligandów liczba możliwych koordynacyjnych wielościanów jest ograniczona kilkoma czynnikami, związanymi z regułami Paulinga .
Wpływ promieni jonowych
| Wielościan | Iloraz krytyczny |
|---|---|
| trójkąt równoboczny |
|
| czworościan | |
| kwadratowy ośmiościan |
|
| pryzmat trygonalny |
|
czworokątny antypryzmat |
|
| sześcian | |
| dwudziestościan | |
kuboctaedr , antykuboctaedr |
W uproszczonym opisie geometrycznym rdzeń chemiczny (zwykle kation ) i jego ligandy (zwykle aniony ) są odpowiednio uważane za twarde kule promieni jonowych i . Opis ten jest szczególnie ważny dla ligandów jednoatomowych. W przypadku ligandów wieloatomowych, takich jak bipirydyny , można rozważyć tylko atomy w bezpośrednim kontakcie z centralną substancją chemiczną; jednakże kształt cząsteczki liganda wpłynie na wielkość koordynującego wielościanu.
Ligandy są w kontakcie z centralnymi związkami chemicznymi. Mogą również wpływać na inne sąsiednie ligandy, ale niekoniecznie. Wielkość miejsca utworzonego przez stykające się ligandy w koordynacyjnym wielościanie wyznacza dolną granicę dla wielkości osadzającego się w nim kationu. Kation nie może zostać osadzony w miejscu utworzonym przez ligandy, jeśli jego rozmiar jest mniejszy niż miejsce, ponieważ w tym przypadku nie ma on bezpośredniego kontaktu z ligandami: przeważają odpychanie elektrostatyczne między ligandami. I struktura kryształu jest nie jest już stabilny.
Obliczenie ilorazu promieni jonowych pozwala wyznaczyć prawdopodobny wielościan koordynacyjny związku chemicznego: wystarczy porównać z ilorazami „krytycznymi” dla wszystkich wielościanów koordynacyjnych. Poza tym rozważany wielościan koordynacyjny nie jest już stabilny i jest prawdopodobne, że związki chemiczne zaadoptują środowisko z wyższym ilorazem krytycznym. Na przykład, w przypadku kwarcu SiO 2 , kation Si 4+ ma promień jonowy 0,41 Å, a anion O 2– ma promień jonowy 1,40 Å , iloraz wynosi 0,293, a koordynacyjny wielościan krzemowy to SiO 4 czworościany .
Wielościany koordynacyjne wysokiego ilorazu krytycznego generalnie odpowiadają wysokiej koordynacji, jednak koordynacja niekoniecznie rośnie wraz z ilorazem krytycznym: kwadrat (koordynacja 4) i ośmiościan (koordynacja 6) mają ten sam iloraz krytyczny.
Iloraz krytyczny jest charakterystyczny dla rozpatrywanego wielościanu koordynacyjnego i można go dokładnie obliczyć w prosty sposób.
Rozważmy na przykład przypadek koordynacji typu płaszczyzny kwadratowej.
Środki ligandów tworzą z boku kwadrat . Wystarczy wyznaczyć krawędź wielościanu koordynacyjnego i jego połowę przekątną w funkcji promieni jonowych i :
Zastępując wyrażeniem w funkcji , otrzymujemy
stąd iloraz krytyczny
Przedstawiona tutaj metoda obliczania ilorazu krytycznego dla kwadratu działa również dla pozostałych wielościanów koordynacyjnych.
Wpływ stopni utlenienia
Zmiana stopnia utlenienia substancji chemicznej wpływa na jej wielościan koordynacyjny. Wpływ stopnia utlenienia na środowisko chemiczne nie jest trywialny. Z jednej strony kation o wysokim stopniu utlenienia będzie miał tendencję do przyciągania dużej liczby anionów w celu skompensowania ładunków elektrostatycznych. Z drugiej strony, promień jonowy kationu zmniejsza się, gdy traci on więcej elektronów , faworyzując wielościan koordynacyjny o niższym ilorazie krytycznym. Wreszcie, dla tego samego stopnia utlenienia, substancja chemiczna może mieć kilka różnych koordynacyjnych wielościanów.
Istnieją jednak korelacje między stopniem utlenienia a wielościanem koordynacyjnym, zwłaszcza w przypadku metali przejściowych :
- przypadek wanadu :
- kation V 3+ ma oktaedryczną koordynację anionów O 2– ;
- kation V 4+ o spinie 1/2 może występować w tetragonalnej lub oktaedrycznej piramidalnej koordynacji O 2– ;
- kation V 5+ może mieć koordynację tetraedryczną, tetragonalną piramidalną lub O 2– oktaedryczną ;
- obudowa miedzi :
- koordynacyjny wielościan kationu Cu + jest liniowy (grupy CuO 2 w miedziycie Cu 2 O, półprzewodnik YBa 2 Cu 3 O 6) Lub tetraedryczne (CuS 4 grupy w Cu 2 FeSnS 4 stannin);
- Koordynacyjny wielościan kationu Cu 2+ (spin 1/2) jest bardzo często płaszczyzną kwadratową (grupy CuO 4 w BaCuSi 2 O 6), tetragonalna piramida (grupy CuO 5 w nadprzewodniku YBa 2 Cu 3 O 7), ośmiościan (grupy CuCl 4 (H 2 O) 2w mitscherlichite K 2 CuCl 4 2H 2 O) lub rzadziej bipiramidy trygonalnej (grupy CuO 5 w olivenicie Cu 4 (AsO 4 ) 2 (O)). W przypadku Cu 2+ , w Efekt Jahna-Tellera prowadzi do silnej deformacji wielościanu koordynacyjnej poza kwadrat.
W przypadku kompleksów w roztworze wpływ stopnia utlenienia jest często interpretowany za pomocą argumentów orbitalnych. Na przykład koordynacja miedzi (II) to zdeformowany ośmiościan (wydłużenie symetrii D 4h na skutek efektu Jahna Tellera). Tak jest na przykład w przypadku Cu (NH 3 ) 4 (H 2 O) 22+ . Natomiast miedź (I) ma koordynację liniową. Tak jest w przypadku organocuprates Cu (CH 3 ) 2- . To samo dotyczy srebra (I) z odczynnikiem Tollens Ag (NH 3 ) 2+ i kompleksy złota (I).
Odkształcenie wielościanu koordynacyjnego
Odkształcenie wielościanu koordynacyjnego MX n wynika głównie z odchylenia kątów wiązań XMX od kątów wyidealizowanych wielościanów oraz z rozkładu długości wiązania, ale także z rozkładu odległości między ligandami.
Koordynacja czworościenna
Do opisu odkształcenia czworościanu MX 4 powszechnie stosuje się trzy bezwymiarowe parametry :
- BLD ( zniekształcenie długości wiązania ):
- AD ( zniekształcenie kątowe ):
- ELD ( zniekształcenie długości krawędzi ):
Uwagi i odniesienia
- (in) LW Finger , RM Hazen i RJ Hemley , „ BaCuSi 2 O 6: Nowy cyklokrzemian z czteroczłonowymi pierścieniami czworościennymi ” , Am. Mineral. , vol. 74, n kość 7-8,1989, s. 952-955 ( czytaj online )
- (en) SR Hall , JT Szymanski i JM Stewart , „ Kesterite, Cu 2 (Zn, Fe) SnS 4i stannit, Cu 2 (Fe, Zn) SnS 4, strukturalnie podobne, ale odrębne minerały ” , kan. Minerał. , vol. 16 N O 21978, s. 131-137
- Ta tabela została częściowo wzięta z angielskiego artykułu Coordination geometry w wersji z 5 listopada 2010 r .
- (w) JL Hoard , „ Struktura krystaliczna srebrnego cyjanku potasu ” , Zeitschrift für Kristallographie, Kristallgeometrie, Kristallphysik, Kristallchemie , vol. 84,1933, s. 231-255
- (en) JK Nimmo i BW Lucas , „ A neutron dyfraction określanie struktury krystalicznej fazy α azotanu potasu w 25 stopniach C i 100 stopniach C ” , J. Phys. C: ciało stałe , vol. 6, N O 21973, s. 201-211 ( DOI 10.1088 / 0022-3719 / 6/2/001 )
- (w) H. Chessin , WC Hamilton i B. Post , " Położenie i parametry termiczne atomów tlenu w kalcycie " , Acta Cryst. , vol. 18 N O 4,1965, s. 689-693 ( DOI 10.1107 / S0365110X65001585 )
- Miessler i Tarr, str. 423.
- (De) R. Brill , C. Hermann i Cl. Peters , „ Studien über chemische Bindung mittels Fourieranalyse III. Die Bindung im Quarz ” , Naturwissenschaften , vol. 27 N O 40,1939, s. 676-677 ( DOI 10.1007 / BF01494994 , czytaj online )
- Miessler i Tarr, str.424.
- (w) S. Åsbrink i LJ Norrby , „ Udokładnienie struktury krystalicznej tlenku miedzi (II) z omówieniem niektórych wyjątkowych esd ” , Acta Cryst. B , tom. 26, n o 1,1970, s. 8-15 ( DOI 10.1107 / S0567740870001838 )
- (in) ARHF Ettema i RA de Groot , „ Obliczenia struktury pasmowej heksagonalnej i sześciennej fazy K 3 Sb ” , J. Phys.: Condens. Materia , tom. 11 N O 3,1999, s. 759-766 ( DOI 10.1088 / 0953-8984 / 11/3/015 , czytaj online )
- Miessler i Tarr, str. 375.
- J.-C. Bouloux i J. Galy , „ Struktura krystaliczna hipowanadanu CaV 4 O 9 », Acta Cryst. B , tom. 29 N O 6,1973, s. 1335-1338 ( DOI 10.1107 / S0567740873004462 )
- (w) Paul B. Moore i S. John Louisnathan , „ Struktura krystaliczna fresnoitu, Ba 2 (TiO) Jeśli 2 O 7 " , Z. Kristall. , vol. 130, n kość 1-61969, s. 438-448 ( DOI 10.1524 / zkri.1969.130.1-6.438 , czytaj online )
- (De) M. Straumanis i A. Ieviņš , „ Die Gitter konstanten des NaCl und des Steinsalzes ” , Zeitschrift für Physik , vol. 102, n kość 5-6,1936, s. 353-359 ( DOI 10.1007 / BF01339176 )
- (w) FJ Gotor , C. Real , MJ Dianez i JM Criado , „ Relacje między teksturą i strukturą BaTiO 3 a jego tetragonalną sześcienną → przejściową entalpią ” , J. Solid State Chem. , vol. 123 n O 21996, s. 301-305 ( DOI 10.1006 / jssc.1996.0183 )
- (w) Robert Leubolt , Herbert IPSER , Peter Terzieff i Kurt L. Komarek , „ Nonstechiometry in B8-type NiSb ” , Z. Anorg. Allg. Chem. , vol. 533 n O 21986, s. 205-214 ( DOI 10.1002 / zaac.19865330226 )
- R. Souane (2005) Synteza i właściwości kompleksowania w odniesieniu do jonu uranylowego pochodnych karboksylowych p-tert-butylokaliksu [6] areny. Praca doktorska na Uniwersytecie L. Pasteura w Strasburgu. s. 90 http://scd-theses.u-strasbg.fr/933/01/these-souane.pdf
- (w) RP Dodge , GS Smith , Q. Johnson i RE Elson , „ Struktura krystaliczna pentachlorku protaktyny ” , Acta Cryst. , vol. 22, n o 1,1967, s. 85-89 ( DOI 10.1107 / S0365110X67000155 )
- P. Aldebert i JP Traverse , „ Badanie metodą dyfrakcji neutronów struktur wysokotemperaturowych La 2 O 3nd 2 O 3 ”, Biuletyn Badań Materiałowych , t. 14 N O 3,Marzec 1979, s. 303-323 ( DOI 10.1016 / 0025-5408 (79) 90095-3 )
- (w) Wheeler P. Davey , " Precyzyjne pomiary halogenków alkalicznych kryształów " , Phys. Obrót silnika. , vol. 21 N O 21923, s. 143-161 ( DOI 10.1103 / PhysRev.21.143 )
- (en) Takeshi Asai , Kunio Nishida i Shichio Kawai , „ Synteza i przewodnictwo jonowe Cu x Li 3-x N ” , Biuletyn Badań Materiałowych , t. 19 N O 10,Październik 1984, s. 1377-1381 ( DOI 10.1016 / 0025-5408 (84) 90203-4 )
- (de) R. Hoppe i B. Mehlhorn , „ Die Kristallstruktur von K 2 ZrF 6 » , Z. Anorg. Allg. Chem. , vol. 425 n O 3,1976, s. 200-208 ( DOI 10.1002 / zaac.19764250303 )
- (w) BF Decker i JS Kasper , „ Struktura ferrytu wapnia ” , Acta Cryst. , vol. 10 N O 4,1957, s. 332-337 ( DOI 10.1107 / S0365110X5700095X )
- (en) JP Laval i A. Abouz , „ Krystalochemia nadmiaru anionu ReO 3 powiązane fazy artykułu: Struktura krystaliczna β-PrZr 3 F 15 » , J. Solid State Chem. , vol. 96 N O 21992, s. 324-331 ( DOI 10.1016 / S0022-4596 (05) 80266-X )
- (in) AP Agron i WR Busing , " Sześciowodzian dwuchlorku wapnia i strontu metodą dyfrakcji neutronów " , Acta Cryst. C , tom. 42 N O 21986, s. 141-143 ( DOI 10.1107 / S0108270186097007 )
- (w) WB Pearson , „ Cu 2 Sb i powiązane struktury ” , Z. Kristall. , vol. 171 n kości 1-2,1985, s. 23-29 ( DOI 10.1524 / zkri.1985.171.1-2.23 )
- (w) S. Samson , „ Struktura krystaliczna związku międzymetalicznego Mg 3 Cr 2 Al 18 » , Acta Cryst. , vol. 11 N O 12,1958, s. 851-857 ( DOI 10.1107 / S0365110X58002425 )
- (en) Sebastian Prinz , Karine M. Sparta i Georg Roth , „ The difyllosilicate Rb 2 (VO) 2 [Si 8 O 19 ]” » , Acta Cryst. C , tom. 64, n o 3,2007, i27-i29 ( DOI 10.1107 / S0108270107068205 )
- (De) Th. Hahn , " Silikate - Struktur, Eigenschaften und Technische Nutzung " , Fakultät für Bergbau und Hüttenwesen der RWTH-Aachen, Technische Mitteilungen , vol. 56 N O 12,1963, s. 501-509
- (od) E. Zobetz , „ Geometrische Größen und für einfache Modellrechnungen BO 4 -Gruppen ” , Z. Kristall. , vol. 191, n kość 1-2,1990, s. 45–57 ( DOI 10.1524 / zkri.1990.191.1–2.45 )
- C. Michel i B. Raveau , „ Oxides A 2 BaCuO 5(A = Y, Sm, Eu, Gd, Dy, Ho, Er, Yb) ”, J. Solid State Chem. , vol. 43, n o 1,1982, s. 73-80 ( DOI 10.1016 / 0022-4596 (82) 90216-X )
- (en) BE Robertson i C. Calvo , „ Struktura krystaliczna i przemiana fazowa α-Cu 2 P 2 O 7 » , Acta Cryst. , vol. 22 N O 5,1967, s. 665-672 ( DOI 10.1107 / S0365110X6700132X )
- (w :) EL Muetterties i LJ Guggenberger , „ Idealized Polytopal Forms. Opis rzeczywistych cząsteczek odniesionych do wyidealizowanych wielokątów lub wielościanów w postaci geometrycznej ścieżki reakcji ” , J. Am. Chem. Soc. , vol. 96, n o 6,1974, s. 1748-1756 ( DOI 10.1021 / ja00813a017 )
- (en) RD Shannon , „ efektywne promienie jonowe Zrewidowane i systematyczne badania odległości międzyatomowych w halogenki i Chalcogenides ” , Acta Cryst. A , tom. 32,1976, s. 751-767 ( DOI 10.1107 / S0567739476001551 )
- (in) Schindler , FC Hawthorne i WH Baur , „ Crystal Chemical Aspects of Vanadium: Polyhed Geometries, Characteristic Bond Valences, and Polymerization of (VO n ) Polyhedra ” , Chem. Mater. , vol. 12 N O 5,2000, s. 1248-1259 ( DOI 10.1021 / cm990490y , czytaj online )
- (en) A. Restori i D. Schwarzenbach , „ Charge density in cuprite, Cu 2 O ” , Acta Cryst. B , tom. 42, n o 3,1986, s. 201-208 ( DOI 10.1107 / S0108768186098336 )
- (en) Mary F. Garbauskas , RW Green , RH Arendt i JS Kasper , „ Badanie rentgenowskie miedzianu itru i baru YBa 2 Cu 3 O 6 » , Inorg. Chem. , vol. 27 N O 5,1988, s. 871-873 ( DOI 10.1021 / ic00278a024 )
- (w) B. Renner i G. Lehmann , " Korelacja zniekształcenia kątowego długości i skoku TO 4 jednostki w kryształach " , Z. Kristall. , vol. 175, n kość 1-2,1986, s. 43-59 ( DOI 10.1524 / zkri.1986.175.1-2.43 )















![{\ displaystyle {\ begin {array} {l} a = 2r_ {a} \\ [1ex] \ displaystyle {\ frac {a {\ sqrt {2}}} {2}} = r_ {a} + r_ { c} \ end {tablica}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7d21c80ce20a5840896f192edd5cdad19813e2f6)








