Odczynnik Lawessona
| Odczynnik Lawessona | |
| Identyfikacja | |
|---|---|
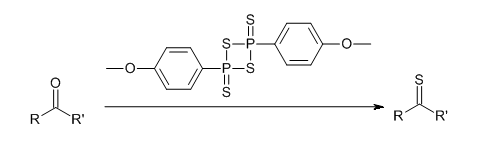
| Nazwa IUPAC | 2,4-bis (4-metoksyfenylo) -1,3-ditia-2,4-difosfetano 2,4-disiarczek |
| N O CAS | |
| N O ECHA | 100,038,944 |
| N O WE | 242-855-4 |
| PubChem | 87949 |
| UŚMIECHY |
COC1 = CC = C (C = C1) P2 (= S) SP (= S) (S2) C3 = CC = C (C = C3) OC , |
| InChI |
InChI: InChI = 1S / C14H14O2P2S4 / c1-15-11-3-7-13 (8-4-11) 17 (19) 21-18 (20,22-17) 14-9-5-12 ( 16-2) 6-10-14 / h 3-10H, 1-2H3 |
| Właściwości chemiczne | |
| Brute formula |
C 14 H 14 O 2 P 2 S 4 [Izomery] |
| Masa cząsteczkowa | 404,467 ± 0,033 g / mol C 41,57%, H 3,49%, O 7,91%, P 15,32%, S 31,71%, |
| Właściwości fizyczne | |
| T ° fuzja | 229 ° C |
| Jednostki SI i STP, chyba że określono inaczej. | |
Przez odczynnik Lawessona to związek chemiczny środek organiczny stosowany jako tionowanie . Spopularyzował go Sven-Olov Lawesson, który jednak nie jest jego wynalazcą.
Odczynnik Lawessona jest bardziej reaktywny niż odczynnik Belleau , ale mniej niż odczynniki Davy'ego .
Thionation
Reakcja tionowania przekształca karbonyl w tiokarbonyl . Odczynnik Lawessona jest najczęściej stosowanym odczynnikiem, ponieważ umożliwia pracę w wyższych temperaturach niż siarkowodór i jest lepiej rozpuszczalny w rozpuszczalnikach organicznych niż pentasiarczek difosforu .
Mechanizm
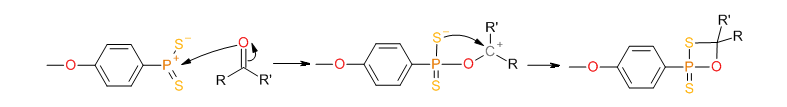
Aktywne miejsca cząsteczki są aktywowane przez otwarcie centralnego pierścienia utworzonego przez fosfor i siarkę. To otwieranie odbywa się głównie za pomocą środków termicznych:
Również zaktualizowane ylidy ditiofosfinowe mogą reagować z grupą karboksylową, tworząc półprodukt tiaoksafosfetanowy:
Utworzenie stabilnego podwójnego wiązania P = O przesuwa reakcję w prawo i prowadzi do rozdzielenia półproduktu:
Ta reakcja przypomina reakcję Wittiga i dotyczy ketonów , amidów i laktamów . Ponieważ estry reagują w bardziej agresywnych warunkach reakcji, możliwe jest przeprowadzenie selektywnych tionacji.
Produkcja i synteza
Odczynnik Lawessona jest syntetyzowany z anizolu i pentasiarczku difosforu .

Zobacz też
Uwagi i odniesienia
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- (w) „ Lawesson's Reagent ” on ChemIDplus , dostęp 18 stycznia 2010
- (w) T. Molina , Mr. Yanez , O. MB , R. Notario and J.-LM Abboud , The thiocarbonyl group , Chichester / New York / Brisbane etc., John Wiley & Sons Ltd, al. „Chemia grup funkcyjnych / Chemia podwójnie wiązanej grupy funkcyjnej”,1997, 1858 s. ( ISBN 0-471-95956-1 )
- „ Odczynnik Lawessona. Przygotowanie, mechanizm działania, zastosowania, notatki ” , na boowiki.info (dostęp 17 lutego 2021 )
- (w) Martin Jesberger , Thomas P. Davis i Leonie Barner , „ Zastosowania odczynnika Lawessona w syntezach organicznych i organometalicznych ” , Synthesis , Vol. 13,Marzec 2003
- Thomsen, I.; Clausen, K.; Scheibye, S.; Lawesson, S.-O. , Thiation with 2,4-Bis (4-metoxyphenyl) -1,3,2,4-Dithiadiphosphetane 2,4-disulfide: N-Methylthiopyrrolidone , Org. Synth. , pot. „lot. 7 ",1990, s. 372