Chlorometan
| Chlorometan | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Struktura chlorometanu |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identyfikacja | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nazwa IUPAC | chlorometan | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonimy |
Chlorek metylu |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O ECHA | 100,000,744 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O WE | 200-817-4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 6327 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 36014 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| UŚMIECHY |
CCl , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / CH3Cl / c1-2 / h1H3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Wygląd | bezbarwny gaz o słodkawym zapachu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości chemiczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Brute formula |
C H 3 Cl [Izomery] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa cząsteczkowa | 50,488 ± 0,003 g / mol C 23,79%, H 5,99%, Cl 70,22%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości fizyczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuzja | -97,6 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| * Temperatura wrzenia | -24,2 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rozpuszczalność | 5 g · l -1 ( woda , 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
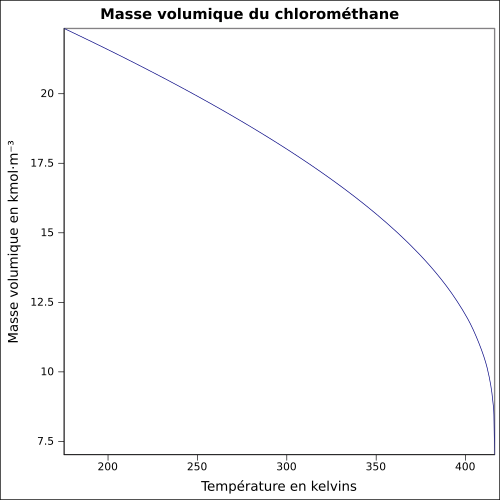
| Masa objętościowa |
2,3065 g · l -1 ( 0 ° C , 1013 mbar )
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura samozapłonu | 632 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Granice wybuchowości w powietrzu | 7,6 - 19 % obj | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nasycenie prężności par |
4,896 bar przy 20 ° C 6,6 bar przy 30 ° C 10,9 bar przy 50 ° C równanie:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punkt krytyczny | 143 ° C , 66,7 bar , 0,353 kg · l -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Potrójny punkt | -97,71 ° C , 0,00876 bar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termochemia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gaz S 0 , 1 bar | 234,36 J · K -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 ciecz, 1 bar | 140,08 J · K -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gaz Δ f H 0 | -83,68 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 ciecz | -102,4 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 6,431 kJ · mol -1 do 175,44 K. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 20,5 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
81,2 J · K- 1 · mol -1 do 298 K.
równanie:
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | -764,0 kJ · mol -1 (gaz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Właściwości elektroniczne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 energia re jonizacji | 11,22 ± 0,01 eV (gaz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Środki ostrożności | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   Niebezpieczeństwo H220, H351, H373, H220 : Skrajnie łatwopalny gaz H351 : Podejrzewa się, że powoduje raka (wskazać drogę narażenia, jeżeli definitywnie udowodniono, że żadna inna droga narażenia nie powoduje takiego samego zagrożenia) H373 : Może powodować uszkodzenie narządów (wskazać wszystkie dotknięte narządy, jeśli są znane) po powtórzonych narażenie lub narażenie długotrwałe (wskazać drogę narażenia, jeżeli definitywnie udowodniono, że żadna inna droga narażenia nie prowadzi do tego samego zagrożenia) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 2 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
23 : gaz łatwopalny Numer UN : 1063 : CHLOREK METYLU; lub GAZ CHŁODNICZY R 40 Klasa: 2.1 Etykieta: 2.1 : Gazy łatwopalne (odpowiada grupom oznaczonym dużą literą F); Pakowanie: -  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klasyfikacja IARC | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupa 3: Nie podlega klasyfikacji ze względu na jego rakotwórczość dla ludzi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoksykologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | 1,8 g · kg -1 (szczur, doustnie ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 0.91 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Próg zapachu | niska: 10 ppm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednostki SI i STP, chyba że określono inaczej. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Metylu , znany także jako chlorek metylu , Freon 40 i R 40 , jest związek chemiczny o wzorze CH 3 Cl. Jest to czynnik chłodniczy, który jest również używany jako odczynnik w wielu syntezach.
Biogeneza i obecność w przyrodzie
W fluorowcoalkany ( gatunki zawierające obligacji węgla - atom chlorowca ) są wytwarzane - prawdopodobnie za pomocą różnych procesów biologicznych - niektórych grzybów, zwierząt i roślin. Cząsteczka CH 3 Cl został zatem zaproponowany jako możliwy marker życia w przypadku wykrycia go w atmosferach skalistych egzoplanet.
Słona roślin Batis maritima się powoduje enzym chlorkiem metylu transferazą , który katalizuje syntezę CH 3 Cl-adenozyny z S-L-metioniny i chloru. To białko oczyszczono, a następnie wprowadzany i ekspresjonowany przez inżynierię genetyczną w bakterii E. coli . Wydaje się również, że jest aktywny w mikro-grzybach, takich jak Phellinus pomaceus , krasnorosty (np. Endocladia muricata ) lub gatunki roślin, które stają się lokalnie inwazyjne , Mesembryanthemum crystallinum , wszystkie znane również z wytwarzania CH 3 Cl. Model laboratoryjny Arabidopsis thaliana .
Obecność we wszechświecie
W 2017 roku cząsteczka CH 3 Clzostał wykryty w Układzie Słonecznym i poza nim . Najpierw przez interferometr ALMA wokół protostar od typu słonecznego IRAS16293-2422 w regionie, w którym planety mogą tworzyć. Następnie za pomocą spektrometru ROSINA (na pokładzie sondy Rosetta ) na komecie 67P / Tchourioumov-Guérassimenko .
Odkrycie CH 3 Clw miejscach poprzedzających (znane) pochodzenie życia wskazuje, że do stwierdzenia obecności życia na innych planetach będą musiały być użyte inne, bardziej ostateczne biomarkery. Z drugiej strony halogenoorganiczne mogą stanowić element zrozumienia chemii związanej z powstaniem życia.
Właściwości fizykochemiczne
Chlorometan są hydrolizowane przez wodę w wysokiej temperaturze w celu metanolu CH 3 OHi chlorowodór HCl:
CH 3 Cl+ H 2 O→ CH 3 OH+ HCl .Ta reakcja jest katalizowana przez związki alkaliczne. Odwrotna reakcja umożliwia syntezę CH 3 Clprzez przepuszczanie chlorowodoru w metanolu, w ewentualnej obecności chlorku cynkowego ZnCI 2jako katalizator lub w reakcji metanolu i chlorowodoru w temperaturze 350 ° C z tlenkiem glinu Al 2 O 3 :
CH 3 OH+ HCl → CH 3 Cl+ H 2 O.W niższych temperaturach chlorek metylu tworzy hydrat z wodą, co jest problemem w systemach chłodniczych.
posługiwać się
Chlorometan służy do wytwarzania dimetylodichlorosilanu Si (CH 3 ) 2 Cl 2poprzez syntezę Müllera-Rochowa :
2 CH 3 Cl+ Si → Si (CH 3 ) 2 Cl 2.Jest to ważny szlak syntetyczny do produkcji silikonów .
Jest również stosowany jako odczynnik w reakcji Wurtza-Fittiga lub reakcji Friedela-Craftsa wykorzystywanej do produkcji alkilobenzenów. Jest ważnym odczynnikiem do metylacji, w szczególności amin do tworzenia czwartorzędowych metyloamin lub grup hydroksylowych do eterów .
Produkcja i synteza
Gaz ten jest wytwarzany przez chlorowanie w metan z chloru gazu o 400 do 500 ° C . Mechanizm chlorowania to rodnikowa reakcja łańcuchowa poprzez rodniki wynikające z dysocjacji chloru. Dysocjację tę można uzyskać termicznie, fotochemicznie lub za pomocą katalizatorów. Preferowana jest trasa termiczna, która prowadzi do serii następujących po sobie podstawień:
CH 4 + Cl 2 → CH 3 Cl + HCl CH 3 Cl + Cl 2 → CH 2 Cl 2 + HCl CH 2 Cl 2 + Cl 2 → CHCI 3 + HCl CHCI 3 + Cl 2 → Cl 4 + HClWynikiem tej serii reakcji jest mieszanina chlorometanu, dichlorometanu , chloroformu i czterochlorku węgla . Te związki są następnie oddzielane przez destylację . W reaktorze wykorzystuje się nadmiar metanu, a recykling stosuje się w obecności gazu obojętnego, aby uniknąć pracy na polu, na którym mieszanina metanu i chloru jest wybuchowa.
Inny sposób syntezy jest hydrochlorowanie z metanolu chlorowodorem. Ta reakcja jest obecnie preferowana, ponieważ zużywa chlorowodór, który jest trudnym do usunięcia produktem ubocznym, zamiast go wytwarzać, jak w przypadku chlorowania. Ponadto w wyniku syntezy powstaje sam chlorometan i unika się wytwarzania związków wielochlorowych.
Uwagi i odniesienia
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- CHLOREK METYLU , karta (e) bezpieczeństwa Międzynarodowego Programu Bezpieczeństwa Chemicznego , konsultacja 9 maja 2009
- Wpis "Chlorek metylu" w chemicznej bazie danych GESTIS IFA (niemieckiego organu odpowiedzialnego za bezpieczeństwo i higienę pracy) ( niemiecki , angielski ), dostęp 2 lutego 2010 r. (Wymagany JavaScript)
- (en) Robert H. Perry i Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 s. ( ISBN 0-07-049841-5 ) , str. 2-50
- (en) "Chlorek metylu" , w NIST / WebBook , skonsultowano
- (w) Carl L. Yaws, Podręcznik diagramów termodynamicznych , t. 1, 2 i 3, Huston, Texas, Gulf Pub. Współ.,1996( ISBN 0-88415-857-8 , 0-88415-858-6 i 0-88415-859-4 )
- (w) David R. Lide, Podręcznik chemii i fizyki , Boca Raton, CRC,2008, 89 th ed. , 2736 str. ( ISBN 978-1-4200-6679-1 ) , str. 10-205
- Grupa robocza IARC ds. Oceny ryzyka rakotwórczości dla ludzi, „ Evaluations Globales de la Carcinogenicité pour l'Homme, Groupe 3: Unclassables as to ich rakotwórczość dla ludzi ” , na http://monographs.iarc.fr , IARC,16 stycznia 2009(dostęp 22 sierpnia 2009 )
- Numer indeksu w tabeli 3.1 załącznika VI do rozporządzenia WE nr 1272/2008 (16 grudnia 2008)
- (in) „ Chlorek metylu ” na ChemIDplus , dostęp
- „ Chlorek metylu ” , na hazmap.nlm.nih.gov (dostęp: 14 listopada 2009 )
- „Chloromethane” , w ESIS , dostęp 2 lutego 2010
- Ni X, Hager LP, „ cDNA Cloning of Batis maritima Methyl Chloride Transferase and Purification of the Enzyme ”, Proc Natl Acad Sci USA , vol. 95 N O 221998, s. 12866–71 ( PMID 9789006 , PMCID 23635 , DOI 10.1073 / pnas.95.22.12866 )
- Ni X, Hager LP, „ Expression of Batis maritima Methyl Chloride Transferase in Escherichia coli ”, Proc Natl Acad Sci USA , vol. 96, n o 7,1999, s. 3611–5 ( PMID 10097085 , PMCID 22342 , DOI 10.1073 / pnas.96.7.3611 )
- Nagatoshi Y, Nakamura T (2007) „Charakterystyka trzech halogenków metylotransferaz u Arabidopsis thaliana” . Plant Biotechnol. 24: 503–506. doi: 10.5511 / plantbiotechnology.24.503.
- „ Pierwsze wykrycie Freonu-40 w ośrodku międzygwiazdowym z ALMA i Rosetta ” , na CNRS ,2 października 2017 r(dostęp 11 października 2017 ) .
- (en) Edith C. Fayolle, Karin I. Öberg, K. Jes Jørgensen, Kathrin Altwegg, Hannah Calcutt i wsp. , „ Protostellar and cometary detections of organohalogens ” , Nature Astronomy , tom. 1,2017, s. 703-708 ( DOI 10.1038 / s41550-017-0237-7 ).
- (en) Manfred Rossberg Wilhelm Lendle Gerhard Pfleiderer Adolf TÖGEL Eberhard-Ludwig Dreher Ernst Langer Heinz Rassaerts Peter Kleinschmidt Heinz Strack Richard Cook Uwe Beck Karl sierpnia Lipper, Theodore R. Torkelson, Eckhard Löser, Klaus K. Beutel, Trevor Mann, Chlorinated Hydrocarbons , Wiley-VCH Verlag GmbH & Co., al. „Encyklopedia chemii przemysłowej Ullmanna”,15 lipca 2006( DOI 10.1002 / 14356007.a06_233.pub2 )