Acenaphthene
| Acenaphthene | |||
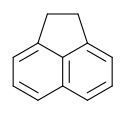  Struktura acenaftenu. |
|||
| Identyfikacja | |||
|---|---|---|---|
| Nazwa IUPAC | 1,2-dihydroacenaftylen | ||
| Synonimy |
1,8-ethylenenaphthalene |
||
| N O CAS | |||
| N O ECHA | 100,001,336 | ||
| N O WE | 201-469-6 | ||
| N O RTECS | AB1000000 | ||
| PubChem | 6734 | ||
| UŚMIECHY |
c2cc1cccc3c1c (c2) CC3 , |
||
| InChI |
InChI: InChI = 1 / C12H10 / c1-3-9-4-2-6-11-8-7-10 (5-1) 12 (9) 11 / h1-6H, 7-8H2 |
||
| Wygląd | Krystaliczny proszek o barwie białej do żółtej | ||
| Właściwości chemiczne | |||
| Brute formula |
C 12 H 10 [Izomery] |
||
| Masa cząsteczkowa | 154,2078 ± 0,0103 g / mol C 93,46%, H 6,54%, |
||
| Podatność magnetyczna | 109,3 × 10-6 cm 3 · mol -1 | ||
| Właściwości fizyczne | |||
| T ° fuzja | 93,4 ° C | ||
| * Temperatura wrzenia | 279 ° C | ||
| Rozpuszczalność |
3,9 mg · l -1 ( woda , 25 ° C ) 36,52 mg · g -1 ( etanol , 25,05 ° C ) 31,10 mg · g -1 ( propan-2-ol , 24,92 ° C ) 50,40 mg · g -1 ( butan-1-ol , 25,1 ° C ) 401,70 mg · g -1 ( toluen , 25,08 ° C ) |
||
| Masa objętościowa | 1,222 g · cm -3 do 20 ° C | ||
| Temperatura samozapłonu | 450 ° C | ||
| Temperatura zapłonu | 135 ° C | ||
| Termochemia | |||
| S 0 stałe | 188,87 J · K -1 · mol -1 | ||
| Gaz Δ f H 0 | 156,8 kJ · mol -1 | ||
| Δ f H 0 stałe | 72 kJ · mol -1 | ||
| Δ fus H ° | 21,4622 kJ · mol -1 do 93,41 ° C | ||
| Δ vap H ° | 63,9 kJ · mol -1 do 25 ° C | ||
| C p |
185,27 J · K -1 · mol -1 (ciało stałe, 17,15 ° C ) 220,85 J · K -1 · mol -1 (gaz, 126,85 ° C ) |
||
| PCI | 6222 kJ · mol -1 | ||
| Właściwości optyczne | |||
| Współczynnik załamania światła | |||
| Środki ostrożności | |||
| SGH | |||
  Ostrzeżenie H315, H319, H335, H410, P261, P273, P305, P338, P351, P501, H315 : Działa drażniąco na skórę H319 : Działa drażniąco na oczy H335 : Może podrażniać drogi oddechowe H410 : Działa bardzo toksycznie na organizmy wodne, powodując długotrwałe skutki P261 : Unikać wdychania pyłu / dymu / gazu / mgły / par / aerozoli. P273 : Unikać uwolnienia do środowiska. P305 : W przypadku dostania się do oczu: P338 : Wyjąć soczewki kontaktowe, jeśli ofiara je nosi i jeśli można je łatwo zdjąć. Kontynuuj płukanie. P351 : Ostrożnie płukać wodą przez kilka minut. P501 : Zawartość / pojemnik usuwać do ... |
|||
| NFPA 704 | |||
| 1 2 1 | |||
| Transport | |||
90 : substancja zagrażająca środowisku, różne materiały niebezpieczne Numer UN : 3077 : MATERIAŁ ZAGRAŻAJĄCY ŚRODOWISKU, STAŁY, INO Klasa: 9 Nalepki: 9 : Różne materiały i przedmioty niebezpieczne 9.1 Opakowania: Grupa pakowania III : substancje niskiego zagrożenia.   |
|||
| Ekotoksykologia | |||
| CL 50 | 600 mg · kg -1 (szczur, ip ) | ||
| LogP | 3,92 | ||
| Związki pokrewne | |||
| Izomery | Acenaftylen | ||
| Jednostki SI i STP, chyba że określono inaczej. | |||
Acenaften jest policykliczne węglowodory aromatyczne (PAH), składa się z cząsteczki naftalenu z atomami węgla 1 i 8 są połączone za pomocą mostka etylenowego . Jest to uwodorniona forma acenaftylenu .
Jest składnikiem smoły , występuje również w węglu kamiennym oraz w bardzo małych ilościach w ropie naftowej .
Historia
Acenaften został po raz pierwszy odkryty przez Marcellina Berthelota w smole w 1867 roku, a następnie zsyntetyzowany z Bardy z α-etylonaftalenu.
Właściwości fizykochemiczne
Acenaften jest prawie nierozpuszczalny w wodzie, natomiast rozpuszcza się w benzenie , eterze , chloroformie i gorącym alkoholu .
Ten węglowodór reaguje z halogenami preferencyjnie w pozycjach 3, 5 i 6 lub nawet 1, w zależności od aktywacji. Na tych stanowiskach odbywa się również nitrowanie i sulfonowanie .
Do uwodorniania prowadzi catylique do formowania tétrahydroacénahtène i décahydroacénahtène natomiast utlenianie daje acenaftylenu , z kwasu naftalowego , na bezwodnik kwasu naftalowego , w acenaphthenequinone , w acénaphténol i acénaphténone .
posługiwać się
Acenaften jest wytwarzany w dużych ilościach w celu syntezy bezwodnika naftalowego przez utlenianie w fazie gazowej. Utlenianie prowadzi się w obecności powietrza, oraz katalizatora opartego na wanadu do 300 - 400 ° C . Kwas naftalenowy jest wytwarzana przez utlenianie w fazie ciekłej w obecności chromianu lub powietrza przy octanu manganu lub octanu kobaltu, na poziomie około 200 ° C . Kondensacja z propanodinitrylem daje kwas naftaleno-1,4,5,8-tetrakarboksylowy . Związki te są związkami pośrednimi do wytwarzania perylenu i perinonowe pigmentów .
Inne półprodukty do produkcji barwników lub farmaceutyków wykorzystują acenaften jako odczynnik: 4-bromacenaften do produkcji bezwodnika 4-bromonaftalowego , 5,6-dichloroacenaftenu i 3,5,6-trichloracenaftenu . Pigment fluorescencyjny Solvent yellow 44 jest wytwarzany przez bezwodnik 4-nitronaftalowy, który jest wynikiem nitrowania i utleniania acenaftenu.
Tworzywa sztuczne stabilne termicznie lub niepalne przez włączenie pochodnych acenaftenu podczas polimeryzacji .
Produkcja i synteza
Smoła zawiera około 0,3% acenaftenu i 2% acenaftylenu, które można przekształcić przez uwodornienie. Acenaften jest skoncentrowany we frakcji smoły o temperaturze wrzenia między 230 a 290 ° C do 25%. Drugą destylację przeprowadza się w celu uzyskania stężonego roztworu o temperaturze wrzenia między 270 a 275 ° C, a następnie przeprowadza się krystalizację w celu uzyskania technicznego acenaftenu (95-99%). Seria destylacji i rekrystalizacji pozwala na lepsze oczyszczenie produktu.
Zobacz też
Linki zewnętrzne
- (en) Metoda pobierania próbek i analizy (pobieranie próbek i analiza)
- (en) Arkusz danych chemicznych dotyczących gruntów
- (en) MSDS at Oxford University Strona Uniwersytetu Oksfordzkiego)
- (en) National Pollutant Inventory - Polycyclic Aromatic Hydrocarbon Fact Sheet
- (en) Wpis „Acenaphthene” z bazy bazy danych PAH
Bibliografia
- (w) Hyp Daubensee J., Jr., James D. Wilson and John L. Laity, „ diamagnetic Susceptibility Exaltation in Hydrocarbons ” , Journal of the American Chemical Society , tom. 91 N O 8,9 kwietnia 1968, s. 1991-1998
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- (i) W. M Haynes CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press / Taylor i Francis,2011, 91 th ed. , 2610 s. ( ISBN 978-143982-077-3 ) , str. 3-4
- (in) „ Acenaphtene ” na ChemIDplus , dostęp 18 stycznia 2010
- (w) Fang He i Pengbiao Liu , „ Rozpuszczalność acenaftylenu w różnych rozpuszczalnikach entre (278 i 323) K ” , Journal of Chemical & Engineering Data , tom. 52, n o 6,2007, s. 2536-2537
- Wpis „Acenaphthene” w bazie danych substancji chemicznych GESTIS IFA (niemieckiego organu odpowiedzialnego za bezpieczeństwo i higienę pracy) ( niemiecki , angielski ), dostęp 18 stycznia 2010 (wymagany JavaScript)
- (en) "Acenaphthene" , w NIST / WebBook , dostęp 18 stycznia 2010
- (w) Ying Duan Lei Raymond Chankalal Anita Chan i Frank Wania , „ przechłodzone ciśnienie ciekłej pary wielopierścieniowych węglowodorów aromatycznych ” , Journal of Chemical & Engineering Data , tom. 47, n o 4,2002, s. 801-806
- (w) JAR Cheda i EF Jr. Westrum , „ Subambient-Temperature Thermophysics of acenaphthene and acenaphthylene: Molecular Disorder in the Latter ” , The Journal of Physical Chemistry , tom. 98 N O 9,1994, s. 2482-2488
- SIGMA-ALDRICH
- (en) Karl Griesbaum, Arno Behr, Dieter Biedenkapp, Heinz-Werner Voges, Dorothea Garbe, Christian Paetz, Gerd Collin, Dieter Mayer, Hartmut Höke, Hydrocarbons , Wiley-VCH Verlag GmbH & Co, pot. „Encyklopedia chemii przemysłowej Ullmanna”,15 czerwca 2000


