Perylene
| Perylene | |
 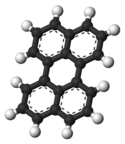 Struktura perylenu |
|
| Identyfikacja | |
|---|---|
| Nazwa IUPAC | Perylene |
| N O CAS | |
| N O ECHA | 100,005,365 |
| N O WE | 205-900-9 |
| PubChem | |
| UŚMIECHY |
c1ccc5cccc4c5c1c2cccc3cccc4c23 , |
| InChI |
InChI: InChI = 1 / C20H12 / c1-5-13- 6-2-11-17-18-12- 4-8-14-7-3-10-16 (20 (14) 18) 15 ( 9-1) 19 (13) 17 / h1-12h |
| Właściwości chemiczne | |
| Brute formula | C 20 H 12 |
| Masa cząsteczkowa | 252,3093 ± 0,0168 g / mol C 95,21%, H 4,79%, |
| Podatność magnetyczna | 171 × 10-6 cm 3 · mol -1 |
| Właściwości fizyczne | |
| T ° fuzja | 273 ° C - 278 ° C |
| * Temperatura wrzenia | 350 ° C - 400 ° C |
| Środki ostrożności | |
| Dyrektywa 67/548 / EWG | |
|
Zwroty S : S22 : Nie wdychać pyłu. S24 / 25 : Unikać kontaktu ze skórą i oczami. Zwroty S : 22, 24/25, |
|
| Klasyfikacja IARC | |
| Grupa 3: Nie podlega klasyfikacji ze względu na jego rakotwórczość dla ludzi | |
| Jednostki SI i STP, chyba że określono inaczej. | |
Perylenu jest związek chemiczny o wzorze C 20 H 12. Jest to wielopierścieniowy węglowodór aromatyczny występujący w postaci brązowej substancji stałej. Nie można go sklasyfikować ze względu na jego rakotwórczość (grupa III IARC) i ogólnie uważa się go za niebezpieczną substancję zanieczyszczającą.
Perylen fluoryzuje na niebiesko, dzięki czemu jest niebieską domieszką dla organicznych diod elektroluminescencyjnych , nawet podstawionych. Jest również organicznym fotoprzewodnikiem . Wykazuje maksimum absorpcji przy 434 nm z molowym współczynnikiem ekstynkcji 38,500 L mol- 1 cm- 1 przy 435,75 nm i jest słabo rozpuszczalny w wodzie (1,2 x 10-5 mmol / l ), podobnie jak wszystkie inne wielopierścieniowe związki aromatyczne.
Wszystkie atomy węgla perylenu są zhybrydyzowane sp 2 , dlatego centralny pierścień nie jest reprezentowany jako piąty pierścień benzenowy (ponieważ wtedy dwa atomy węgla byłyby zhybrydyzowane sp 3, a cząsteczka straciłaby część swojego aromatycznego charakteru i fluorescencji nieruchomości). Strukturę perylenu dogłębnie badano metodą dyfraktometrii rentgenowskiej .
Uwagi i odniesienia
- (w) Hyp Daubensee J., Jr., James D. Wilson and John L. Laity, „ diamagnetic Susceptibility Exaltation in Hydrocarbons ” , Journal of the American Chemical Society , tom. 91 N O 8,9 kwietnia 1968, s. 1991-1998
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- Grupa robocza IARC ds. Oceny ryzyka rakotwórczości dla ludzi, „ Evaluations Globales de la Carcinogenicité pour l'Homme, Groupe 3: Unclassables as to ich rakotwórczość dla ludzi ” , na http://monographs.iarc.fr , IARC,16 stycznia 2009(dostęp 22 sierpnia 2009 )
- SIGMA-ALDRICH
- Donaldson, DM; Robertson, JM; White, JG „Struktura krystaliczna i molekularna perylenu”. Proc. R. Soc. Lond. Do matematyki. Fiz. Sci. 1953 , 220 , 311–321. Pierwsza strona (JSTOR)
