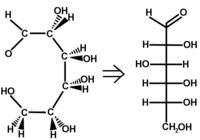
Reprezentacja cząsteczek
Przedstawienie cząsteczek jest stosowane w dziedzinie chemii w celu opisania charakteru i ewentualnie strukturę cząsteczek , a co za tym idzie, innych związków chemicznych . Te wzory i reprezentacje graficzne pozwalają mniej lub bardziej dokładnie wskazać liczbę i rodzaj atomów, z których składa się związek chemiczny, jego wiązania międzyatomowe i kształt w przestrzeni. Konkretne reprezentacje są używane w chemii organicznej i biochemii .
Formuła, reprezentacja i projekcja
Do oznaczania graficznych reprezentacji cząsteczek używa się różnych terminów : mówi się w ten sposób o surowym wzorze , przedstawieniu Crama lub projekcji Fischera .
- Wzory są używane do opisania liczby i rodzaju atomów w cząsteczce (wzór ogólny), aby pokazać, jak są one ze sobą powiązane (wzór Lewisa, strukturalny, półstrukturalny itp .). Wzory są używane głównie do prostego i zwięzłego przedstawiania cząsteczek i dlatego są często używane w równaniach chemicznych .
- Reprezentacja Crama umożliwia bezpośrednie opisanie trójwymiarowej struktury cząsteczki za pomocą diagramu, który umożliwia wizualizację cząsteczki istniejącej w przestrzeni.
- Rzuty cząsteczek nie reprezentują ich bezpośrednio : cząsteczki są rzutowane i spłaszczane na dwóch wymiarach (arkusz) na różne sposoby, w zależności od zastosowanej projekcji. Umożliwiają one pośrednią reprezentację części cząsteczek, które istnieją w przestrzeni, stosując ścisłe zasady rzutowania.
Pojęcie wiązania chemicznego
Celem tego paragrafu nie jest szczegółowe wyjaśnienie, czym jest wiązanie chemiczne, ani lista wszystkich istniejących wiązań chemicznych. Więcej informacji na ten temat w artykule o wiązaniu chemicznym
W tym artykule będziemy rozmawiać głównie o wiązaniach kowalencyjnych i jonowych . W rzeczywistości wiązanie chemiczne jest bardzo rzadko czysto kowalencyjne (tak jest w przypadku wiązania między dwoma identycznymi atomami, jak w cząsteczce wodoru ) lub czysto jonowe. Rzeczywista więź jest mieszaniną tych dwóch postaci.
Wiązanie kowalencyjne
Kiedy dwa atomy są połączone kowalencyjnie, następuje połączenie jednej lub więcej par elektronów, to znaczy, że dwa (lub więcej) elektronów będą należeć do obu atomów w tym samym czasie. Istnieją dwa rodzaje wiązań kowalencyjnych:
- Czysta kowalencja: występuje połączenie dubletu elektronów, każdy atom wprowadza elektron początkowo w stanie celibatu; to łącze reprezentuje pojedyncza linia;
- Celownik kowalencyjny: istnieje połączenie dubletu elektronów, tylko jeden z dwóch atomów dostarczy dublet; Do reprezentacji tego wiązania często używana jest strzałka od dawcy do akceptora elektronów.
Wiązanie jonowe
Wiązania jonowe wynikają z różnic w elektroujemności (zdolności do przyciągania elektronów) atomów obecnych w cząsteczce.
Aby zrozumieć, czym jest wiązanie jonowe, musimy rozważyć dwa połączone ze sobą atomy. Jeśli jeden jest bardziej elektroujemny, będzie przyciągał elektrony z drugiego. Atom bardziej elektroujemny będzie wtedy naładowany trochę ujemnie, a drugi trochę dodatnio. Ta różnica w ładunku stworzy siłę elektrostatyczną, która będzie przyciągać dwa atomy (ładunek dodatni i ładunek ujemny przyciągają się wzajemnie). Jeśli ta różnica w elektroujemności jest bardzo ważna, to mówimy o wiązaniu jonowym. Większość wiązań obejmujących dwa różne pierwiastki jest częściowo jonowa, przy czym charakter jonowy jest na ogół tym ważniejszy, że ważna jest różnica w elektroujemności.
Reprezentacje nie specyficzne dla chemii organicznej
Te reprezentacje mają zastosowanie do wszystkich cząsteczek i wszystkich istniejących jonów . Są dość łatwe w użyciu.
Brute formula
Surowy wzór dostarcza informacji tylko o składzie chemicznym cząsteczek (lub jonów), to znaczy o liczbie i rodzaju atomów, które je tworzą, oraz o ładunku elektrycznym związków, jeśli są one jonami. Nie dostarcza informacji o przestrzennym rozmieszczeniu atomów ani o typie wiązań chemicznych .
Aby napisać prostą formułę, wskazujemy pierwiastek chemiczny za pomocą jego symbolu (por. Układ okresowy pierwiastków ), a ilość tego pierwiastka za pomocą liczby w indeksie po prawej stronie danego pierwiastka. Ładunek elektryczny związku, jeśli taki ma, jest pokazany jako wykładnik na końcu wzoru. Liczba ładunków elementarnych jest wskazywana przez liczbę, po której następuje znak +, jeśli związek jest naładowany dodatnio (jeśli brakuje mu jednego lub więcej elektronów ) lub przez a -, jeśli związek jest naładowany ujemnie (jeśli ma nadmiar elektronów).
PrzykładyNie wszystkie te przykłady zostaną powtórzone w każdej sekcji.
-
Chemia nieorganiczna
- Woda : H 2 O
- Kwas siarkowy : H 2 S O 4
- Jon oksoniowy : H 3 O + (ogólnie ten związek jest naładowany dodatnio, jego ładunek wynosi + e, gdzie e jest ładunkiem elementarnym)
- Tetraaminecopper (ll): Cu ( NH 3) 4 2+( nawiasy oznaczają, że istnieją cztery cząsteczki amoniaku związane z centralnym atomem miedzi)
Formuła Lewisa
Wzór Lewisa został stworzony przez Gilbert Lewis na początku XX XX wieku . Zwykła stanowią połączenia montażowe węgla im ( kowalencyjne i jonowe ), ale także elektronami o wartościowości , które nie uczestniczą w wiązań. Model Lewisa umożliwia odwzorowanie struktury cząsteczki, ale nie daje możliwości pokazania kształtu cząsteczki w przestrzeni.
Reprezentacja Lewisa opiera się na prostych zasadach. W związku z tym, że nie opisano wszystkie cząsteczki, w tym kompleksie z metalami (takimi jak rdzy).
Wzór atomu LewisaOpisana poniżej metoda działa globalnie dla elementów z pierwszych trzech okresów (wiersz tabeli) układu okresowego pierwiastków
Aby ustalić wzór Lewisa atomu, konieczne jest ustalenie jego konfiguracji elektronicznej . Jest na to prosta metoda :
- Określić liczbę elektronów w powłoce wartościowości pierwiastka. W tym celu liczymy miejsce elementu zaczynając od lewej strony tabeli. Zatem wodór ma elektron walencyjny w warstwie, węgiel ma cztery, azot pięć, a chlor wrzesień
- Określ liczbę pojedynczych elektronów i niewiążących dubletów pierwiastka. Musisz tylko wiedzieć, że:
- jeśli element ma co najwyżej cztery elektrony w powłoce walencyjnej, to wszystkie są pojedyncze; tak więc wodór ma jeden elektron, węgiel ma cztery,


- gdy jest więcej niż cztery elektrony walencyjne, wszystkie elektrony dodane do czterech singli tworzą niewiążący dublet ; chlor ma trzy niewiążące dublety i jeden pojedynczy elektron, a azot ma jeden niewiążący dublet i trzy pojedyncze elektrony.

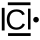
- jeśli element ma co najwyżej cztery elektrony w powłoce walencyjnej, to wszystkie są pojedyncze; tak więc wodór ma jeden elektron, węgiel ma cztery,
Po ustaleniu konfiguracji elektronowej atomu przedstawiamy jego wzór Lewisa. Element jest reprezentowany przez jego symbol. Wokół tego symbolu umieszczone są pojedyncze elektrony, reprezentowane przez punkt i niewiążące dublety, reprezentowane przez linię.
Wzór Lewisa cząsteczkiW przypadku cząsteczek wzór Lewisa opiera się na prostych regułach praktycznych (których przestrzeganie nie zawsze jest możliwe), w tym na zasadzie bajtu lub duetu.
Reguła bajtów oznacza, że każdy atom z drugiego i trzeciego okresu musi zbliżyć się do konfiguracji elektronicznej rzadkich gazów (o dużej stabilności), mając osiem elektronów w swojej powłoce walencyjnej. Zasada duetu dotyczy tylko atomu wodoru, musi on mieć dwa elektrony w powłoce walencyjnej.
Aby ustalić model cząsteczki Lewisa, należy najpierw ustalić wzór Lewisa dla każdego z jej atomów. Następnie łączymy te atomy tak, aby każdy z nich przestrzegał zasady bajtu lub duetu. W tym celu najpierw połączymy pojedyncze elektrony z każdego atomu. Jeśli to nie wystarczy, używamy celowanych wiązań kowalencyjnych lub dzielimy kilka niewiążących dubletów, aby otrzymać dwa pojedyncze elektrony. (Zobacz przykłady)
Przykłady-
 Tutaj pojedyncze elektrony są po prostu połączone, jedna możliwość.
Tutaj pojedyncze elektrony są po prostu połączone, jedna możliwość.
-
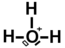 Ten jon jest naładowany dodatnio, więc brakuje mu elektronu, stąd pusty prostokąt na tlenie, który reprezentuje brakujący elektron. Aby utworzyć ten jon, jeden z dwóch niewiążących dubletów tlenu został złamany, w wyniku czego powstały dwa pojedyncze elektrony, jeden tworzy dublet z trzecim wodorem, a drugi jest nieobecny, co odpowiada dodatnim ładunkom. Cząsteczka, której wzór Lewisa zawiera pojedynczy elektron, nazywana jest „rodnikiem”. Ta konfiguracja jest bardzo niestabilna, więc rodniki są bardzo reaktywne.
Ten jon jest naładowany dodatnio, więc brakuje mu elektronu, stąd pusty prostokąt na tlenie, który reprezentuje brakujący elektron. Aby utworzyć ten jon, jeden z dwóch niewiążących dubletów tlenu został złamany, w wyniku czego powstały dwa pojedyncze elektrony, jeden tworzy dublet z trzecim wodorem, a drugi jest nieobecny, co odpowiada dodatnim ładunkom. Cząsteczka, której wzór Lewisa zawiera pojedynczy elektron, nazywana jest „rodnikiem”. Ta konfiguracja jest bardzo niestabilna, więc rodniki są bardzo reaktywne.
Cząsteczka etanolu:
Model kwasu siarkowego:
Płaski wzór strukturalny
Płaski wzór strukturalny umożliwia przedstawiają w sposób bardzo prosty i szybki sposób struktury cząsteczki, jak również wiązań chemicznych. Ale nie pozwala na przedstawienie kształtu cząsteczki w przestrzeni.
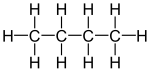
Płaski wzór strukturalny przypomina uproszczoną formułę Lewisa. Rzeczywiście, przedstawienie jest prawie identyczne, ale nie pokazujemy niewiążących dubletów, aby uprościć i rozjaśnić pismo. Zwykle wiązania są pokazane pod kątem 90 °, ale czasami są pokazane pod różnymi kątami, aby przybliżyć rzeczywistą strukturę cząsteczki w przestrzeni (np. 120 ° wokół podwójnego wiązania węgiel-węgiel ).
Przykłady- Cząsteczka butanu:
Reprezentacja Crama
Przedstawienie Cram mogą wykazywać postać w przestrzeni cząsteczki i jej struktury. Z drugiej strony nie reprezentuje wiązań chemicznych (brak różnicy w wiązaniu wielokrotnym i pojedynczym).
Aby zilustrować kształt cząsteczki, różne kierunki, w jakich mogą przyjmować wiązania chemiczne, są skodyfikowane w następujący sposób:
- łącze w płaszczyźnie (arkuszu) jest reprezentowane przez pojedynczą linię
- link skierowany do czytelnika jest reprezentowany przez pełny trójkąt skierowany w stronę płaszczyzny
- łącze, które oddala się od czytelnika, jest reprezentowane przez zakreskowany trójkąt skierowany w stronę płaszczyzny
Orientacja wiązań chemicznych jest przedstawiana dokładniej poprzez zmianę kątów między wiązaniami, aby jak najbardziej przylegały do rzeczywistości. Ta reprezentacja umożliwia w szczególności wizualizację asymetrycznych atomów węgla i określenie, czy cząsteczka jest chiralna .
Przykład
Przedstawienie Cram cząsteczki etanolu .
Reprezentacje specyficzne dla chemii organicznej
Reprezentacje te są specyficzne dla chemii organicznej, ponieważ używają reguł specyficznych dla wiązań węgiel-węgiel lub węgiel-wodór .
Pół rozwinięta formuła (samolot)
Formuła Strukturalna, jak sama nazwa wskazuje, jest skondensowaną formą Formuły Strukturalnej. Nie reprezentujemy już wiązań węgiel-wodór, które są skondensowane w postaci: CH n(gdzie n liczba atomów wodoru związanych z atomem węgla). Przedstawiamy wiązania węgiel-węgiel i rozróżniamy wiązania pojedyncze i wielokrotne.
Przykłady- CH 3- CH 2 OH, cząsteczka etanolu, z rodziny alkoholi.
- CH 3 -CO-CH 3, cząsteczka acetonu z rodziny ketonów.
Wzór szkieletowy to szybki i łatwy sposób na przedstawienie struktury cząsteczki organicznej .
Nie reprezentujemy już atomów węgla ani przenoszonych przez nie atomów wodoru. Przedstawiono atomy wodoru przenoszone przez heteroatomy (pierwiastki inne niż węgiel i wodór). Wiązania węgiel-węgiel są przedstawione ukośną linią. We wzorze szkieletowym atomy węgla znajdują się więc na przecięciu dwóch segmentów. Rozróżniamy wiązania wielokrotne i pojedyncze: pojedyncze wiązanie będzie reprezentowane przez linię, podwójne wiązanie przez dwa równoległe segmenty.
Przedstawiamy wiązanie między heteroatomami lub grupami funkcyjnymi i atomami węgla, z którymi są połączone segmentem; grupa funkcyjna lub heteroatom jest umieszczona na końcu tego segmentu. Atomy wodoru przenoszone przez atomy węgla nie są pokazane, segment którego jeden koniec nie jest połączony z żadną grupą funkcyjną odpowiada w rzeczywistości -CH 3.
Przykłady-
 szkieletowy wzór cząsteczki etanolu
szkieletowy wzór cząsteczki etanolu
-
 szkieletowy wzór cząsteczki memantyny
szkieletowy wzór cząsteczki memantyny
-
 wzór szkieletowy niektórych ważnych polimerów
wzór szkieletowy niektórych ważnych polimerów
Projekcja Newmana
Newman występ jest bardzo użyteczny do badania różnych konformacji (kierunek z konformerem do kolejnego poprzez obrót wokół pojedynczego wiązania węgiel-węgiel) o związku organicznego . Ten występ jest zwykle używany tylko z czterowartościowymi atomami węgla (związanymi z czterema innymi atomami).
Aby przedstawić cząsteczkę w projekcji Newmana, musimy spojrzeć na cząsteczkę w osi pojedynczego wiązania węgiel-węgiel, nie przedstawiamy tych dwóch atomów węgla w projekcji Newmana, ale wiązania.
Wiązania węglowe na pierwszym planie są reprezentowane przez trzy segmenty zaczynające się od tego samego punktu, kąty między każdym z tych segmentów wynoszą 120 °, jak w rzeczywistości. Węgiel w tle jest reprezentowany przez okrąg, na którym umieszczamy trzy pozostałe wiązania. (zobacz przykład)
Ta reprezentacja umożliwia łatwą wizualizację efektów oddziaływań sterycznych między grupami przenoszonymi przez dwa sąsiednie węgle. Umożliwia również łatwe określenie konformacji Z lub E alkenu powstałej w wyniku reakcji eliminacji .
PrzykładProjekcja Fischera
Projekcja Fischera jest stosowany głównie stanowią cukry i aminokwasy. Został wymyślony przez Hermanna Emila Fischera .
Nie przedstawiamy atomów węgla, znajdują się one na przecięciu segmentów poziomych i linii pionowej. Łańcuch węglowy jest reprezentowany przez linię pionową, tak że wiązania pokazane pionowo odsuwają się od czytnika. Linki pokazane poziomo wychodzą z płaszczyzny arkusza w kierunku czytelnika (patrz przykład). Najbardziej utleniony węgiel znajduje się na początku łańcucha (u góry C = O).
Ta reprezentacja umożliwia łatwe rozróżnienie chiralnych enancjomerów L lub D.
PrzykładProjekcja Hawortha
Projekcja hawortha umożliwia stanowią strukturę cykliczną OSE (lub monosacharydów) o prostej widzenia trójwymiarowej.
W tej projekcji nie są przedstawione ani atomy węgla, ani wodoru, ale z drugiej strony wiązania węgiel-węgiel są reprezentowane przez linię. Ponadto linki najbliżej czytelnika są pogrubione.
Przykład
Projekcja Hawortha α- D- glukopiranozy