Tlenek tantalu (V)
| Tlenek tantalu (V) | |
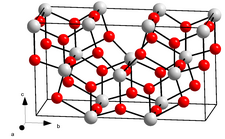 __ Ta 5+ __ O 2− Sieć krystaliczna tlenku tantalu (V) |
|
| Identyfikacja | |
|---|---|
| N O CAS | |
| N O ECHA | 100.013.854 |
| N O WE | 215-238-2 |
| N O RTECS | WW5855000 |
| PubChem | 518712 |
| UŚMIECHY |
O = [Ta] (= O) O [Ta] (= O) = O , |
| InChI |
Std. InChI: InChI = 1S / 5O.2Ta Std. InChIKey: PBCFLUZVCVVTBY-UHFFFAOYSA-N |
| Wygląd | bezwonny biały proszek |
| Właściwości chemiczne | |
| Brute formula | Ta 2 O 5 |
| Masa cząsteczkowa | 441,8928 ± 0,0015 g / mol O 18,1%, Ta 81,9%, |
| Właściwości fizyczne | |
| T ° fuzja | 1872 ° C |
| Rozpuszczalność | < 10 mg · L -1 do 20 ° C |
| Masa objętościowa | 8,2 g · cm -3 |
| Związki pokrewne | |
| Inne związki | |
| Jednostki SI i STP, chyba że określono inaczej. | |
Tantalu (V), tlenek lub pięciotlenek tantalu , jest związek chemiczny o wzorze Ta 2 O 5. Występuje jako bezwonne, białe ciało stałe, które jest nierozpuszczalne we wszystkich rozpuszczalnikach, ale które może zostać zaatakowane przez mocne zasady i kwas fluorowodorowy HF (aq). Jest to materiał obojętny o wysokim współczynniku załamania światła i niskim współczynniku pochłaniania, co czyni go materiałem stosowanym na powłoki. Jest również szeroko stosowany do produkcji kondensatorów ze względu na wysoką przenikalność .
Źródła i rafinacja
Tantal znajduje się w tantalicie i kolumbicie - kolumbij to przestarzała nazwa niobu - obecny w pegmatytach , skałach magmowych . Mieszaniny tantalitu i kolumbitu nazywane są koltanem . Microlite i pirochlor odpowiednio zawierają około 70 do 10% tantalu.
Do minerałów z tantalu zazwyczaj zawierają znaczące ilości niobu, który sam jest cennym metalu, więc oba te metale są wydzielane do celów handlowych. Cały proces jest hydrometalurgiczny i rozpoczyna się od etapu ługowania, w którym metal poddaje się obróbce kwasem fluorowodorowym i siarkowym w celu wytworzenia rozpuszczalnych w wodzie fluorowodorów, aby umożliwić oddzielenie metalu. Te metale od różnych niemetalicznych zanieczyszczeń zawartych w skałach:
(FeMn) (NbTa) 2 O 6+ 16 HF → H 2 [TaF 7 ]+ H 2 [NbOF 5 ]+ FeF 2+ MnF 2+ 6 H 2 O.Fluorowodory tantalu i niobu usuwa się z roztworu wodnego metodą ekstrakcji ciecz-ciecz za pomocą rozpuszczalników organicznych, takich jak cykloheksanon lub keton metylowo-izobutylowy . Ten etap umożliwia łatwe usunięcie różnych zanieczyszczeń metalicznych, takich jak żelazo i mangan, które pozostają w fazie wodnej w postaci fluorków . Następnie przeprowadza się oddzielenie tantalu i niobu przez dostosowanie pH . Niob wymaga większej kwasowości, aby pozostać w roztworze i dlatego może być selektywnie usuwany przez ekstrakcję w mniej kwaśnej wodzie. Czysty roztwór fluorowodoru tantalu jest następnie neutralizowany amoniakiem, aby uzyskać wodorotlenek tantalu (V) Ta (OH) 5który można ostatecznie kalcynować do tlenku tantalu (V) Ta 2 O 5 :
H 2 [TaF 7 ]+ 5 H 2 O+ 7 NH 3→ Ta (OH) 5+ 7 NH 4 F., 2 Ta (OH) 5→ Ta 2 O 5+ 5 H 2 O.Tlenek tantalu (V) jest powszechnie stosowany w elektronice w postaci cienkich warstw . Dla tych zastosowań, może on być wytwarzany przez epitaksję z fazy gazowej metaloorganicznych (MOCVD), lub powiązanych procesów, co wiąże się hydrolizie z lotnych halogenków lub alkoholami , takimi jak etanolan tantalu (V) Ta 2 (OEt) 10 :
Ta 2 (OEt) 10+ 5 H 2 O→ Ta 2 O 5+ 10 EtOH 2 TaCl 5+ 5 H 2 O→ Ta 2 O 5+ 10 HCl .Struktura i właściwości
Struktury krystalicznej tlenku tantalu (V) jest nieco omawiane. Ciało stałe jest brudne, bezpostaciowe lub polikrystaliczne . Pojedyncze kryształy są trudne w uprawie. Badanie metodą krystalografii rentgenowskiej ograniczało się do dyfrakcji proszkowej, która dostarcza mniej informacji strukturalnych. Zidentyfikowano co najmniej dwa polimorfy : postać niskotemperaturowa, znana jako L - lub β-Ta 2 O 5i postać wysokotemperaturowa zwana H - lub α-Ta 2 O 5. Przejście między tymi dwiema formami, co odbywa się od 1000 do 1360 ° C , jest powolna i odwracalne, obie formy współistniejącą między tymi dwiema temperaturami. Te dwa polimorfy składają się z łańcuchów zbudowanych z ośmiościanów TaO 6i pięciokątne bipiramidy TaO 7wspólne krawędzie i ich przeciwległe wierzchołki. Układzie krystalicznym jest rombowy The grupa przestrzenna z p-Ta 2 O 5będący Pna 2 w obu przypadkach na podstawie rentgenowskiej analizy dyfraktometrycznej pojedynczego kryształu. Opublikowano również postać wysokociśnieniową, w której atomy tantalu przyjmują geometrię koordynacji 7, aby uzyskać strukturę jednoskośną (grupa przestrzenna C2).
Uzyskanie materiału o jednorodnej strukturze jest trudne, co doprowadziło do publikacji różnych właściwości tlenku tantalu (V). Twoje 2 O 2jest izolatorem elektrycznym o niedozwolonej szerokości pasma , którego publikowana wartość waha się między 3,8 a 5,3 eV w zależności od trybu produkcji. Ogólnie rzecz biorąc, im bardziej amorficzny materiał, tym szerszy jest jego zakazany pas. Należy zauważyć, że wartości eksperymentalne są znacznie wyższe niż wartości obliczone z modeli komputerowych ( 2,3 do 3,8 eV ).
Dielektryczna tlenku tantalu (V) jest rzędu 25 ° C, jednak wartości powyżej 50 również zostały opublikowane. Ten materiał jest ogólnie uważany za dielektryk o wysokim współczynniku κ .
Reakcje
Tlenek tantalu (V) nie reaguje znacząco z kwasem solnym HCl ani z kwasem bromowodorowym HBr, ale rozpuszcza się w kwasie fluorowodorowym HF i reaguje z wodorofluorkiem potasu KHF 2 i kwas fluorowodorowy HF, jak następuje:
Ta 2 O 5+ 4 KHF 2+ 6 HF → 2 K 4 [TaF 7 ]+ 5 H 2 O.Ta 2 O 5można zredukować do metalicznego tantalu za pomocą metalicznych środków redukujących, takich jak wapń i glin :
Ta 2 O 5+ 5 Ca → 2 Ta + 5 CaO .Aplikacje
W elektronice
Ze względu na dużą szczelinę i wysoką przenikalność , tlenek tantalu (V) jest używany w wielu różnych zastosowaniach elektronicznych, zwłaszcza w kondensatorach tantalowych ( cale ) . Są one stosowane w budownictwie samochodowym , telefonach komórkowych , pagerach , obwodach elektronicznych , cienkich warstwach elementów elektronicznych i elektronice mikrofalowej. W 1990, zainteresowanie tlenku tantalu (V) wzrósł w zakresie zastosowań, takich jak dielektrycznej wysokiej kappa do kondensatorów z pamięci DRAM . Stosowany jest w kondensatorach on-chip metal - izolator - metalowych w mikrofalowych układach scalonych CMOS .
W optyce
Ze względu na wysoki współczynnik załamania światła tlenek tantalu (V) został użyty do produkcji szkła do obiektywów fotograficznych .
Uwagi i odniesienia
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- Entry „Tantal (V) tlenek” w chemicznej bazy GESTIS z IFA (ciała niemieckiej odpowiedzialnej za bezpieczeństwo i higienę pracy) ( niemiecki , angielski ), dostęp 16 października 2013 (Javascript required)
- (in) Strona ditantale pentoxide w witrynie webElements.com.
- (w) Frederick Fairbrother, „The Chemistry of Niobium and Tantalum” Elsevier Publishing Company (1967), str. 1-28, Nowy Jork. ( ISBN 978-0-444-40205-9 ) .
- (en) Charlotta Askeljung, Bengt-Olov Marinder i Margareta Sundberg , „ Wpływ obróbki cieplnej na strukturę L-Ta 2 O 5 :: badanie metodami XRPD i HRTEM ” , Journal of Solid State Chemistry , t. 176 n o 1,15 listopada 2003, s. 250-258 ( czytaj online ) DOI : 10.1016 / j.jssc.2003.07.003
- (en) NC RS Stephenson and Roth , „ Systematyka strukturalna w układzie binarnym Ta 2 O 5 -WO 3 . V. Struktura niskotemperaturowej formy tlenku tantalu L -Ta 2 O 5 » , Acta Crystallographica Section B - Structural Crystallography and Crystal Chemistry , vol. 27 N O 5,Maj 1971, s. 1037-1044 ( czytaj online ) DOI : 10.1107 / S056774087100342X
- (en) GM Wolten AB i Chase , „Dane pojedynczego kryształu dla β Ta 2 O 5 i A KPO 3 » , Zeitschrift für Kristallographie - Crystalline Materials , vol. 129 n kości 5-6,lipiec 2010, s. 365-368 ( czytaj online ) DOI : 10.1524 / zkri.1969.129.5-6.365
- (w) IP Zibrov, wiceprezes Filonenko, pan Sundberg i P.-E. Werner , „ Struktury i przejścia fazowe B -Ta 2 O 5 i Z -Ta 2 O 5 : dwie wysokociśnieniowe formy Ta 2 O 5 » , Acta Crystallographica Section B - Structural Science , vol. 56, n o 4,sierpień 2000, s. 659-665 ( czytaj online ) DOI : 10.1107 / S0108768100005462
- (w) Kaupo Kukli Jaan Aarik Aleks Aidla Oksana Kohan, Teet Uustare i Väino Sammelselg , „ Properties of tantalium thin film created by atomic layer deposition ” , Thin Solid Films , Vol. 260 n O 2 15 maja 1995, s. 135-142 ( czytaj online ) DOI : 10.1016 / 0040-6090 (94) 06388-5
- (en) RM Fleming, DV Lang, CDW Jones, L. Steigerwald, DW Murphy, GB Alers, Y.-H. Wong, RB van Dover, JR Kwo i AM Sergent , „ Transport ładunku zdominowany przez defekt w amorficznym Ta 2 O 5 cienkie filmy ” , Journal of Applied Physics , vol. 88 N O 2,2000, s. 850 ( czytaj online ) DOI : 10.1063 / 1.373747
- (en) Prakash A. Murawala, Mikio Sawai, Toshiaki Tatsuta, Osamu Tsuji, Shizuo Fujita1 i Shigeo Fujita , „ Structural and Electrical Properties of Ta 2 O 5 Wyhodowany przez CVD wzbogacony plazmą ciekłą przy użyciu źródła Penta Ethoxy Tantalum ” , Japanese Journal of Applied Physics , vol. 32, n o 1,1993, s. 368-375 ( czytaj online ) DOI : 10.1143 / JJAP.32.368
- (w) R. Ramprasad , „ Pierwsze zasady badania defektów niedoboru tlenu w pięciotlenku tantalu ” , Journal of Applied Physics , tom. 94 N O 9, 2003, s. 5609 ( czytaj online ) DOI : 10.1063 / 1.1615700
- (en) H. Sawada i K. Kawakami , „ Elektroniczna struktura niedoboru tlenu w Ta 2 O 5 ” , Journal of Applied Physics , vol. 86 N O 21999, s. 956 ( czytaj online ) DOI : 10.1063 / 1.370831
- (w) Ramy Nashed, MI Walid Hassan, Yehea Ismailc i Nageh K. Allam , „ Odkrywanie wzajemnego oddziaływania struktury krystalicznej i elektronicznej struktury pasmowej tlenku tantalu (Ta 2 O 5 ) ” , Physical Chemistry Chemical Physics , vol. 15 N O 5,2013, s. 1352-1357 ( czytaj online ) DOI : 10.1039 / C2CP43492J
- (w) V. Macagno i JW Schultze , „ Wzrost i właściwości cienkich warstw tlenkowych to elektrody tantalowe ” , Journal of Electroanalytical Chemistry and Interfacial Electrochemistry , vol. 180, n kość 1-2, 10 grudnia 1984, s. 157-170 ( czytaj online ) DOI : 10.1016 / 0368-1874 (84) 83577-7
- (w) Mr. Hiratani, S. Kimura, T. Hamada, S. Iijima i N. Nakanishi , „ Hexagonal polymorph of tantal pentoxide with Enhanced dielectric-constant ” , Applied Physics Letters , vol. 81 N O 13, 2002, s. 2433 ( czytaj online ) DOI : 10.1063 / 1.1509861
- (w) Anatoly Agulyansky , „ Fluorotantalan potasu w stanie stałym, rozpuszczonym i stopionym ” , Journal of Fluorine Chemistry , tom. 123 n O 2 Październik 2003, s. 155-161 ( czytaj online ) DOI : 10.1016 / S0022-1139 (03) 00190-8
- (w) S. Ezhilvalavan i TY Tseng , „ Preparat and Properties of tantal pentoxide (Ta 2 O 5 ) cienkie folie do zastosowań w ultra dużych układach scalonych (ULSI) - przegląd ” , Journal of Materials Science: Materials in Electronics , vol. 10, n o 1,1999, s. 9-31
- (en) Solomon Musikant, „Optical Glas Composition”. Materiały optyczne: wprowadzenie do wyboru i zastosowania (1985), str. 28, CRC Press. ( ISBN 978-0-8247-7309-0 )