Kwas selenowy
| Kwas selenowy | |||
| |||
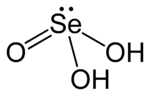
| Struktura kwasu selenowego | |||
| Identyfikacja | |||
|---|---|---|---|
| Nazwa IUPAC | kwas selenowy | ||
| N O CAS | |||
| N O ECHA | 100,029,067 | ||
| N O WE | 231-974-7 | ||
| N O RTECS | VS7175000 | ||
| PubChem | 1091 | ||
| ChEBI | 26642 | ||
| UŚMIECHY |
O [Se] (O) = O , |
||
| InChI |
Std. InChI: InChI = 1S / H2O3Se / c1-4 (2) 3 / h (H2,1,2,3) Stand. InChIKey: MCAHWIHFGHIESP-UHFFFAOYSA-N |
||
| Wygląd | higroskopijne białe ciało stałe | ||
| Właściwości chemiczne | |||
| Brute formula | H 2 SeO 3 | ||
| Masa cząsteczkowa | 128,97 ± 0,03 g / mol H 1,56%, O 37,22%, Se 61,22%, |
||
| Właściwości fizyczne | |||
| T ° fuzji | 70 ° C ( rozkład ) | ||
| Rozpuszczalność | 1670 g · L -1 | ||
| Masa objętościowa | 3,004 g · cm od -3 do 15 ° C | ||
| Środki ostrożności | |||
| SGH | |||
   Niebezpieczeństwo H301, H331, H373, H410, P261, P273, P311, P301 + P310, P501, H301 : Działa toksycznie po połknięciu H331 : Działa toksycznie w następstwie wdychania H373 : Może powodować uszkodzenie narządów (wymienić wszystkie dotknięte narządy, jeśli są znane) poprzez powtarzane lub długotrwałe narażenie (wskazać drogę narażenia, jeżeli definitywnie udowodniono, że inne drogi narażenia nie powodują zagrożenie) H410 : Działa bardzo toksycznie na organizmy wodne, powodując długotrwałe skutki P261 : Unikać wdychania pyłu / dymu / gazów / mgieł / par / aerozoli. P273 : Unikać uwolnienia do środowiska. P311 : Skontaktować się z OŚRODKIEM ZATRUĆ lub lekarzem. P301 + P310 : W przypadku połknięcia: natychmiast skontaktować się z OŚRODKIEM ZATRUĆ lub lekarzem. P501 : Zawartość / pojemnik usuwać do ... |
|||
| Transport | |||
60 : materiał toksyczny lub wykazujący niewielki stopień toksyczności Numer UN : 3283 : ZWIĄZEK SELENU, NSA Klasa: 6.1 Etykieta: 6.1 : Substancje toksyczne Opakowanie: Grupa pakowania II : substancje umiarkowanie niebezpieczne;  |
|||
| Jednostki SI i STP, chyba że określono inaczej. | |||
Kwas selenawy jest związek chemiczny o wzorze H 2 SeO 3. Jest to główne kwasy tlenowe z selenu , inne stanowią kwas selenowy H 2 SeO 4. Jest to analogowy z kwasu siarkowego H 2 SO 3, ale łatwiej jest to wyodrębnić. Uzyskuje się go łatwo poprzez dodanie dwutlenku selenu SeO 2i woda H 2 O. W skrystalizowanym stanie stałym jego cząsteczki są piramidalne, połączone wiązaniami wodorowymi . W roztworze wodnym jest dikwasem diprotycznym.
H 2 SeO 3 H + + HSeO 3- (p K a = 2,62) HSeO 3- H + + SeO 32– (p K a = 8,32)Jest słabo utleniający, o dość powolnej kinetyce . Przy 1 mol · L -1 H + :
H 2 SeO 3+ 4 H + + 4 e - Se + 3 H 2 O ( E o = + 0,74 V ).Przy 1 mol · L -1 jonów OH - :
SeO 32– + 4 e - + 3 H 2 O Se + 6 OH - ( E o = -0,37 V ).Jest stosowany w syntezie organicznej do produkcji 1,2-dialdehydów , takich jak glioksal O = CH - CH = O.
Głównym zastosowaniem jest kwas selenawy w niebieszczenia powierzchniach metalu, w szczególności stali z broni . Dlatego używamy kwasu selenowego H 2 SeO 3z azotanem miedzi (II) Cu (NO 3 ) 2i kwas azotowy HNO 3do zmiany koloru stali ze srebrnoszarego na szaro-niebieski lub czarny. Zamiast tego inne procesy obejmują siarczan miedzi CuSO 4i kwas fosforowy H 3 PO 4. We wszystkich przypadkach tworzy się warstwa pasywacji w selenku miedzi (I) Cu 2-δ If, co odróżnia te procesy od innych niebieszczeń, w wyniku których powstaje tlenek żelaza (II, III) FeO · Fe 2 O 3.
Jest również używany w niektórych testach używania narkotyków.
Uwagi i odniesienia
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- Wpis "Kwas selenowy" w chemicznej bazie danych GESTIS IFA (niemieckiego organu odpowiedzialnego za bezpieczeństwo i higienę pracy) ( niemiecki , angielski ), dostęp 22 maja 2017 (wymagany JavaScript)
- (w) Anthony R. Ronzio i TD Waugh , „ Glyoxal bisulfite ” , Organic Syntheses , vol. 24, 1944, s. 61 ( DOI 10.15227 / orgsyn.024.0061 , czytaj online )
- (w) „ Test koloru Odczynniki / Zestawy do wstępnej identyfikacji substancji odurzających ” , egzekwowania prawa i Korekty Standardów i testowanie programu na amerykańskiego Departamentu Sprawiedliwości, Biuro Programów Sprawiedliwości, Narodowego Instytutu Sprawiedliwości , lipiec 2000(dostęp 22.05.2017 ) .
