Acetylocholinoesteraza
| Acetylocholinoesteraza | |||||||||||||||||||
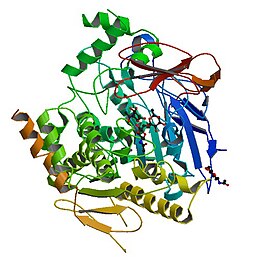 Struktura ludzkiej acetylocholinoesterazy ( PDB 1B41 ) | |||||||||||||||||||
| Główne cechy | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Symbol | BÓL | ||||||||||||||||||
| Nr WE | 3.1.1.7 | ||||||||||||||||||
| Homo sapiens | |||||||||||||||||||
| Umiejscowienie | 7 q 22,1 | ||||||||||||||||||
| Waga molekularna | 67 796 Da | ||||||||||||||||||
| Liczba pozostałości | 614 aminokwasów | ||||||||||||||||||
| Linki dostępne z GeneCard i HUGO . | |||||||||||||||||||
| |||||||||||||||||||
W enzymologii An acetylocholinoesterazy jest hydrolaza który katalizuje się reakcję :
CH 3 COOCH 2 CH 2 N + (CH 3 ) 3+ H 2 O→ CH 3 COO -+ HOCH 2 CH 2 N + (CH 3 ) 3.Te enzymy zapewnienia rozszczepienia z acetylocholiny , a neuroprzekaźnik w jonów octanu i choliny w synapsach , reakcja niezbędnym dla neuronów cholinergicznych powrotu do stanu spoczynkowego po aktywacji przez impulsów nerwowych , na przykład w silniku płyty .
Istnieje również białko z 535 reszt z aminokwasami , N -glycosylée o aktywności enzymatycznej acetylocholinoesterazy (AChE), związany przez glikozylofosfatydyloinozytolu (GPI) na powierzchni czerwonych krwinek . Polimorfizm (Yta → Ytb: His353Asn) tego erytrocytów AChE jest źródłem antygenów układu grupowego krwi Cartwright , systemu YT (011), antygenów Yta (001) bardzo powszechnych i Ytb (002) rzadkich. Gen ACHE , OMIM (en) 112100 , zlokalizowany w 7q22.1, częstości alleli w Europie: Yt a 0,9559, Yt b 0,0441. Genetycznie powiązany z genem Kell, lod-score 3,48 dla Θ = 0,28, tj. Odległość 28 centymorgów . Składanie na czwartym eksonie oznacza, że na poziomie C-końcowym białko to może być zakotwiczone przez GPI na powierzchni erytrocytów, ale nie w tkance nerwowej.
Acetylocholinoesteraza Tetramer acetylocholinesterazy myszy ( Mus musculus , PDB 1MAA )
Tetramer acetylocholinesterazy myszy ( Mus musculus , PDB 1MAA )
| Nr WE | WE |
|---|---|
| numer CAS |
| IUBMB | Wpis IUBMB |
|---|---|
| IntEnz | Widok IntEnz |
| BRENDA | Wejście BRENDA |
| KEGG | Wejście KEGG |
| MetaCyc | Szlak metaboliczny |
| PRIAM | Profil |
| PDB | Struktury |
| UDAĆ SIĘ | AmiGO / EGO |
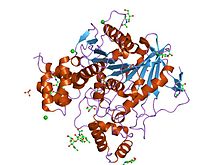 Butyrylocholinoesteraza ludzka etylofosforylowana ( PDB 1XLV )
Butyrylocholinoesteraza ludzka etylofosforylowana ( PDB 1XLV )
| Pfam | PF00135 |
|---|---|
| InterPro | IPR002018 |
| WŁASNOŚĆ | PDOC00112 |
| SCOP | 1acj |
| SUPER RODZINA | 1acj |
| Rodzina OPM | 135 |
| Białko OPM | 1p0i |
| CDD | cd00312 |
Uwagi i odniesienia
- (w) G. Kryger, Mr. Harel, K. Giles, L. Toker, B. Velan, A. Lazar, C. Kronman, D. Barak, Ariel N., A. Shafferman, I. Silman and Sussman JL , „ Struktury rekombinowanej natywnej i zmutowanej ludzkiej acetylocholinoesterazy E202Q skompleksowanej z toksyną jadu węża fasciculin-II ” , Acta Crystallographica. Sekcja D, Krystalografia biologiczna , t. 56 N O Pt 11 listopad 2000, s. 1385-1394 ( PMID 11053835 , DOI 10.1107 / S0907444900010659 , czytaj online )
- wartości dotyczące masy oraz liczby reszt wskazanych tutaj są związki o prekursora białka otrzymanego z translacji z genu przed potranslacyjnych modyfikacji , i mogą się znacznie różnić od odpowiednich wartości dla osób funkcjonalne białko .
- Geoff Daniels ludzkiej krwi grupy , 2 e wydanie, Blackwell Publishing.
- (w) Yves Bourne, Palmer Taylor, Peter E. i Pascale Bougis Marchot , „ Crystal Structure of Mouse Acetylcholinesterase - A Peripheral site-occlusion Loop in a tetrameric Assembly ” , Journal of Biological Chemistry , tom. 274 n O 5, 29 stycznia 1999, s. 2963-2970 ( PMID 9915834 , DOI 10.1074 / jbc.274.5.2963 , czytaj online )
- (w) Florian Nachon, Oluwatoyin A. Asojo Gloria EO Borgstahl Patrick Masson i Oksana Lockridge , „ Rola wody w starzeniu się ludzkiej butyrylocholinoesterazy Inhibitowana przez echothiophate: Struktura kryształu sugeruje dwa alternatywne mechanizmy starzenia ” , Biochemistry , vol. 44, n o 4, Luty 2005, s. 1154-1162 ( PMID 15667209 , DOI 10.1021 / bi048238d , czytaj online )