Organomagnez
Magnezoorganicznym jest związek organiczny z węgla - magnezu wiązania . Jest to ważna rodzina związków metaloorganicznych w syntezie organicznej, ponieważ obejmuje odczynniki Grignarda , które są mieszanymi związkami magnezoorganicznymi w postaci R - Mg X , gdzie R to łańcuch węglowy, a X to halogen , zwykle brom. Lub chlor , czasem jod - atom fluoru nie jest powszechnie stosowany z uwagi na zbyt małą polaryzowalności z difluoro F 2. Odczynniki te są szeroko stosowane w przemyśle, a ich odkrycie pod koniec XIX -go wieku przez francuskiego chemika Victora Grignarda włączył go dostać Nagrodę Nobla w dziedzinie chemii w 1912 roku, ponieważ mogą one wiązać różnorodne klocki aby z cząsteczek organicznych.
Oprócz odczynników Grignarda, związki magnezoorganiczne obejmują cząsteczki, takie jak dimetylomagnez (CH 3 ) 2 Mg, dibutylomagnez (CH 3 CH 2 CH 2 CH 2 ) 2 Mglub antracen-magnez .
Charakter metaloorganiczny R - Mg - X
Carbon ma elektroujemność silny: . I my też to zauważamy . Dlatego ten fizyczny fakt nakłada polaryzacji C - MS: C -M związku . Zauważamy odwrócenie polaryzacji klasycznych wiązań węglowych: w metaloorganicznym węgiel niesie ładunek (węgiel ten nazywany jest karboanionem), ponadto wiązanie to jest w 35% jonowe, co pozwoli na reakcję np. Z halogenkiem alkilowym ( R -X ) tworząc wiązanie węgiel-węgiel .
Organomagnez to jedna z najsilniejszych zasad Brönsteda w chemii organicznej o pKa rzędu 40 do 60. R-Mg-X jest silnym nukleofilem .
Synteza organomagnezu
Ze względu na ich skrajną zasadowość organomagnez nie występuje naturalnie. Ogólne wyniki syntezy są następujące:
Tryb pracy
Syntezy z magnezoorganicznego delikatna: the Środowisko reakcji może być bezwodne, ze względu na właściwości żądanego produktu; reakcja jest silnie egzotermiczna, a rozpuszczalnik jest lotny i łatwopalny. Niewłaściwa obsługa skutkuje również powstaniem pasożytniczego produktu - zwanego „ Wurtz Coupling ”.
Wymagane materiały :
- Piłka trójkolorowa;
- Lejek do odlewania izobarycznego;
- Chłodnica zwrotna;
- Utrzymuje CaCl 2 (lub pracuje w obojętnej atmosferze);
- Mieszadło magnetyczne z grzaniem;
- Wióry magnezowe;
- Eter dietylowy lub bezwodny THF;
- Pochodna halogenowana;
- Kąpiel wodna, a następnie zimna woda.
Tryb pracy
- Wykonać zestaw do dodawania z refluksem, chroniąc środowisko reakcyjne przed wilgocią atmosferyczną i umieszczając owalny pręt magnetyczny w trójszyjnej kolbie.
- W tricolu umieść wióry magnezu, które zostały wcześniej aktywowane w piekarniku. Przykryj je kilkoma cm 3 bezwodnego eteru etylowego. Dodaj mały kryształ diody.
- Lejkę zalać roztworem chlorowcowanej pochodnej w bezwodnym eterze etylowym i zamknąć szklanym korkiem.
- Wlej kilka kropli roztworu halogenku na wióry magnezu, odczekaj kilka minut do zaobserwowania odbarwienia występującego w medium reakcyjnym.
- Gdy zabarwienie jodu zniknie w medium reakcyjnym, podgrzać w łaźni wodnej w celu wywołania refluksu i wlać halogenek powoli i kropla po kropli, mieszając magnetycznie.
- Po zakończeniu dodawania ogrzać środowisko reakcyjne do wrzenia, aby uzyskać pełną reakcję.
Komentarze
Aby zapobiec występowaniu sprzężenia Würtza między zsyntetyzowanym organomagnezem i halogenkiem. Od początku reakcji eter wrze: refluks służy do skraplania oparów eteru przepływających do kolby; refluks należy również utrzymywać na bardzo niskim poziomie, aby nie wywoływać wspomnianej powyżej reakcji pasożytniczej. Nie ma potrzeby ogrzewania podczas całej manipulacji, ponieważ reakcja jest bardzo egzotermiczna .
Ostatecznie otrzymany roztwór ma ogólnie dość jasnoszarą barwę.
Rozpuszczalnik
Eter odgrywa tutaj podwójną rolę, solwatuje utworzony organomagnez i stabilizuje go, organomagnez jest tu kwasem Lewisa, rozpuszczalnik pełni tutaj rolę zasady Lewisa , dlatego niewiążące dublety tlenu stabilizują reaktywne centrum magnez . Można np. Zastosować eter dietylowy lub też THF - tetrahydrofuran , por. Niżej wymienione.

Środowisko, w którym kąpie się organomagnez, musi być całkowicie bezwodne: reakcja woda / RMgX jest ożywiona.
Reaktywność organomagnezu
Reakcje na zwykłych związkach organicznych
Na wodzieReakcja związków magnezoorganicznych z wodą jest bardzo żywa (jest to reakcja kwasowo-zasadowa : p K a (RH / R-) = 50) i egzotermiczna. Dlatego tryb pracy wymaga całkowitego odwodnienia powietrza w naczyniach szklanych, a także powierzchni i rozpuszczalników. Z wyjątkiem szczególnych przypadków, ta reakcja jest uważana za pasożytniczą i prowadzi do zniszczenia organomagnezu.
Reakcja organomagnezu na wodę jest następująca:
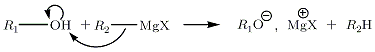 Zawiera kwasy karboksylowe
Zawiera kwasy karboksylowe
 Z aminami
Z aminami
 Z terminalnymi alkinami
Z terminalnymi alkinami

Reakcje substytucji nukleofilowej
Podstawienie nukleofilowe, przykład I 2Proponujemy nukleofilową substytucję RMgX na I 2 (indukowana jest polarność tej cząsteczki).
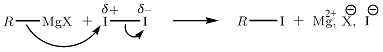 Podstawienie nukleofilowe pochodnymi chlorowcowanymi
Podstawienie nukleofilowe pochodnymi chlorowcowanymi
Pochodna halogenowana: mechanizm R'-X: SN2
R-MgX + R'-X -> RR '+ MgX2
Uwaga: działa dobrze z RI i Ar-CH2X, ponieważ są stabilizowane przez efekt indukcyjny dla RI i mezomer dla Ar-CH2X
Reakcja na epoksydyMechanizm: SN2
W eterze:
R ---- Mg ---- X + O (CH2) 2 (cykl) → R-CH2-CH2-O-Mg-X
Następnie hydroliza kwasowa H3O +:
R-CH2-CH2-O-Mg-X + H + → R-CH2-CH2-OH + MgX +
Reakcje addycji nukleofilowej ...
... na aldehydach i ketonach- Na aldehydy :

Reakcja pomiędzy organomagnezu i aldehydów prowadzi do wytworzenia alkoholu o średnim, jeśli R 1 i R 2 łańcuchy zawierają co najmniej jeden atom węgla. Jeśli węgiel wspierający końcowej grupy alkoholowej jest asymetryczny, tj. Jeśli dwa łańcuchy R są różne, produkt będzie składał się z dwóch izomerów o konfiguracji R i S.
- Na ketony :

Ta reakcja prowadzi do powstania trzeciorzędowego alkoholu. Jeśli chodzi o aldehydy, jeśli utworzony węgiel jest asymetryczny, otrzymuje się mieszaninę R / S 50/50; w związku z tym nie ma stereoselektywności. Badanie mechanizmu reakcji pokazuje, że w rzeczywistości istnieje cykliczny związek pośredni:

- Szczególny przypadek syntezy alkoholu pierwszorzędowego :
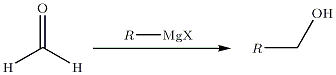 ... na estrach
... na estrach
Reakcja jest podobna do reakcji na ketonie. Po hydrolizie otrzymujemy półacetal w sposób pośredni ;
To jest niestabilne, ulega eliminacji prowadząc do powstania ketonu. Obecny organomagnez reaguje chemoselektywnie z ketonem przed estrem, który jest mniej reaktywny, ponieważ jądro węgla jego karbonylu jest w pewnym stopniu maskowane przez niewiążące elektrony tlenu połączone pojedynczym wiązaniem. Ogólna ocena reakcji prowadzi zatem do powstania trzeciorzędowego alkoholu, bez możliwości wyodrębnienia pośredniego ketonu.
... na chlorkach acylowychReakcja jest podobna do reakcji na ketonie, ale jest szybsza, ponieważ jądro węglowe związane z chlorem wykazuje ładunek dodatni bardziej atrakcyjny dla rodnika magnezoorganicznego.
R ---- Mg ---- X + R'-CO-Cl → R'-CO-R + Cl-Mg-X
Dlatego reakcja prowadzi do powstania dającego się wyodrębnić ketonu, jeśli nie ma zbyt dużo organomagnezu. Ten niestabilny keton będzie reagował ze środkiem magnezoorganicznym znajdującym się w środowisku reakcji zgodnie z następującą reakcją: R'-CO-R + RMgX → R-R'COMgX-R, a następnie pod działaniem H2O otrzymamy trzeciorzędowy alkohol. Jeśli chcemy zatrzymać się na etapie ketonowym, musimy pracować przy -65 ° C
... na CO 2
Stosowanie dwutlenku węgla w postaci suchego lodu . Reakcja w -40 ° C prowadzi do powstania kwasu karboksylowego R-COOH.
Uwagi i odniesienia
- Victor Grignard , „ O niektórych nowych metaloorganicznych kombinacjach magnezu i ich zastosowaniu w syntezach alkoholi i węglowodorów ”, Cotygodniowe raporty z sesji Académie des sciences , t. 130, 1900, s. 1322-1325 ( czytaj online )
- (w) „ Nagroda Nobla w dziedzinie chemii w 1912 r. ” (Dostęp 27 października 2018 r . ) .




