Rodzinna hipercholesterolemia
Rodzinna hipercholesterolemia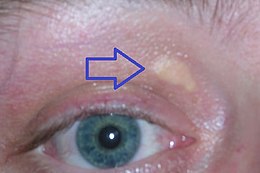 Xanthelasma , złogi lipidów koloru płowożółtego (pomarańczowo-żółtego) w kącie nosa oka na powiece, jeden z objawów klinicznych rodzinnej hipercholesterolemii.
Xanthelasma , złogi lipidów koloru płowożółtego (pomarańczowo-żółtego) w kącie nosa oka na powiece, jeden z objawów klinicznych rodzinnej hipercholesterolemii.
| Specjalność | Endokrynologia |
|---|
| ICD - 10 | E78.0 |
|---|---|
| OMIM | 143890 |
| DiseasesDB | 4707 |
| MedlinePlus | 000392 |
| eMedycyna | 121298 |
| Siatka | D006938 |
| Lek | Statyna , kolesewelam ( in ) , rosuwastatyna i ezetymib |
FH jest zaburzeniem genetycznym odpowiedzialnym za znaczący wzrost poziomu we krwi cholesterolu (przede wszystkim, że z lipoproteiny o małej gęstości ). Głównym zagrożeniem jest wystąpienie chorób układu krążenia w młodszym wieku niż w pozostałej części populacji.
Historyczny
Związek między znaczną hipercholesterolemią a chorobami układu krążenia podejrzewano już w latach trzydziestych XX wieku, a formy rodzinne zidentyfikowano dekadę później. Autosomalnie dominująco dziedziczenia wykazano w 1964 roku i odpowiedzialność mutacją w genie LDLR w 1980 dzieło Josepha Goldsteina i Michaela Browna na ten receptor zyskały im Nagroda Nobla w dziedzinie fizjologii lub medycyny w 1985 roku.
Przyczyna
Jest to choroba genetyczna z dominacją autosomalną . Zaangażowanych jest kilka genów, kodujących białka biorące udział w syntezie i eliminacji receptorów LDL : LDL ( LDLR ), apolipoproteiny B (APOB) i konwertazy proproteiny subtylizyna / keksyna typu 9 ( PCSK9 ). Zidentyfikowano ponad 1000 mutacji w genie LDLR, które mogą być odpowiedzialne za rodzinną hipercholesterolemię.
W zależności od rodzaju mutacji mniej lub bardziej istotny może być poziom cholesterolu we krwi i jego translacja kliniczna lub progresywna.
Epidemiologia
Forma heterozygotyczna dotyka co 500 osób w populacji ogólnej. W Stanach Zjednoczonych byłby prawie dwukrotnie większy. Forma homozygotyczna dotyka 1/160 000-1 / 1 000 000 osób.
Kliniczny
Główną konsekwencją tej choroby jest wyraźny wzrost poziomu cholesterolu LDL we krwi (zwykle 2-6 g / lw postaci heterozygotycznej i 6-12 g / lw postaci homozygotycznej).
Badanie kliniczne jest na ogół słabe. Czasami jednak może zauważyć obecność żółtaków (małe, stałe, żółtawe obrzęki podskórne, zwane ksantelazmami, gdy dotyczą powiek), łuk rogówki, wszystkie świadczące o zlokalizowanych złogach tłuszczowych. Ksantomy te częściej znajdują się na grzbietach dłoni i ścięgnach Achillesa, ale te ostatnie pojawiają się około trzeciej dekady życia.
Ewolucja
W przypadku braku odpowiedniego leczenia istnieje bardzo zwiększone ryzyko wczesnej choroby sercowo-naczyniowej w tej chorobie. W postaci heterozygotycznej ryzyko rozwoju chorób układu krążenia wynosi około 50% w wieku 50 lat u mężczyzn i 60 lat u kobiet.
Atak postaci homozygotycznej jest cięższy i doprowadził, przed opracowaniem skutecznych metod leczenia, do śmierci z powodu choroby wieńcowej serca przed osiągnięciem wieku 20-30 lat.
Leczenie
Na ten temat opublikowano kilka zaleceń . Te z „European Atherosclerosis Society” pochodzą z 2013 roku. Te z „National Lipid Association” pochodzą z 2011 roku.
Są to w zasadzie statyny . Pozwala to na zmniejszenie ryzyka sercowo-naczyniowego do poziomu zbliżonego do populacji wolnej od tej choroby.
Testowane są inne cząsteczki, takie jak mipomersen czy lomitapid , które umożliwiają obniżenie poziomu cholesterolu LDL, ale na razie nie pozwalają na to, aby wykazać mniejsze ryzyko incydentów sercowo-naczyniowych. Przeciw PCSK9 są bardziej skuteczne niż statyn do obniżania poziomów cholesterolu we krwi, pewne wykazywały zmniejszenia ryzyka sercowo-naczyniowego.
Wykazano, że ewolokumab obniża poziom cholesterolu LDL o 75%
Znalezienie przypadku powinno prowadzić do badań innych członków rodziny na obecność cholesterolu we krwi.
Uwagi i odniesienia
- Muller C, Xanthomata, hipercholesterolemia, dusznica bolesna , Acta Med Scand, 1938; 89: 75–84
- Wilkinson CF Jr, Hand EA, Fliegelman MT, Essential familial hypercholesterolemia , Ann Intern Med, 1948; 29: 671–686
- Khachadurian AK, The inheritance of pierwotnej rodzinnej hipercholesterolemii , Am J Med, 1964; 37: 402–407
- Brown MS, Goldstein JL, A receptor-mediated path for cholesterol homeostasis , Science, 1986; 232: 34–47
- Leigh SE, Foster AH, Whittall RA, Hubbart CS, Humphries SE, Aktualizacja i analiza bazy danych rodzinnej hipercholesterolemii receptora lipoprotein o niskiej gęstości University College London , Ann Hum Genet, 2008; 72: 485-498
- Gidding SS, Champagne MA, de Ferranti SD i in. Agenda for familial hypercholesterolemia: A Scientific Statement from the American Heart Association , Circulation, 2015; 132: 2167-2192
- Marks D, Thorogood M, Neil HA, Humphries SE, Przegląd dotyczący diagnozy, historii naturalnej i leczenia rodzinnej hipercholesterolemii , Atherosclerosis, 2003; 168: 1-14
- z Ferranti SD, Rodday AM, Mendelson MM, Wong JB, Leslie LK, Sheldrick RC, Prevalence of familial hypercholesterolemia in the 1999-2012, United States National Health and Nutrition Examination Surveys (NHANES) , Circulation, 2016; 133: 1067- 1072
- Gill PJ, Harnden A, Familial hypercholesterolemia , BMJ, 2012; 344: e3228
- Naukowy Komitet Sterujący w imieniu Simon Broome Register Group, Ryzyko śmiertelnej choroby wieńcowej serca w rodzinnej hipercholesterolemii , BMJ, 1991; 303: 893-6
- Nordestgaard BG, Chapman MJ, Humphries SE i wsp. Rodzinna hipercholesterolemia jest niedodiagnozowana i niedostatecznie leczona w populacji ogólnej: wytyczne dla klinicystów dotyczące zapobiegania chorobie niedokrwiennej serca: stwierdzenie konsensusu Europejskiego Towarzystwa Miażdżycy , Eur Heart J, 2013; 34: 3478–390a
- Goldberg AC, Hopkins PN, Toth PP i wsp. Rodzinna hipercholesterolemia: badania przesiewowe, diagnostyka i leczenie pacjentów pediatrycznych i dorosłych: wytyczne kliniczne panelu ekspertów National Lipid Association na temat hipercholesterolemii rodzinnej , J Clin Lipidol, 2011; 5: 133–140
- Versmissen J, Oosterveer DM, Yazdanpanah M i wsp. Skuteczność statyn w rodzinnej hipercholesterolemii: długoterminowe badanie kohortowe ' ', BMJ, 2008; 337: a2423
- Raal FJ, Santos RD, Blom DJ i wsp. Mipomersen, inhibitor syntezy apolipoproteiny B, do obniżania stężenia cholesterolu LDL u pacjentów z homozygotyczną rodzinną hipercholesterolemią: randomizowane, podwójnie zaślepione, kontrolowane placebo badanie , Lancet, 2010; 375: 998-1006
- Cuchel M, Meagher EA, Theron HdT i wsp. Skuteczność i bezpieczeństwo mikrosomalnego inhibitora białka transferu trójglicerydów u pacjentów z homozygotyczną rodzinną hipercholesterolemią: jednoramienne, otwarte badanie fazy 3 , Lancet, 2013; 381: 40-46
- Shrank WH, Barlow JF, Brennan TA, „New Therapies in the Treatment of High Cholesterol” , JAMA, 2015; 314: 1443-1444
- N Engl J Med 2020; 383: 1317-1327 DOI: 10.1056 / NEJMoa2019910 https://www.nejm.org/doi/full/10.1056/NEJMoa2019910?query=TOC .