Reakcja Prinsa

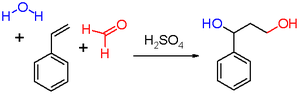
Reakcji Prins jest reakcja organiczna składa się z elektro dodanie aldehydu lub ketonu do alkenu lub alkinu, a następnie wychwytywanie nukleofilem lub usunięcia danego H + jonów . Wynik reakcji zależy od warunków reakcji. W przypadku wody i kwasu protonowego, takiego jak kwas siarkowy, jako medium reakcyjnego i formaldehydu, produktem otrzymanym w reakcji jest 1,3-diol. W przypadku braku wody, kationowy związek pośredni traci proton, dając alkohol allilowy. Przy nadmiarze formaldehydu i niskiej temperaturze reakcji, produktem reakcji jest dioksan. Gdy wodę zastępuje się kwasem octowym, powstają odpowiednie estry.
Historia
Pierwszymi odczynnikami stosowanymi przez holenderskiego chemika Hendrika Jacobusa Prinsa (de) w jego publikacji z 1919 r. Były styren (ryc. 2), pinen, kamfen, eugenol, izosafrol i anetol.
Hendrik Jacobus Prins odkrył dwie nowe reakcje organiczne podczas swoich badań doktoranckich w latach 1911-1912. Pierwszą z nich jest dodanie związku polifluorowcowego do olefin, a drugą reakcją jest katalizowany kwasem dodatek aldehydów do związków olefinowych. Pierwsze badania reakcji Prinsa miały charakter eksploracyjny i nie wzbudzały większego zainteresowania aż do 1937 roku. Rozwój krakingu ropy naftowej w 1937 roku zwiększył produkcję węglowodorów nienasyconych. W związku z tym dostępność na rynku niższej olefiny sprzężonej z aldehydem wytworzonym w wyniku utleniania parafiny o niskiej temperaturze wrzenia zwiększyła zainteresowanie badaniem kondensacji olefin-aldehydów. Później reakcja Prinsa pojawiła się jako potężna technika tworzenia wiązań CO i CC w syntezie różnych cząsteczek w syntezie organicznej.
Reakcję zbadano w ramach badań w 1937 roku nad zastosowaniem diolefin w kauczuku syntetycznym .

Mechanizm reakcji
Mechanizm reakcji dla tej reakcji jest przedstawiony na schemacie 5. Odczynnik karbonylową (2) jest protonowany kwas protonowy i do powstałego jonu oksoniowego 3 dwie struktury rezonansowe , który można wyciągnąć. Ten elektrofil angażuje się w elektrofilową addycję z alkenem w karbokokokacyjnym związku pośrednim 4.
Dokładną ilość ładunku dodatniego obecnego na drugorzędowym atomie węgla w tym półprodukcie należy określić dla każdej serii reakcji.
Istnieją dowody na udział sąsiednich grup tlenu hydroksylowego lub sąsiedniego atomu węgla. Gdy ogólna reakcja wykazuje wysoki stopień zgodności , nagromadzony ładunek będzie niewielki.
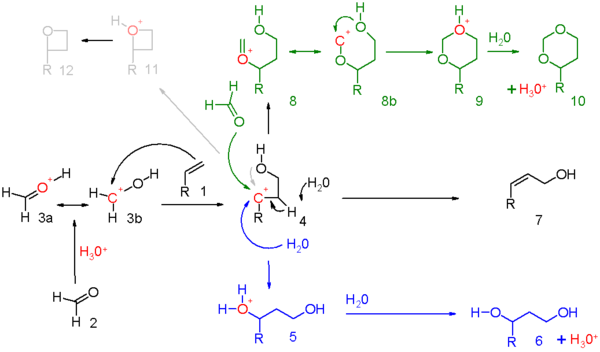
Trzy tryby reakcji otwarte dla tego związku pośredniego oksokarbenowego to:
- na niebiesko: wychwycenie karbokationu przez wodę lub dowolny odpowiedni nukleofil poprzez 5 do 1,3-addukt 6;
- w kolorze czarnym: wydzielanie protonów w reakcji eliminacji związku nienasyconego 7. Gdy alken niesie grupę metylenową, eliminację i dodanie można połączyć z przeniesieniem protonu allilowego do grupy karbonylowej, która w rzeczywistości jest enem reakcja na Schemacie 6 ;
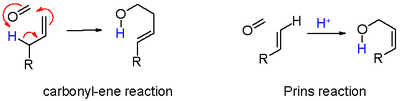
- na zielono: wychwycenie karbokationu przez dodatkowy odczynnik karbonylowy. W tym trybie ładunek dodatni jest rozpraszany na tlenie i węglu w strukturach rezonansowych 8a i 8b. Zamknięcie pierścienia prowadzi przez związek pośredni 9 do dioksanu 10. Przykładem jest konwersja styrenu do 4-fenylo-m-dioksanu;
- na szaro: tylko w określonych reakcjach i gdy karbokation jest bardzo stabilny, reakcja przebiega na skróty do oksetanu 12. Reakcja fotochemiczna Paternò-Büchi pomiędzy alkenami i aldehydami do oksetanów jest prostsza.
Wariacje
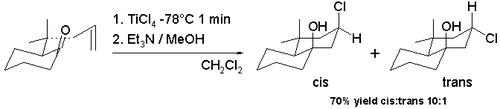
Istnieje wiele odmian reakcji Prinsa, ponieważ łatwo poddaje się ona reakcjom cyklizacji i ponieważ możliwe jest wychwycenie jonu oksokarbenowego z szeroką gamą nukleofilów. Jedną z takich modyfikacji jest reakcja halo-Prins, polegająca na zastąpieniu kwasów protonowych i wody kwasami Lewisa, takimi jak chlorek cynowy i tribromek boru . Chlorowiec jest obecnie nukleofil rekombinacji z karbokationem. Cyklizacja niektórych allilowych pulegonów ze schematu 7 z tetrachlorkiem tytanu w dichlorometanie w temperaturze -78 ° C daje dostęp do szkieletu dekaliny z grupą hydroksylową i grupą chloru głównie w konfiguracji cis (91% cis). Ta obserwowana diastereoselektywność cis wynika z pośredniego tworzenia alkoholanu trichlorotytanu, umożliwiającego łatwe dostarczanie chloru do jonu karbokationowego z tej samej powierzchni. Izomer trans jest korzystny (98% cis) przy przechodzeniu do reakcji z tetrachlorkiem cyny w temperaturze pokojowej.
Reakcja Prins-pinakol jest reakcją kaskadową reakcji Prinsa i przegrupowania pinakolu . Grupa karbonylowa w odczynniku na Schemacie 8 jest zamaskowana jako acetal dimetylowy, a grupa hydroksylowa jako eter triizopropylosililowy (TIPS). W przypadku chlorku cynowego kwasu Lewisa, jon oksoniowy jest aktywowany, a przegrupowanie pinakolu powstałego związku pośredniego Prins powoduje kurczenie się pierścienia i powrót dodatniego ładunku do eteru TIPS, który ostatecznie tworzy grupę aldehydową w produkcie końcowym jako mieszaninę Izomery cis i trans o umiarkowanej diastereoselektywności.

Kluczowy związek pośredni oksokarbenowy może być utworzony innymi drogami niż proste protonowanie karbonylu. Na kluczowym etapie syntezy eksiguolidu, ten ostatni został utworzony przez protonowanie estru winylowego:


Bibliografia
- Vijaykumar S. Marakatti , „ Projektowanie stałych katalizatorów kwasowych do reakcji prinsa i metylacji toluenu ”, INFLIBNET ,2015( czytaj online )
- RL Shriner i Philip R. Ruby, 4-Fenylo-m-dioksan , Organic Syntheses , al. lot. 4, str. 786 (1963); lot. 33, s. 72 (1953).
- R. Brandon Miles , Chad E. Davis i Robert M. Coates , „ Syn- and Anti-Selective Prins Cyclizations of δ, ε-Unsaturated Ketones to 1,3-Halohydrins with Lewis Acids ”, The Journal of Organic Chemistry , tom . 71, n o 4,2006, s. 1493–1501 ( PMID 16468798 , DOI 10.1021 / jo052142n )
- Larry E. Overman i Emile J. Velthuisen , „ Scope and Facial Selective of the Prins-Pinacol Synthesis of Attached Rings ”, The Journal of Organie Chemistry , vol. 71, n o 4,2006, s. 1581–1587 ( PMID 16468809 , DOI 10.1021 / jo0522862 )
- Min Sang Kwon , Sang Kook Woo , Seong Wook Na i Eun Lee , „ Total Synthesis of (+) - Exiguolide ”, Angewandte Chemie International Edition , vol. 47 N O 9,2008, s. 1733–1735 ( PMID 18214872 , DOI 10.1002 / anie.200705018 )
Zobacz też
- Heteropolyacid
Linki zewnętrzne
- Reakcja Prinsa w całkowitej syntezie alkaloidów , na chemii.msu.edu
- Reakcja z Prins , na organic-chemistry.org