Reakcja Bergmana
Bergman cyklizacji lub pierścień zamykający z Bergman , nazwany chemika US Robert Bergman (DE) jest reakcja przegrupowania w chemii organicznej do enediynowe pochodną rodnika z benzenu .
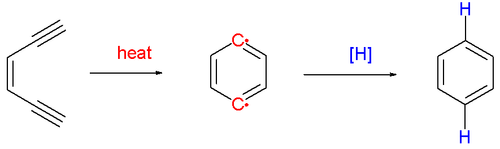
Reakcja zachodzi przez pirolizę (powyżej 200 ° C ), tworząc bardzo reaktywny związek 1,4-benzenodiylowy dwurodnikowy . Ten ostatni reaguje z donorami rodników wodorowych, takimi jak cykloheksa-1,4-dien, dając odpowiedni are . Przez traktowanie tetrachlorometan, 1,4-dichlorobenzen uzyskuje , i metanol , alkohol benzylowy .
Gdy enyn jest częścią 10-węglowego pierścienia (np. Cyklodeka-3-en-1,5-diyn na poniższym rysunku), reakcja może zachodzić w znacznie niższych temperaturach (tutaj 37 ° C ) dzięki napięciu cyklu .

Naturalne związki, takie jak kalicheamycyna, zawierają tę samą 10-węglową jednostkę pierścieniową i są cytotoksyczne . Tworzą pośredni dwuniciowy dwuniciowy, opisany powyżej, który może przecinać jednoniciowe i dwuniciowe DNA . Istnieją nowe leki oparte na tej właściwości, w tym przeciwciała monoklonalne, takie jak mylotarg .
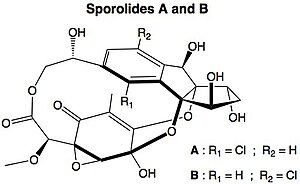
Zaproponowano również dwurodnikowy mechanizm tworzenia pewnych biomolekuł pochodzenia morskiego, sporolidów , które zawierają w swojej strukturze cholorobenzen.
W tym mechanizmie źródłem halogenu jest sól halogenkowa. Modelowa reakcja z cyklodeka-1,5-diyn-3-enem , bromkiem litu jako źródłem halogenu, kwasem octowym jako źródłem wodoru w DMSO w 37 ° C sprawia, że teoria ta jest realna:

Reakcja jest pierwszego rzędu w enedynie, z utworzeniem p- benzzynu A jako etapem ograniczającym . Jon halogenkowy, a następnie daje dwa elektrony w trakcie formowania się nowego wiązania C-Br, oraz rodniki tranzytu elektronów poprzez wiązania ulotne C1-C4, do utworzenia pośredniego anionu B . Ten anion jest potężną bazą zdolną do usuwania protonów nawet z DMSO w celu uzyskania produktu końcowego. Nie obserwuje się tworzenia związków dibromo lub diwodorowych.
Linki zewnętrzne
- (en) Bergman Cycloaromatization Powerpoint Whitney M. Erwin 2002
- (w) Portal Bergmana Cycloaromatization Organic Chemistry
Uwagi i odniesienia
- Reakcje nazwisk: zbiór szczegółowych mechanizmów reakcji autorstwa Jie Jack Li, opublikowany Springer 2003 ( ISBN 3-540-40203-9 )
- (in) Projektowanie i synteza proleków aktywowanych heterocyklicznie fuzją enediyne do woli Luca Banfi Andrea Basso Giuseppe Guanti i Renata Riva arkivoc 2006 HL-1786GR 261-275 Streszczenie
- (w) Charles L. Perrin , Betsy L. Rodgers i Joseph M. O'Connor , „ Nucleophilic Addition to a p-Benzyne Derived from year enediyne: A New Mechanism for Halide Incorporation into Biomolecules ” , Journal of the American Chemical Society , vol. 129 n O 15,2007, s. 4795-4799 ( DOI 10.1021 / ja070023e )
- Nowy sposób dodawania halogenków Stu Borman Wiadomości z dziedziny chemii i inżynierii 2 kwietnia 2007 r. Link
- ( fr ) Ten artykuł jest częściowo lub w całości zaczerpnięty z artykułu w angielskiej Wikipedii zatytułowanego „ Bergman cyclization ” ( zobacz listę autorów ) .