Julia olefinacja
Julia olefinowania (lub Julia-Lythgoe olefinowania ), który wykonuje swoją nazwę Marc Julia , jest reakcją umożliwiając uzyskanie alkenu ( 3 ) przed atakiem fenyl sulfonu ( 1 ) na aldehydu lub ketonu , a następnie przez funkcjonalizację alkoholu i redukcyjną eliminację przy użyciu amalgamatu sodu lub jodku samaru (II).
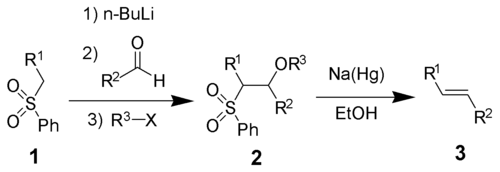
Ta reakcja silnie sprzyja tworzeniu trans alkenu .
Mechanizm reakcji
Po deprotonowaniu anion fenylosulfonowy ( 2 ) atakuje aldehyd, tworząc alkoholan 3 . Jest to funkcjonalizowane przez R 3 X, dając stabilny produkt pośredni 4 . Dokładny mechanizm redukcji przez amalgamat sodu nie jest znany, ale wykazano, że przechodzi on przez rodnik winylowy ( 5 ). Protonowanie rodnika winylowego daje oczekiwany produkt ( 6 ).

Stereochemia otrzymanego alkenu jest niezależna od stereochemii pośredniego sulfonu 4 . Można sobie wyobrazić, że rodnik pośredni jest w równowadze i uzyskuje się produkt najbardziej stabilny termodynamicznie.
Bibliografia
- (en) GE Keck , KA Savin i wsp. , „ Use of Samarium Diiodide as an Alternative to Sodium / Mercury Amalgam in the Julia-Lythgoe Olefination ” , J. Org. Chem. , vol. 60 N O 10,1995, s. 3194–3204 ( ISSN 0022-3263 , DOI 10.1021 / jo00115a041 ).
- M. Julia i J.-M. Paris , „ Syntheses using V (+) sulfones - method of general synthesis of double binding ”, Tetrahedron Lett. , vol. 14 N O 49,1973, s. 4833–4836 ( ISSN 0040-4039 , DOI 10.1016 / S0040-4039 (01) 87348-2 ).
- (en) PJ Kocienski , B. Lythgoe i wsp. , „ Zakres i stereochemia syntezy olefin z β-hydroksysulfonów ” , J. Chem. Soc., Perkin Trans. 1 , N O 8,1978, s. 829-834 ( ISSN 0300-922X , DOI 10.1039 / P19780000829 ).
Bibliografia
Na ten temat opublikowano kilka recenzji:
- (en) PJ Kocienski , „ Recent Sulphone-Based Olefination Reactions ” , Phosphorus Sulphur Silicon Relat. Elem. , vol. 24, n kość 1-2,1985, s. 97-127 ( ISSN 1042-6507 , DOI 10.1080 / 03086648508073398 ).
- Kelly, SE Comp. Org. Syn. 1991 , 1 , 792-806. (Przejrzeć)
- ( fr ) Ten artykuł jest częściowo lub w całości zaczerpnięty z artykułu Wikipedii w języku angielskim zatytułowanego „ Julia olefination ” ( zobacz listę autorów ) .