Eliminacja redukcyjna
Redukcyjna eliminacja jest podstawowy krok w Organometallic Chemistry , w których stan utlenienia centrum metalu zmniejsza się podczas wytwarzania nowe kowalencyjne wiązanie pomiędzy dwoma ligandami . Jest to reakcja odwrotna addycji utleniającej i często jest etapem tworzenia produktu w wielu procesach katalitycznych. Ponieważ addycja oksydacyjna i redukcyjna eliminacja są reakcjami odwrotnymi, te same mechanizmy mają zastosowanie do obu procesów, a równowaga produktu zależy od termodynamiki obu reakcji.
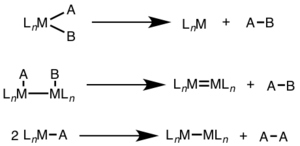
Eliminacja redukcyjna jest często obserwowana na wysokich stopniach utlenienia i może obejmować zmianę dwuelektronową w pojedynczym centrum metalu (jednojądrzastym) lub zmianę jednego elektronu w każdym z dwóch centrów metalu (dwupierścieniową, dwupierścieniową lub bimetaliczną).
W przypadku monojądrowej eliminacji redukcyjnej stopień utlenienia metalu zmniejsza się o dwa, podczas gdy liczba elektronów na orbitali d metalu wzrasta o dwa. Ta ścieżka jest wspólna dla metali d 8 (Ni (II), Pd (II) i Au (III)) id 6 metali (Pt (IV), Pd (IV), Ir (III) i Rh (III)). Ponadto eliminacja jednojądrowa redukcyjna wymaga, aby usuwane grupy znajdowały się w pozycji cis względem siebie na metalowym środku.

W przypadku dwujądrowej eliminacji redukcyjnej stopień utlenienia każdego metalu zmniejsza się o jeden, podczas gdy liczba d elektronów każdego metalu wzrasta o jeden. Ten typ reaktywności jest na ogół obserwowany w przypadku metali pierwszej linii, które preferują zmianę stopnia utlenienia o jedną jednostkę, ale zaobserwowano go w przypadku metali drugiej i trzeciej linii.
Podobnie jak w przypadku dodatku utleniającego, istnieje kilka mechanizmów eliminacji redukcyjnej. Dominującym mechanizmem jest mechanizm uzgodniony , co oznacza, że jest to trójcentryczny niepolarny stan przejściowy z zachowaniem stereochemii . Ponadto mechanizm S N 2 , który przebiega przez odwrócenie stereochemii lub mechanizm rodnikowy , który przebiega przez względną inwersję stereochemii, są innymi możliwymi drogami eliminacji redukcyjnej.
Uwagi i odniesienia
- Robert H. Crabtree , Organometallic Chemistry of the Transition Metals , Wiley,2014, 173 pkt. ( ISBN 978-1-118-13807-6 )
- John F. Hartwig , Organotransition Metal Chemistry, from Bonding to Catalysis , University Science Books,2010, 321 str. ( ISBN 978-1-891389-53-5 )
- Gillie i Stille, „ Mechanizmy 1,1-redukcyjnej eliminacji z palladu ”, J. Am. Chem. Soc. , vol. 102 n O 15,1980, s. 4933–4941 ( DOI 10.1021 / ja00535a018 )
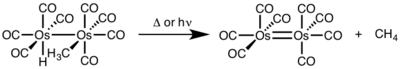
- Okrasinski and Nortom, „ Mechanism of Reductive Elimination. 2. Kontrola Dinuclear vs. Mononuclear Elimination of Methane from cis-Hydridomethyltetracarbonylosmium ”, J. Am. Chem. Soc. , vol. 99,1977, s. 295–297 ( DOI 10.1021 / ja00443a076 )
- Crabtree, Robert H. (2014). Organometallic Chemistry of the Transition Metals (wyd. 6). Wiley. p. 173. ( ISBN 978-1-118-13807-6 ) .