Reakcja Suzuki
Reakcja Suzuki , Suzuki-Miyaura reakcji lub reakcji sprzęgania Suzuki-Miyaura jest reakcja sprzęgania i stosowane w chemii organicznej , w której grupy arylowa i drugi skrapla grupę arylową, z wytworzeniem pojedynczej cząsteczki. Zwykle, tę reakcję z użyciem kwas poddaje się reakcji z chlorowcem pochodnej taki jak atom bromu lub jodu, z katalizatorem palladu . Ta reakcja chemiczna została po raz pierwszy opublikowana w 1979 roku przez Akirę Suzuki (鈴木 章) (który otrzymał Nagrodę Nobla w dziedzinie chemii w 2010 roku za to odkrycie) i Norio Miyaura (宮 浦 憲 夫). Reakcja wymaga katalizatora palladowego zawierającego ligandy fosfinowe .

Warunki reakcji
Ta reakcja działa również przy użyciu grupy trifluorometanosulfonianowej (OTf) zamiast pochodnej chlorowcowanej , a także zastosowania estru boronowego zamiast kwasu boronowego. Następującą względną reaktywność zwykle obserwuje się dla każdej grupy stosowanej podczas reakcji sprzęgania : R 2 -I> R 2 -OTf> R 2 -Br >> R 2- Cl.
Mechanizm reakcji
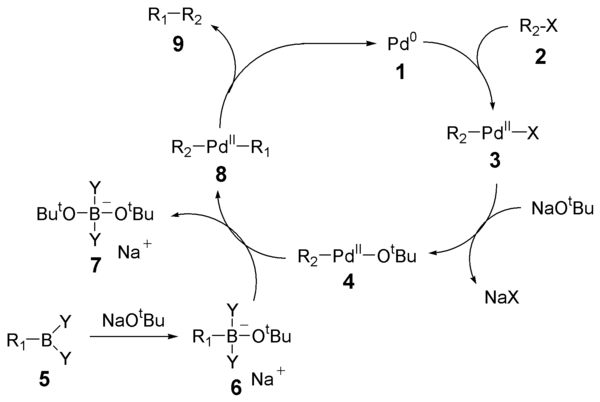
Cykl katalityczny sprzęgła Suzuki składa się z czterech odrębnych etapów:
- utleniające dodanie halogenku 2 do katalizatora palladowego Pd (0) 1 z wytworzeniem Pd (II) 3 ;
- wymiana anionu związanego z palladem z anionem zasady: metateeza, która daje 4 ;
- Transmetalowania pomiędzy Pd (II) 4 i boranu alkilu kompleks 6 ;
- eliminacja redukcyjna w celu utworzenia wiązania σ C-C 9 i regeneracji katalizatora Pd (0) 1 .
Czwartorzędowy boru anion zwiększa nukleofilowości z arylem grupa R 1 i przyspiesza jego transfer do palladu w czasie transmetalacji etapie . Wybór ligandów z katalizatora wpływa na reaktywność. Z ligandami o dużych rozmiarach i bogatych w elektrony jako P ( t -Bu) 3 przyspieszyć szybkość etapu dodawania oksydacyjnego reakcji chlorków zazwyczaj niereaktywne.
Uwagi i odniesienia
- (en) N. Miyaura , K. Yamada i in. , „ Nowe stereospecyficzne sprzęganie krzyżowe przez katalizowaną palladem reakcję 1-alkenyloboranów z halogenkami 1-alkenylu lub 1-alkinylu ” , Tetrahedron Lett. , vol. 20 N O 36,1979, s. 3437–3440 ( ISSN 0040-4039 , DOI 10.1016 / S0040-4039 (01) 95429-2 ).
- (En) N. Miyaura i A. Suzuki , „ Stereoselective synthesis of arylated ( E ) -alkenes by the reaction of alk-1-enylboranes with aryl halides in the present of palladium catalal ” , J. Chem. Soc., Chem. Wspólny. , N O 19,1979, s. 866-867 ( ISSN 0022-4936 , DOI 10.1039 / C39790000866 ).