Walina
| Walina | |
 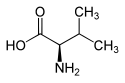 L lub S (+) - walina i D lub R (-) - walina |
|
| Identyfikacja | |
|---|---|
| Nazwa IUPAC | Kwas 2-amino-3-metylobutanowy |
| Synonimy |
V, Val |
| N O CAS |
(racemiczny) (L) lubS(+) (D) lubR(-) |
| N O ECHA | 100,000,703 |
| N O WE | 200-773-6 (L) 211-368-9 (D) |
| FEMA | 3444 |
| Właściwości chemiczne | |
| Brute formula |
C 5 H 11 N O 2 [Izomery] |
| Masa cząsteczkowa | 117,1463 ± 0,0056 g / mol C 51,26%, H 9,46%, N 11,96%, O 27,32%, |
| pKa | 2,3 (COOH) i 9,6 (NH2) |
| Właściwości biochemiczne | |
| Kodony | GUU, GUC, GUA, GUG |
| izoelektryczne pH | 5.96 |
| Niezbędny aminokwas | tak |
| Występowanie u kręgowców | 6,8% |
| Środki ostrożności | |
| WHMIS | |
|
Produkt niekontrolowanyTen produkt nie jest objęty kontrolą zgodnie z kryteriami klasyfikacji WHMIS. |
|
| Jednostki SI i STP, chyba że określono inaczej. | |
Walina (Skróty IUPAC - IUBMB : Val i V ) jest kwaśny α-aminokwas, którego enancjomer L jest jednym z 22 tworzących białka aminokwasów , a jedna z dziewięciu aminokwasów dla człowieka . Charakteryzuje się niepolarną grupą izopropylową . Jego nazwa pochodzi od waleriany . Jest kodowana na informacyjnych RNA przez Guu, GUC, Gua i Gug kodonów .
Jego łańcuch boczny ma rozgałęziony i symetryczny alifatyczny charakter .
Biosynteza
Walina jest biosyntetyzowana w roślinach w kilku etapach z kwasu pirogronowego . Następnie powstaje związek pośredni, α-ketoizowalerianian, który ulega redukcyjnej aminacji z glutaminianem. W biosyntezie biorą udział enzymy:
- Syntaza acetylomleczanowa ;
- Acetohydroksyizomeroreduktaza ;
- Dehydrataza kwasu dihydroksykwasowego ;
- Aminotransferaza walinowa .
Pierwsza część tej ścieżki metabolicznej również wytwarza leucynę .
Uwagi i odniesienia
- obliczona masa cząsteczkowa od „ atomowych jednostek masy elementów 2007 ” na www.chem.qmul.ac.uk .
- (w) Francis A. Carey, „ Tabela PK i wartościach pH ” , w Wydziału Chemii na Uniwersytecie w Calgary , 2014(dostęp 26 lipca 2015 )
- (w) Mr. Beals, L. Gross, S. Harrell, " Amino Acid Frequency " on The Institute for Environmental Modeling (ITSH) to the University of Tennessee (dostęp: 26 lipca 2015 )
- „ Walina (l) ” w bazie produktów chemicznych Reptox z CSST (Quebec organizacji odpowiedzialnej za bezpieczeństwo i higienę pracy), dostęp 25 kwietnia 2009
- http://www.nutrition-expertise.fr/acides-amines/ordre-alphabetique/383-valine.html
- Lehninger, Albert L.; Nelson, David L.; Cox, Michael M. (2000), Principles of Biochemistry ( 3rd ed.), New York: WH Freeman, ( ISBN 1-57259-153-6 ) .