Niewydolność oddechowa
Niewydolność oddechowa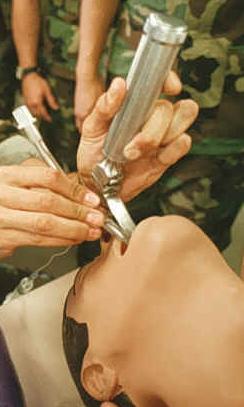 Intubacja ustno-tchawicza (tutaj pokazana na manekinie) jest leczeniem zaburzeń oddechowych.
Intubacja ustno-tchawicza (tutaj pokazana na manekinie) jest leczeniem zaburzeń oddechowych.
| Specjalność | Medycyna ratunkowa, pulmonologia i resuscytacja. |
|---|
| CISP - 2 | R99 |
|---|---|
| ICD - 10 | J96.0 |
| ChorobyDB | 6623 |
| eMedycyna | 167981 |
| eMedycyna | med / 2011 |
| Siatka | D012131 |
| Objawy | Duszność , sinica . |
| Powoduje | Choroba płuc , niewydolność serca , zespół ostrej niewydolności oddechowej , dekompensacja POChP . |
| Leczenie | Terapia tlenowa i leczenie przyczyny. |
Niewydolności oddechowej jest niewydolność oddechowa nagle występujących i objawiającego się dusznością Ważne (duszność). Układ oddechowy nie jest już w stanie zapewnić normalnej wymiany gazowej tlenu i dwutlenku węgla . Jest to nagły przypadek medyczny, który może zagrażać życiu pacjenta i powoduje około jednej trzeciej hospitalizacji na oddziałach intensywnej terapii.
Istnieją dwa główne rodzaje niewydolności oddechowej: hipoksemiczna , gdy obniża się tylko ciśnienie parcjalne tlenu we krwi tętniczej, oraz hiperkapniczna , gdy dodawane jest zwiększenie ciśnienia parcjalnego dwutlenku węgla .
Rozpoznanie niewydolności oddechowej ma przede wszystkim charakter kliniczny: potrzeba kilku dodatkowych badań, a wśród nich dominuje pomiar zawartości tlenu we krwi saturometrem , badanie gazów krwi próbką tętniczą i klatką piersiową x -promień . Inne badania pozwolą jednak doprecyzować diagnozę etiologiczną i zidentyfikować proces powodujący niepowodzenie.
Zarówno dorośli, jak i dzieci mogą cierpieć na niewydolność oddechową. U dorosłych, zakażeń płucnych , decompensations z przewlekłym zapaleniem oskrzeli , zespół ostrej niewydolności oddechowej (ARDS) i niewydolność serca są jednymi z najczęstszych przyczyn. U małych dzieci najbardziej zaangażowane jest zapalenie oskrzelików i bakteryjne infekcje płuc. U noworodków chodzi głównie o ARDS i wdychanie smółki .
Leczenie niewydolności oddechowej opiera się przede wszystkim na dodatkowej podaży tlenu wziewnego. Można to osiągnąć w pierwszej kolejności za pomocą okularów tlenowych , maski o wysokim stężeniu lub wysokoprzepływowego systemu do tlenoterapii donosowej . Jeśli to leczenie jest niewystarczające, ustawiana jest pomoc wentylacyjna . Może to być nieinwazyjne , przez maskę nosowo-wargową dostarczającą pacjentowi sprężone powietrze lub inwazyjne, przez intubację dotchawiczą . W ostateczności w niektórych przypadkach można rozpocząć pozaustrojowe natlenianie błonowe (ECMO). Równolegle leczy się przyczynę niewydolności oddechowej.
Po leczeniu następują głównie objawy, pulsoksymetr i gazometria krwi tętniczej.
Rokowanie zaburzeń oddechowych jest bardzo zmienne w zależności od przyczyny. Ogólnie śmiertelność wynosi około 30%, a większa w przypadku pacjentów w ekstremalnych wieku życia, w tym z istotnych chorób współistniejących i tych o większej początkowej ciężkości. U pacjentów, którzy przeżyli, powrót czynności płuc jest długi, ale następstwa oddechowe są na ogół umiarkowane. Jakość życia może jednak pozostać obniżona przez kilka lat.
Epidemiologia
Częstość występowania niewydolności oddechowej w Europie Zachodniej wynosi od 78 do 150 na 100 000 mieszkańców.
Badanie przeprowadzone w 2002 roku na około 1500 dorosłych pacjentach przyjętych na oddziały intensywnej terapii w 16 krajach wykazało, że 32% zostało przyjętych z powodu niewydolności oddechowej. Wśród pacjentów przyjętych z innych powodów 35% prezentowało niewydolność oddechową w trakcie ich początkowej patologii.
W odniesieniu do dzieci jest to częsty powód przyjęcia na oddział intensywnej opieki pediatrycznej, dotykający nawet dwie trzecie pacjentów. W brytyjskim badaniu dotyczącym powodów przyjęcia na dziecięce oddziały intensywnej opieki medycznej przyczyny oddechowe dotyczyły 20% dzieci w 1982 r., 19% w 1995 r. i 27% w 2006 r.
Definicja i patofizjologia
Ogólny
Ostra niewydolność oddechowa występuje, gdy układ oddechowy nagle nie zapewnia wymiany gazowej tlenu i dwutlenku węgla . Zwykle określa się ją na podstawie analizy gazów rozpuszczonych we krwi tętniczej . Tętnicze ciśnienie cząstkowe tlenu ( PaO 2 ) mniejszą niż 60 mm Hg (czyli 8,0 kPa ) jest wartością progową w celu określenia stanu niedotlenienia . Znajduje to odzwierciedlenie w zmniejszeniu oksymetrem pulsowym , przy saturacji obwodowej (SPO 2 ) pomiędzy 80 a 94%.
Rodzaje zaburzeń oddechowych
Generalnie wyróżniamy:
- hipoksemiczna niewydolność oddechowa , znana jako „typ 1”,
- hiperkapniczna niewydolność oddechowa , znana jako „typ 2”.
- Niektórzy lekarze rozróżniają również ostrą niewydolność oddechową, znaną jako „typ 3” (w kontekście okołooperacyjnym) i „typ 4” (występujący w stanie wstrząsu hemodynamicznego ).
Hipoksemiczna niewydolność oddechowa
Hipoksemiczna niewydolność oddechowa może wystąpić w kilku okolicznościach prowadzących do niewydolności samego płuca: nieodpowiedni stosunek wentylacji do perfuzji, pojawienie się efektu przecieku , upośledzona dyfuzja pęcherzykowo-włośniczkowa lub hipowentylacja pęcherzykowa.
Hiperkapniczna niewydolność oddechowa
Hiperkapniczna niewydolność oddechowa występuje podczas nieprawidłowości w mechanice wentylacji uniemożliwiających eliminację CO 2 . Niedotlenienie następnie towarzyszyć hiperkapnii zdefiniowany przez PaCO 2 większy niż 45 mm Hg (czyli 6,0 kPa ). Nagromadzenie CO 2 obniża pH krwi; kwasicy oddechowej rozstrzygane gdy staje się mniejszy niż 7,35 .
Szczególny przypadek dzieci
Dzieci, zwłaszcza młodsze, częściej niż dorośli mają problemy z oddychaniem. Rzeczywiście, mniejsze odcinki ich dróg oddechowych zwiększają opór przepływu powietrza i ułatwiają niedrożność oskrzeli przez wydzieliny lub obrzęki. Mniejsza sztywność ściany klatki piersiowej również przyczynia się do zwiększonej pracy oddechowej. Przepona i dodatkowe mięśnie oddechowe również zawierają mniej powolnych włókien mięśniowych niż u osób dorosłych, co sprzyja wyczerpaniu oddechowemu. Wreszcie bardzo małe dzieci mają niedojrzały układ nerwowy, który predysponuje je do bezdechów i bradypnei .
Objawy kliniczne
Rozpoznanie niewydolności oddechowej ma przede wszystkim charakter kliniczny i można je postawić bezpośrednio przy łóżku pacjenta. Obraz kliniczny łączy w sobie bezpośrednie konsekwencje ataku na układ oddechowy i zastosowane przez organizm środki kompensacyjne.
Objawy walce są zdominowane przez zwiększenie szybkości oddychania ( polypnea ), które mogą być związane z napinania mięśni oddechowych.
Oznaki nasilenia, zwane również oznakami bankructwa, różnią się w zależności od dotkniętych narządów. Odzwierciedlają one globalny wpływ zaburzeń oddechowych i najczęściej wskazują na potrzebę wspomagania wentylacji. Na poziomie oddechowym głównymi objawami są paradoksalne oddychanie brzuszne i sinica . Tej ostatniej może brakować w przypadku poważnej anemii , jeśli poziom hemoglobiny jest niższy niż 5 g · dl -1 . Neurologicznie hiperkapnia, jeśli jest obecna, powoduje asteryksję i zaburzenia czujności i zachowania (pobudzenie lub śpiączka). Wreszcie w planie krążenia ostra serce płucne to niewydolność prawokomorowa. Towarzyszy jej paradoksalny puls i może wiązać się z niewydolnością układu krążenia aż do wstrząsu .
W przypadku hiperkapnii obraz może być uzupełniony obfitym poceniem.
Pacjenci, zarówno dorośli, jak i dzieci, nosiciele chorób nerwowo-mięśniowych, mogą wykazywać niewiele objawów klinicznych; w tych populacjach należy łatwo wywołać niewydolność oddechową i wykonać pomiar gazów tętniczych. U osób starszych mniej wyraźne objawy kliniczne mogą prowadzić do błądzenia diagnostycznego.
Dodatkowe testy
Pomiary stałych fizjologicznych ( częstotliwość serca i oddechów , ciśnienie krwi , saturacja krwi ) uzupełniają badanie kliniczne i pozwalają na szybką ocenę powagi sytuacji. Niewiele dodatkowych badań jest koniecznych do ustalenia diagnozy niewydolności oddechowej. W sytuacjach nagłych prześwietlenie klatki piersiowej i gazometria krwi tętniczej są jedynymi badaniami wymaganymi do postawienia diagnozy. Zgodnie z pierwszymi elementami orientacji można by jednak przeprowadzić inne badania w celu określenia przyczyny niewydolności oddechowej. Nie powinny jednak opóźniać rozpoczęcia leczenia.
Standardowe badanie krwi może wskazać przyczynę: hiperleukocytoza w przypadku infekcji bakteryjnej, wzrost CRP w przypadku zapalenia, wzrost D-dimeru w przypadku zatorowości płucnej , BNP w przypadku niewydolności serca.
Echokardiografii i opłucnej mogą być pomocne w różnicowaniu przyczyn niedotlenienia krwi niewydolności oddechowej. Tomografii komputerowej (CT), pierś może wyglądać zator płuc, zwłóknienie znaki lub określić bardziej precyzyjnie zmian uwidocznionych na rtg klatki piersiowej. W kontekście zakaźnym (gorączka lub ropna plwocina) analiza plwociny , a także posiewy krwi mogą umożliwić poszukiwanie odpowiedzialnych zarazków. Grypa jest systematycznie poszukiwane podczas epidemii w gorączkowej pacjenta.
Bronchoskopię może być wskazana, gdy przyczyną zaburzeń oddychania nie jest oczywiste. Umożliwia pobranie próbek do celów bakteriologicznych, ale także zbadanie morfologii drzewa oskrzelowego poprzez wykonanie w razie potrzeby biopsji oraz wykonanie płukania oskrzelowo-pęcherzykowego .
Procedura diagnostyczna
Istnieje wiele przyczyn zaburzeń oddechowych. Rozpoznanie etiologiczne opiera się na badaniu klinicznym, uzupełnionym o RTG klatki piersiowej i badanie gazowe tętnic.
Pierwszym krokiem diagnostycznym jest sprawdzenie swobody górnych dróg oddechowych. Ta diagnoza ma charakter kliniczny. Wdychanie ciała obcego jest najczęstszą przyczyną u dzieci i osób w podeszłym wieku z zaburzeniami połykania, ale każda choroba powoduje krtani lub tchawicy ENT niedrożności może być zaangażowany. Może więc wystąpić guz krtani , zwężenie tchawicy , zapalenie nagłośni lub obrzęk naczynioruchowy . Gdy drogi oddechowe są wolne, prześwietlenie klatki piersiowej i osłuchiwanie mogą zdiagnozować uszkodzenie opłucnej i miąższu płucnego . Na poziomie opłucnej, każdy wysięk o dużej obfitości ( odma opłucnowa lub wysięk płynowy ) może powodować niewydolność oddechową. Na poziomie płuc niedodma to brak wentylacji mniej lub bardziej ważnego terytorium, często przez niedrożność mechaniczną. Do chorób płuc , w szczególności bakterii, które wpływają na znaczne objętości płuc są powszechną przyczyną niewydolności oddechowej, jak obrzęk płuc, czy serca ( ostry obrzęk płuc ) lub uszkodzenie ( zespół ostrej niewydolności oddechowej i ARDS). W tym drugim przypadku ważne jest, aby pamiętać, że zapalenie płuc, bakteryjne lub wirusowe (na przykład Covid-19 ), może być przyczyną ARDS. Wreszcie, ataki śródmiąższowej choroby płuc mogą być przyczyną niewydolności oddechowej. U pacjentów leczonych z powodu choroby nowotworowej ważne jest określenie daty ostatniej chemioterapii i ewentualnie przeszczepienia szpiku kostnego . Rzeczywiście, te terapie mogą prowadzić do immunosupresji, a następnie należy szukać infekcji oportunistycznych.
Gdy radiografia i badanie kliniczne nie są bardzo pomocne, pomiar gazu tętniczego umożliwia ukierunkowanie diagnozy. Prawidłowość kapnii (ciśnienie CO 2 ) i pH wskazuje na zatorowość płucną lub ciężką ostrą astmę . Zator będzie poszukiwany przez tomografię komputerową klatki piersiowej; badanie fizykalne może być bardzo szorstkie, ale obejmuje również objawy niewydolności prawokomorowej i ostrego serca płucnego, zwłaszcza w przypadku masywnej i proksymalnej zatorowości. Gdy pomiary gazów wskazują na kwasicę oddechową, która objawia się wzrostem kapnii i wodorowęglanów, niewydolność oddechowa jest zwykle wynikiem dekompensacji przewlekłej patologii. Najczęściej jest to zaostrzenie przewlekłej obturacyjnej choroby płuc (POChP). Mogą być zaangażowane uszkodzenia nerwowo-mięśniowe, takie jak miastenia gravis lub zespół Guillain-Barré . Polio były częstą przyczyną do wprowadzenia szczepionki; wentylację płucną pacjentów zapewniało następnie, po ostrej fazie, stalowe płuco . Wreszcie uszkodzenie ciemieniowe może być również odpowiedzialne za niewydolność oddechową. Te wielokrotne złamania żeber , mogą być uwzględnione w szczególności pacjentów, których stan podstawowy wentylacji jest niepewna. Do miopatii , wrodzone lub nabyte, są także czasami zaangażowany, za naruszenie mięśni wdechowych. W przypadku tych przewlekłych chorób należy szukać pierwiastka, który spowodował dekompensację: nadkażenie oskrzeli, zator tętnicy płucnej, pneumopatia, operacja klatki piersiowej czy niewydolność lewego serca mogą być wtedy również odpowiedzialne za niewydolność oddechową. Może również wystąpić zatrucie opiatami lub innymi substancjami o działaniu depresyjnym na układ oddechowy.
Powoduje
Niewydolność oddechowa jest wywoływana przez brak surfaktanta płucnego (surfaktant, którego białka powierzchniowo czynne nie tylko ułatwiają wymianę tlenu i CO2, ale chronią przed wirusami, takimi jak grypa A ). Ten niedobór surfaktanta może mieć wiele przyczyn, czasami nasilany u mężczyzn, ponieważ produkcja surfaktanta płucnego jest powiązana z układem hormonalnym i głównie kontrolowana przez chromosom X (ludzie mają tylko jeden). Jest hamowany na przykład przez dihydrotestosteron u płodu męskiego i żeńskiego. Odwrotnie, antyandrogen (np. flutamid ) hamuje dymorfizm płciowy w produkcji surfaktantów.
U dorosłych
U dorosłych, ze względu na bardzo niejednorodne badania, brakuje danych na temat globalnego rozmieszczenia różnych przyczyn zaburzeń oddechowych.
W badaniu z 1995 r. na niemieckiej kohorcie stwierdzono infekcje płuc (15%, w tym zachłystowe zapalenie płuc ) jako najczęstszą etiologię, a następnie przyczyny sercowe ze wstrząsem kardiogennym (13%) i niewydolnością lewego serca (7, 6%).
Skandynawska kohorta badana w 1999 roku wykazała infekcje płuc (23%) jako główną przyczynę, następnie niedodmę (15%) i dekompensację przewlekłej obturacyjnej choroby płuc (13%), a następnie niewydolność lewego serca (9%); wstrząs kardiogenny dotyczy tylko 5% przypadków.
Analiza kohorty brazylijskiej przeprowadzonej w 2011 r. w oddziałach intensywnej opieki medycznej i chirurgicznych wykazała, że jako główną przyczynę niewydolności oddechowej zespół ostrej niewydolności oddechowej (ARDS) (10%), a następnie zapalenie płuc (8%), nie- posocznica płucna (7%), niewydolność serca (6%) i uraz klatki piersiowej (6%). Jednak u większości pacjentów (38%) bezpośrednio po operacji wystąpiła ostra niewydolność oddechowa.
Pozaszpitalne bakteryjne zapalenie płuc wiąże się z hospitalizacją tylko w 20% przypadków; tylko 10% z nich będzie miało niewydolność oddechową. Jednak u pacjentów z obniżoną odpornością niewydolność oddechowa jest pierwszą przyczyną hospitalizacji na oddziale intensywnej terapii i intensywnej terapii, głównie z powodu infekcji płuc; Może to być zarówno klasyczne społeczność - ponoszone zapalenie płuc, a także jako zakażenia oportunistyczne , w szczególności zakażeń grzybiczych. Rzadziej może to być efekt uboczny niektórych terapii przeciwnowotworowych, zwłaszcza chemioterapii, a niektóre terapie celowane mogą być odpowiedzialne za zapalenie płuc z nadwrażliwości, takie jak śródmiąższowe zapalenie płuc . Jednak u pacjentów z czynną chorobą nowotworową najczęstszą przyczyną jest bakteryjne zapalenie płuc (47%), następnie infekcje oportunistyczne (31%), aw 22% przypadków przyczyny niezakaźne.
ARDS dotyczy od 1,7 do 19,5% wszystkich pacjentów przyjętych na oddziały intensywnej terapii dla dorosłych, przy czym najczęściej podaje się liczby na poziomie około 7%.
W śródmiąższowej chorobie płuc, takiej jak idiopatyczne zwłóknienie płuc , niewydolność oddechowa może wystąpić w dwóch głównych przypadkach. U pacjentów już zdiagnozowanych ostre zaostrzenie odpowiada pogorszeniu przez mniej niż miesiąc stanu oddechowego i zmian obserwowanych w obrazowaniu, bez towarzyszącej patologii płucnej. Zaburzeń oddechowych może być jednak sposobu wykrywania choroby śródmiąższowej, zwłaszcza do płuc, idiopatyczne zwłóknienie connectivitis i zapalenie naczyń z udziałem płuc i zwłóknienie polekowego.
U dzieci
Główną przyczyną niewydolności oddechowej u noworodków ( zwykle wcześniaków ) jest niedobór surfaktantów płucnych . Temu niepokojowi można zapobiec stosując przedporodową terapię kortykosteroidami (która jest jednak bardziej skuteczna u dziewcząt niż u chłopców); ta różnica w wytwarzaniu surfaktantów płucnych płodu w zależności od płci jest również obserwowana w modelu zwierzęcym , na który a priori wpływa receptor androgenowy (AR).
Zabieg ten znacząco zmniejszył liczbę chorób błony szklistej i przyczynił się do zmniejszenia śmiertelności niemowląt (mniejsza zachorowalność i śmiertelność wcześniaków).
U noworodków w okresie przedterminowym najczęstszą przyczyną niewydolności oddechowej u 43% pacjentów jest ARDS, następnie inhalacja smółki (9,7%) oraz zapalenie płuc lub posocznica (8, 3%). Przemijający szybki oddech noworodka jest zaangażowany w 4% przypadków, ale szczególnie często u dzieci urodzonych przez cesarskie cięcie, nawet u dzieci urodzonych o czasie. W przypadku braku przejścia płodu w zwężonym kanale rodnym, płuca w rzeczywistości nie są wypłukiwane z zawartego w nich płynu płucnego płodu.
Rzadziej niektóre wrodzone wady serca mogą również powodować niewydolność oddechową.
U małych dzieci zapalenie oskrzelików odpowiada za 26,7% niewydolności oddechowej, a bakteryjne zapalenie płuc 15,8%. Zmiany w obrzękach płuc odpowiadają za około 10% przypadków, przy czym ARDS powoduje niewiele ponad połowę z nich.
Astma dziecko jest mniej odpowiedzialny za niewydolnością oddechową ze względu na pojawienie się nowych LMPCh.
Utrzymany
To jest nagły przypadek medyczny . Niewydolność oddechowa wymaga opieki szpitalnej z transportem medycznym. W zależności od stanu pacjenta może nastąpić bezpośrednie przyjęcie na intensywną terapię. Pacjenta należy położyć do odpoczynku, w miarę możliwości w pozycji półsiedzącej. Przygotowywana jest infuzja dożylna.
W przypadku wdychania ciała obcego , duszności lub braku skutecznego kaszlu, należy pilnie wykonać manewr Heimlicha .
Terapia tlenowa
Ze względu na pilną potrzebę niewydolności oddechowej leczenie rozpoczyna się w fazie przedszpitalnej. Po zapewnieniu swobody górnych dróg oddechowych pierwszym zabiegiem ratunkowym jest tlenoterapia . Można to zrobić na kilka sposobów w zależności od nasilenia: okulary, maska na twarz o wysokim stężeniu, system wysokiego przepływu przez nos.
Głównym czynnikiem ograniczającym w tlenoterapii maskami wysokostężonymi jest przepływ tlenu. Jeśli może osiągnąć 15 l/min , jego skuteczność kliniczna jest jednak ograniczona przez przepływy wentylacyjne, które pacjent jest w stanie zmobilizować. W rzeczywistości, gdy szczytowe natężenie przepływu wdechowego jest większe niż natężenie przepływu dostarczanego tlenu, objętość wdychanego powietrza jest uzupełniana przez powietrze w pomieszczeniu.
Systemy do tlenoterapii donosowej o wysokim przepływie , do 60 l/min , przezwyciężają to szczególne ograniczenie, pozwalając pacjentowi wdychać tylko dostarczoną mieszaninę gazów. Uzupełniają je nawilżacz i grzałka pozwalająca na lepszą tolerancję dostarczanego gazu. Ich kaniule donosowe są również lepiej tolerowane przez pacjentów niż maski o wysokim stężeniu. Systemy te zostały po raz pierwszy zastosowane w pediatrii, ale obecnie są rozszerzone na osoby dorosłe. Zarezerwowane dla pacjentów z wystarczającą spontaniczną aktywnością oddechową, mogą zapobiec przejściu na autentyczną pomoc oddechową. Liczne błędy systematyczne badań przeprowadzonych na osobach dorosłych nie pozwalają jednak na ocenę skuteczności leczenia w porównaniu z konwencjonalną tlenoterapią.
Wspomaganie wentylacji
Wspomaganie wentylacji jest konieczne, gdy nasilenie niewydolności oddechowej zagraża życiu i obserwuje się co najmniej jeden objaw niepowodzenia. Można ją również rozpocząć na podstawie kryteriów gazometrycznych hipoksemii opornej na tlenoterapię lub kwasicy oddechowej spowodowanej hiperkapnią dodaną.
Wspomaganie wentylacji może być zapewnione na dwa sposoby: wentylacja nieinwazyjna i intubacja tchawicy. Wentylację nieinwazyjną można przeprowadzić w izbie przyjęć lub na oddziale intensywnej terapii. Wentylacja inwazyjna po intubacji wykonywana jest na oddziale intensywnej terapii.
Wentylacja nieinwazyjnaNieinwazyjne wentylacyjny (NIV) posiada wszystkie mechaniczne sposoby wentylacyjne, które nie korzystają z pierwszego wewnątrztchawicznej gdzie nasobuccal maskę doprowadza powietrze pod nadciśnieniem. Odciążając mięśnie klatki piersiowej, zapobiega wyczerpaniu oddechowemu. Dostarczane przez nią dodatnie ciśnienie wydechowe umożliwia również rekrutację pęcherzyków płucnych.
NIV jest zarezerwowana dla izolowanych niewydolności oddechowej u pacjentów współpracujących i należy ją rozpocząć wcześnie, nie czekając na początek kwasicy. Jest przeciwwskazany u pacjentów z urazami twarzy lub górnych dróg oddechowych, ciężkimi urazami mózgu oraz w przypadku niestabilności hemodynamicznej .
Główną zaletą technik NIV jest uniknięcie powikłań intubacji oraz pomoc w przywróceniu fizjologicznej mechaniki wentylacji. Wskaźnik niepowodzeń, określony potrzebą intubacji tchawicy, jest niski. Sukces leczenia NIV mierzy się zmniejszeniem częstości oddechów, wzrostem objętości wdychanego powietrza, poprawą czujności, mniejszym wykorzystaniem dodatkowych mięśni wdechowych, a w przypadku pomiaru gazu za pomocą korekcji hipoksemii i hiperkapnia.
Rozwój technik NIV od lat 90. umożliwił zatem zmniejszenie liczby intubacji. W ARDS zastosowanie NIV pozwala uniknąć około 50% intubacji. NIV jest zalecana jako leczenie pierwszego rzutu dekompensacji POChP, gdzie zmniejsza liczbę intubacji o 65% i zmniejsza śmiertelność o 46%. W ostrym obrzęku płuc NIV zmniejsza względne ryzyko śmiertelności wewnątrzszpitalnej, częstość intubacji i długość pobytu. Jest również bardzo przydatny w leczeniu tępego urazu klatki piersiowej ze znacznym zmniejszeniem śmiertelności (3% vs. 22%). W przypadku patologii nerwowo-mięśniowych często stosuje się NIV, ale brak badań z randomizacją ogranicza możliwość zaleceń. Jego zastosowanie w astmie jest kontrowersyjne i nie zaleca się stosowania go jako leczenia pierwszego rzutu w śródmiąższowych patologiach płuc ze względu na często szybkie pogorszenie stanu pacjentów. Jednak NIV pełni funkcję prewencyjną pooperacyjną po operacji supramezokolicznej jamy brzusznej, gdzie umożliwia zmniejszenie liczby intubacji. Jego profilaktyczne zastosowanie w chirurgii klatki piersiowej jest mało udowodnione.
Stosowanie lekkiej sedacji w celu poprawy tolerancji NIV, zwłaszcza u noworodków, jest delikatne ze względu na depresyjny charakter stosowanych leków. Brak potrzeby sedacji, w przeciwieństwie do intubacji, jest również uważany za jedną z zalet tej techniki. W przypadku stosowania lekkiej sedacji monitorowanie powinno być częstsze. Zidentyfikowano kilka czynników ryzyka niepowodzenia NIV: asynchronia między pacjentem a maszyną, klaustrofobia, obecność leków hamujących oddychanie i zwykle brak zespołów opieki.
Gdy wentylacja nieinwazyjna nie jest możliwa lub nie poprawia stanu pacjenta, konieczna jest intubacja tchawicy . Ponowna ocena NIV musi nastąpić wcześnie, 30 minut do 2 godzin po jej rozpoczęciu, aby nie opóźniać intubacji, która stała się konieczna.
Wentylacja inwazyjnaWentylacja inwazyjna łączy intubację tchawicy i tracheostomię , dwie techniki, których celem jest wprowadzenie mieszaniny gazów bezpośrednio do tchawicy pacjenta. Pacjent z zaburzoną czujnością lub innymi przeciwwskazaniami do NIV może odnieść korzyść z intubacji po leczeniu. Ponadto w przypadku niedrożności górnych dróg oddechowych, takiej jak zwężenie krtani lub tchawicy , wentylacja inwazyjna eliminuje barierę skutecznego wentylowania pacjenta. W szczególnym kontekście patologii śródmiąższowych, których zmiany uważa się za nieodwracalne, konieczność wentylacji inwazyjnej wiąże się z tak poważnym nasileniem choroby, że niektórzy zalecają intubację tylko tych pacjentów, którzy mogą potencjalnie odnieść korzyść z przeszczepu płuca. U tych pacjentów zaleca się unikanie w jak największym stopniu potencjalnie nieuzasadnionej wentylacji inwazyjnej.
Można stosować różne tryby wentylacji mechanicznej, w zależności od tego, czy występuje sedacja, ale także w zależności od choroby podstawowej. Dwa główne stosowane tryby to wentylacja kontrolowana i wentylacja wspomagana. W wspomaganiu wentylacji to spontaniczny wdech pacjenta wyzwala cykl urządzenia. Zazwyczaj ustala się próg częstotliwości: gdy pacjentowi zabiera dużo czasu na wdech, maszyna rozpoczyna swój cykl. Wręcz przeciwnie, w kontrolowanej wentylacji respirator dostarcza ustaloną objętość lub ciśnienie z określoną częstotliwością; wymaga to uspokojenia pacjenta w celu uniknięcia zmagań z respiratorem . W takim przypadku sedację należy okresowo przerywać w celu oceny zdolności pacjenta do samoistnej wentylacji. W przypadku niedodmy niekiedy zaleca się (przy niskim poziomie wiarygodności) manewry rekrutacji płuc, polegające na wzroście ciśnienia w dłuższym okresie czasu, a nawet traktuje się je jako środek zapobiegawczy.
Jeśli intubacja jest przedłużona, można wykonać tracheostomię. Około 12% pacjentów z niewydolnością oddechową będzie potrzebować tracheostomii. Mediana czasu, w którym tracheostomia pozostaje na miejscu, wynosi sześć dni.
Wentylacja dotchawicza pomaga chronić drogi oddechowe przed wdychaniem śliny lub płynu żołądkowego. Ułatwia również aspirację wydzieliny oskrzelowej.
Ze względu na swój inwazyjny charakter, zarówno intubacja, jak i tracheostomia mogą być źródłem powikłań, w szczególności zapalenia płuc nabytego podczas wentylacji mechanicznej . Są to najczęstsze infekcje szpitalne na oddziale intensywnej terapii.
Od 7 do 28% dzieci z zapaleniem oskrzelików wymaga intubacji. W przypadku astmy dziecięcej od 5 do 17% ciężkich ostrych ataków astmy wymaga intubacji.
Pozaustrojowe natlenianie błonowe (ECMO)
Jeżeli mimo wszystko wspomaganie wentylacji nie zapewnia prawidłowego dotlenienia i dekarboksylacji, można rozpocząć pozaustrojowe natlenianie błonowe (ECMO) w środowisku intensywnej terapii. Obwód ECMO składa się z kaniul do drenażu, a następnie ponownego wstrzykiwania krwi pacjenta, pompy i membrany umożliwiającej wymianę gazową. W niewydolności oddechowej korzystnie stosuje się tzw. żylno-żylne ECMO. Krew jest następnie odprowadzana z żyły głównej lub prawego przedsionka serca i ponownie wstrzykiwana do prawego przedsionka po natlenieniu i dekarboksylacji. Można umieścić dwie różne kaniule, ale istnieją również kaniule dwuprzepływowe, umożliwiające pobranie krwi przy wejściu do prawego przedsionka i ponowne wstrzyknięcie w pobliżu zastawki trójdzielnej . Następnie miesza się z przepływem krwi, który nie został zintegrowany z obwodem pompy.
Niektóre systemy nie pozwalają dekarboksylacji być przeprowadzona wymiana CO 2 przez membranę jest łatwiejsze niż w przypadku tlenu. Jest to szczególnie stosowane w dekompensacji POChP i ciężkiej astmie, gdzie hiperkapnia może być większa i bardziej szkodliwa niż hipoksemia. W wyjątkowych przypadkach ECMO można wykorzystać, aby umożliwić oczekiwanie na przeszczep płuc w przypadkach, gdy jest to wskazane.
U dzieci stosowanie ECMO w populacjach pediatrycznych jest przedmiotem dyskusji w niektórych wskazaniach, zwłaszcza w ARDS, gdzie nie wydaje się, aby poprawiało przeżycie. Z drugiej strony u noworodków jego stosowanie pozostaje zalecane.
Czas stosowania ECMO wynosi na ogół mniej niż 28 dni (84-88% pacjentów), a mediana czasu trwania wynosi od siedmiu do ośmiu dni. Śródmiąższowe patologie układu oddechowego na ogół wymagają dłuższej pomocy. Najczęstszą przyczyną wycofania ECMO jest powrót funkcji oddechowej u 54% pacjentów. Jednak wystąpienie powikłań może wymagać odstawienia ECMO.
Chociaż powikłania neurologiczne występują rzadziej w ECMO żylno-żylnych niż w innych formach wspomagania krążenia, nadal dotyczą 8,5% dorosłych pacjentów i do 20% noworodków. W tych powikłaniach neurologicznych dominują krwotoki śródczaszkowe (42%), udar (20%) i śmierć mózgu (23,5%). W rzeczywistości, aby zapobiec krzepnięciu krwi w obwodzie ECMO, konieczna jest antykoagulacja w dawce leczniczej. Mogą więc wystąpić zarówno powikłania zakrzepowe, jak i krwotoczne.
Przeżycie całkowite pacjentów, którzy wymagali ECMO z powodu niewydolności oddechowej, jest według badań bardzo niejednorodne. U dorosłych wynosi od 32 do 90%. U noworodków przeżywalność wynosi od 18 do 50%, a u dzieci od 22 do 66%.
Odzwyczajanie wentylacyjne
Po przejściu ostrego epizodu należy jak najszybciej przerwać wspomaganie wentylacji.
Kiedy pacjent jest zaintubowany, faza odzwyczajania pacjenta od respiratora może być złożona. Czasami można wykonać tracheostomię; zmniejszając pracę wentylacyjną, ułatwia to pacjentowi. Nie ma zaleceń dotyczących czasu zakładania tracheostomii; analizę należy przeprowadzić indywidualnie dla każdego przypadku.
Przed wycofaniem wentylacji inwazyjnej wykonuje się jeden lub więcej testów wycofania. Wspomaganie mechaniczne jest wtedy zredukowane do minimum, a spontaniczna wentylacja pacjenta jest monitorowana. Monitorowane są również pomiary gazu, stabilność hemodynamiczna i komfort pacjenta. Jeśli test odsadzenia nie powiedzie się, wspomaganie wentylacji należy wznowić na co najmniej 24 godziny.
Po pomyślnym zakończeniu próby odsadzenia należy wykonać kilka kroków przed ekstubacją. Pacjent powinien być w stanie samodzielnie skutecznie kaszleć, być dobrze wybudzonym i mieć mało wydzieliny oskrzelowej.
Po ekstubacji można wykonać wsparcie NIV. Pomaga to zmniejszyć ryzyko ponownej intubacji. Jest to szczególnie przydatne u pacjentów z czynnikami ryzyka niepowodzenia ekstubacji, takimi jak hiperkapnia, niewydolność serca i nieskuteczny kaszel, a nawet zalecane u pacjentów z POChP. Następnie NIV zostaje zatrzymana, gdy nie ma już klinicznych ani gazometrycznych objawów niewydolności oddechowej.
Możliwe jest również zastosowanie wysokoprzepływowej tlenoterapii donosowej zamiast NIV po ekstubacji, szczególnie u dzieci i wcześniaków.
Inne zabiegi
W zależności od przyczyny zaburzeń oddechowych zostaną wprowadzone inne, bardziej specyficzne terapie: antybiotykoterapia w przypadku bakteryjnego zapalenia płuc, terapia kortykosteroidami itp. Obfity wysięk opłucnowy musi zostać odprowadzony . Zator płucny wymaga antykoagulacji , a czasem fibrynolizy . Ciężka ostra astma będzie leczona lekami rozszerzającymi oskrzela . Pacjenci z urazami klatki piersiowej również odnoszą korzyści z znieczulenia zewnątrzoponowego . W dekompensacji miastenii konieczna jest plazmafereza lub leczenie immunoglobulinami. Kiedy obserwuje się niedożywienie , należy o nie zadbać w zwykły sposób.
Fizjoterapia klatki piersiowej codziennie jest ważną częścią zarządzania. U przytomnych pacjentów ułatwia drenaż oskrzeli oraz poprawia wydolność oddechową poprzez zmniejszenie niedodmy. Na bardziej ogólnym poziomie fizjoterapia umożliwia również walkę z neuropatią intensywnej terapii , utratą autonomii oraz powikłaniami odleżyn, takimi jak odleżyny .
Stanie i podnoszenie na krześle (lub przynajmniej podnoszenie wezgłowia łóżka u pacjentów poddawanych wentylacji inwazyjnej) są powszechnie praktykowane.
Monitorowanie i kontynuacja
Od lat 80. pulsoksymetria umożliwia nieinwazyjne monitorowanie saturacji krwi obwodowej. Jednak jego niezawodność jest osłabiona w przypadku słabej perfuzji tkanek (np. w stanie wstrząsu krążeniowego), stosowania zabiegów zwężających naczynia krwionośne, takich jak noradrenalina , a nawet hipotermii . Decyzje terapeutyczne dotyczące wspomagania wentylacji muszą zatem być podejmowane w przypadku bezpośredniego pomiaru PaO 2 , pH i PaCO 2 poprzez wykonanie pomiaru gazu tętniczego, który pozostaje badaniem referencyjnym. Chociaż do oszacowania tych wartości można użyć krwi włośniczkowej, próbki krwi z żył obwodowych nie nadają się do tych pomiarów.
Stosunek P / F jest obliczany poprzez podzielenie PaO 2 przez ułamek tlenu we wdychanym powietrzu. Pozwala śledzić ewolucję zmian w obrzękach płuc, w szczególności ARDS .
W przypadku wspomagania wentylacji, w szczególności intubacji, możliwe jest pośrednie monitorowanie kapnii za pomocą kapnografii . Jest to analiza wydychanych gazów, umożliwiająca ilościowe określenie wydychanego CO 2 .
Codzienna kontrola RTG klatki piersiowej jest przedmiotem dyskusji u pacjentki pod wentylacją mechaniczną, ze względu na słabą jakość zdjęć wykonywanych w pozycji leżącej. Konieczne jest jednak wykonanie zdjęcia RTG po założeniu sondy intubacyjnej lub cewnika do żyły centralnej w celu weryfikacji jego położenia, a podczas obserwacji zachowuje on wartość oczyszczenia.
Rokowanie
Śmiertelność
Rokowanie w przypadku ostrej niewydolności oddechowej jest bardzo zależne od przyczyny, a także początkowego nasilenia.
Całkowita śmiertelność dorosłych z niewydolnością oddechową wynosi 31%. Ogólne czynniki złego rokowania to obecność istotnych chorób współistniejących i niedożywienie. W śródmiąższowych patologiach płuc rokowanie jest bardzo złe, z całkowitą śmiertelnością wewnątrzszpitalną wynoszącą 50%, która może sięgać 96%, a przewidywana długość życia rzadko przekracza sześć miesięcy. Spośród pacjentów, którym udaje się opuścić szpital, 42% umiera w ciągu roku. Śmiertelność dorosłych z ARDS wynosi 35-45%.
U dzieci ogólna śmiertelność jest bardzo zmienna w zależności od serii i waha się od 24 do 34%. W 2012 roku infekcje płuc odpowiadały za 2% śmiertelności wśród dzieci poniżej piątego roku życia w Stanach Zjednoczonych, w porównaniu do 18% na całym świecie. Ogólna śmiertelność dzieci, u których wystąpił obrzęk płuc, jest jednak wyższa, zbliżona do śmiertelności dorosłych (27%). Czynnikami złego rokowania są skrajny wiek życia i występowanie chorób współistniejących, w szczególności przewlekłych chorób układu oddechowego i immunosupresji. Na przykład śmiertelność może osiągnąć 90% u młodych pacjentów z białaczką.
W populacji pediatrycznej całkowite przeżycie pacjentów wymagających ECMO wynosi 57%, z dużymi różnicami w zależności od przyczyny niewydolności oddechowej: pacjenci z krztuścem przeżywają tylko w 39% przypadków, w porównaniu z 83% pacjentów astmatycy.
Następstwa
Pacjenci, dorośli lub dzieci, którzy doświadczyli epizodu niewydolności oddechowej, są bardziej narażeni na rozwój przewlekłej choroby płuc, zarówno obturacyjnej (takiej jak astma , POChP , rozedma płuc ), jak i restrykcyjnej .
Powrót do funkcji płuc przebiega powoli, do roku po wypisaniu ze szpitala. Obserwowane początkowo uszkodzenie może składać się z zespołu obturacyjnego, restrykcyjnego lub mieszanego, z lub bez zmniejszenia dyfuzji pęcherzykowo-włośniczkowej. Najczęściej jest umiarkowana i niewielu pacjentów skarży się na duszność.
Odżywczo pacjenci stracili średnio 18% masy ciała po wypisaniu z oddziału ciągłego monitorowania , ale 71% odzyskało zdrową wagę w ciągu jednego roku. Jeśli jakość życia pogorszy się po wypisie z hospitalizacji, ma tendencję do poprawy w następnym roku. Pięć lat po ARDS dorośli pacjenci mają nieprawidłową czynność płuc. Jednak nadal stanowią one ograniczenie ćwiczeń i pogorszenie jakości życia.
U dzieci brakuje danych na temat długoterminowych następstw poznawczych.
Bibliografia
- Klaus Lewandowski , „ Wkład w epidemiologię ostrej niewydolności oddechowej ”, Critical Care , tom. 7, n O 4,2003, s. 288-290 ( ISSN 1364-8535 , PMID 12930552 , przeczytany online , dostęp 27 grudnia 2019 ).
- (en) Grupa badawcza FINNALI , Rita Linko , Marjatta Okkonen i Ville Pettilä , „ Ostra niewydolność oddechowa na oddziałach intensywnej terapii. FINNALI: prospektywne badanie kohortowe ” , Medycyna Intensywnej Terapii , tom. 35 N O 8,sierpień 2009, s. 1352–1361 ( ISSN 0342-4642 i 1432-1238 , DOI 10.1007 / s00134-009-1519-z , przeczytane online , dostęp 20 stycznia 2020 r. ).
- (en) Jean-Louis Vincent Serdar Akça Arnaldo de Mendonça i Philip Haji-Michael , „ Epidemiologia niewydolności Acute Respiratory u krytycznie chorych pacjentów ” , Chest , vol. 121 n O 5,maj 2002, s. 1602-1609 ( DOI 10.1378 / chest.121.5.1602 , przeczytaj online , dostęp 19 grudnia 2019 ).
- Schneider et al 2012 ..
- (en) Poongundran Namachivayam , Frank Shann , Lara Shekerdemian i Anna Taylor , „ Trzy dekady pediatrycznej intensywnej opieki: kto został przyjęty, co wydarzyło się na oddziale intensywnej terapii i co wydarzyło się później *: ” , Pediatric Critical Care Medicine , lot. 11 N O 5,wrzesień 2010, s. 549-555 ( ISSN 1529-7535 , DOI 10.1097 / PCC.0b013e3181ce7427 , czytanie online , dostęp 13 stycznia 2020 ).
- College pulmonologii Nauczycielami " dorosłych oddechowych " (dostęp 9 lutego, 2020 ) .
- Roussos wsp 2003 ..
- Michael E. Hanley i Roger C. kości „ ostrej niewydolności oddechowej ”, Postgraduate Medicine , tom. 79, n o 1,1 st styczeń 1986, s. 166-176 ( ISSN 0032-5481 , DOI 10.1080 / 00325481.1986.11699244 , przeczytane online , dostęp 14 stycznia 2020 ).
- Friedman et al 2018 .
- Rajnish K. Gupta i David A. Ewards, „ Monitoring Respiratory Depression Due To Opiates ”, w Anesthesia Patient Safety Foundation ,czerwiec 2018(dostęp 7 stycznia 2020 r . ) .
- Markou wsp 2004 .
- (w) Bishwajit Bhattacharya i Kimberly Davis , „Assessment and Management of Acute Respiratory Distress in the ICU” w Surgical Critical Care Therapy , Springer International Publishing,2018( ISBN 978-3-319-71711-1 , DOI 10.1007 / 978-3-319-71712-8_15 , czytaj online ) , s. 161-169.
- (en) Jean-Yves Fagon , „ Ostra niewydolność oddechowa u osób starszych ” , Critical Care , tom. 10 N O 4,2006, s. 151 ( PMID 16887005 , PMCID PMC1751014 , DOI 10.1186/cc4982 , odczyt online , dostęp 27 grudnia 2019 r. ).
- (w) Hiroshi Sekiguchi , Louis A. Schenck , Ryohei Horie i Jun Suzuki , „ Ultrasonografia w intensywnej terapii różnicuje ARDS, obrzęk płuc i inne przyczyny we wczesnym stadium hipoksemii ostrej niewydolności oddechowej ” , Chest , tom. 148 n O 4,październik 2015, s. 912-918 ( DOI 10.1378 / chest.15-0341 , przeczytaj online , dostęp 14 stycznia 2020 ).
- (i) Jonathan Dakin Mark Griffiths , „ Lekarz płucnej intensywnej opieki 1: płuc badań ostrej niewydolności oddechowej ” , Thorax , obj. 57, n o 1,1 st styczeń 2002, s. 79-85 ( PMID 11809996 , PMCID PMC1746170 , DOI 10.1136 / thorax.57.1.79 , czytanie online , dostęp 20 stycznia 2020 ).
- (en) David Schnell , Julien Mayaux , Jérôme Lambert i Antoine Roux , „ Ocena kliniczna w celu identyfikacji przyczyn ostrej niewydolności oddechowej u pacjentów z rakiem ” , European Respiratory Journal , tom. 42 N O 2Sierpień 2013, s. 435-443 ( ISSN 0903-1936 i 1399-3003 , DOI 10.1183 / 09031936.00122512 , przeczytane online , dostęp 14 stycznia 2020 r. ).
- (en) Paola Faverio Federica De Giacomi Luca Sardella Giuseppe Fiorentino , „ zarządzanie ostrej niewydolności oddechowej śródmiąższowych chorób płuc: Przegląd klinicznych i spostrzeżeń ” , BMC płuc Medicine , tom. 18, n o 1,grudzień 2018, s. 70 ( ISSN 1471-2466 , PMID 29764401 , PMCID PMC5952859 , DOI 10.1186 / s12890-018-0643-3 , odczyt online , dostęp 16 stycznia 2020 r. ).
- (w) Albert Dahan , Leon Aarts i Terry W. Smith , „ Wpływ, odwrócenie i zapobieganie depresji oddechowej wywołanej przez opioidy: ” , Anestezjologia , tom. 112 n o 1,styczeń 2010, s. 226–238 ( ISSN 0003-3022 , DOI 10.1097 / ALN.0b013e3181c38c25 , przeczytane online , dostęp 7 stycznia 2020 r. ).
- (w) KL Hartshorn , EC Crouch , R. White i P Eggleton , „ Dowody na ochronną rolę surfaktantu płucnego białka D (SP-D) w stosunku do wirusów grypy typu A. ” , Journal of Clinical Investigation , tom. 94, n o 1,1 st lipca 1994, s. 311-319 ( ISSN 0021-9738 , PMID 8040272 , PMCID PMC296311 , DOI 10.1172 / JCI117323 , odczyt online , dostęp 14 maja 2020 r. )
- (w) Heber C. Nielsena , pana Howarda Zinmanem i John S. Torday , " dihydrotestosteron hamuje Rabbit Fetal płuc powierzchniowo czynnego Production " , Journal of Clinical Investigation , Vol. 69, n o 3,1 st marca 1982, s. 611-616 ( ISSN 0021-9738 , PMID 6916770 , PMCID PMC371018 , DOI 10.1172/JCI110488 , odczyt online , dostęp 14 maja 2020 r. )
- (w) Kuiama Lewandowski , Jutta Metz , Christel Deutschmann , Heinrich Preiss , Ralf Kuhlen , Antonio Artigas i Konrad J. Falke , „ Zapadalność, nasilenie i śmiertelność ostrej niewydolności oddechowej w Berlinie, Niemcy. ” , American Journal of Respiratory and Critical Care Medicine , tom. 151 n O 4,Kwiecień 1995, s. 1121–1125 ( ISSN 1073-449X i 1535-4970 , DOI 10.1164 / ajrccm.151.4.7697241 , przeczytane online , dostęp 20 stycznia 2020 ).
- (w) Owe R. Luhr , Kristian Antonsen , Magnus Karlsson i Sidsel Aardal , „ Zapadalność i śmiertelność po ostrej niewydolności oddechowej i zespół ostrej niewydolności oddechowej w Szwecji, Danii i Islandii ” , American Journal of Respiratory and Critical Care Medicine , lot . 159 N O 6,Czerwiec 1999, s. 1849-1861 ( ISSN 1073-449X i 1535-4970 , DOI 10.1164 / ajrccm.159.6.9808136 , przeczytane online , dostęp 20 stycznia 2020 ).
- (w) Suelene Aires Franca Carlos Toufen André Luiz D. Hovnanian i André Luís P. Albuquerque , „ Epidemiologia ostrej niewydolności oddechowej u hospitalizowanych pacjentów: brazylijskie prospektywne badanie kohortowe ” , Journal of Critical Care , tom. 26 N O 3,czerwiec 2011, s. 330.e1-330.e8 ( DOI 10.1016 / j.jcrc.2010.10.010 , przeczytany online , dostęp 20 stycznia 2020 ).
- (w) Simon V. Baldwin , „ Lekarz pulmonologiczny w oddziale intensywnej opieki medycznej 3: Zarządzanie w stanach krytycznych pozaszpitalnego zapalenia płuc ” , Thorax , tom. 57, n o 3,1 st marca 2002, s. 267-271 ( PMID 11867834 , PMCID PMC1746268 , DOI 10.1136 / thorax.57.3.267 , przeczytane online , dostęp 20 stycznia 2020 ).
- (i) Bruno L. Ferreyro i Laveena Munshi , „ przyczyny ostrej niewydolności oddechowej w gospodarz o upośledzonej odporności: ” , Current Opinion in Critical Care , tom. 25, n o 1,luty 2019, s. 21-28 ( ISSN 1070-5295 , DOI 10.1097/MCC.0000000000000569 , czytanie online , dostęp 14 stycznia 2020 ).
- (en) Jean-Louis Vincent , Yasser Sakr i Marco Ranieri , „ Epidemiologia i skutki ostrej niewydolności oddechowej u pacjentów oddziałów intensywnej terapii: ” , Critical Care Medicine , tom. 31, n o Dodatkukwiecień 2003, S296 – S299 ( ISSN 0090-3493 , DOI 10.1097/01.CCM.0000057906.89552.8F , odczyt online , dostęp 20 stycznia 2020 ).
- .
- (w) Jeevarathi Gnanaratnem i Neil N. Finer , " Ostra niewydolność oddechowa u noworodków: " , Current Opinion in Pediatrics , tom. 12 N O 3,Czerwiec 2000, s. 227-232 ( ISSN 1040-8703 , DOI 10.1097/00008480-200006000-00009 , przeczytaj online , dostęp 4 lutego 2020 r. ).
- (w) Heber C. Nielsen , pan Howard Zinman i John S. Torday , „ Dihydrotestosteron hamuje produkcję płucnego środka powierzchniowo czynnego płodu królika ” , Journal of Clinical Investigation , tom. 69, n o 3,1 st marca 1982, s. 611-616 ( ISSN 0021-9738 , PMID 6916770 , PMCID PMC371018 , DOI 10.1172/JCI110488 , odczyt online , dostęp 14 maja 2020 r. )
- (en) Reese H. Clark , „ Epidemiologia niewydolności oddechowej u noworodków urodzonych o przybliżony wiek ciążowy 34 tygodni lub więcej ” , Journal of Perinatologii , vol. 25 N O 4,kwiecień 2005, s. 251–257 ( ISSN 1476-5543 , DOI 10.1038 / sj.jp.7211242 , czytanie online , dostęp 5 lutego 2020 ).
- (en) Peter G. Dahlem , Willem MC van Aalderen , Marije E. Hamaker , Marcel GW Dijkgraaf i Albert P. Bos , " Przypadki i krótkoterminowe skutki ostrego uszkodzenia płuc u dzieci wentylowanych mechanicznie " , Europejski Dziennik oddechowy , obj. 22 N O 6,1 st grudzień 2003, s. 980-985 ( ISSN 0903-1936 i 1399-3003 , DOI 10.1183 / 09031936.03.00003303 , przeczytane online , dostęp 13 stycznia 2020 r. ).
- (en) JR Masclans , P. Pérez-Terán i O. Roca , „ Rola wysokoprzepływowej terapii tlenowej w ostrej niewydolności oddechowej ” , Medicina Intensiva (wydanie angielskie) , tom. 39 N O 8,listopad 2015, s. 505-515 ( DOI 10.1016 / j.medine.2015.05.004 , czytaj online , dostęp 26 grudnia 2019 ).
- (en) Jeffrey J. Ward , „ wysoka przepływ tlenu Podawanie przez kaniulę do nosa dla dorosłych i perinatalnej Pacjentów ” , Pielęgnacja oddechowy , vol. 58, n o 1,1 st styczeń 2013, s. 98-122 ( ISSN 0020-1324 i 1943-3654 , DOI 10.4187 / respcare.01941 , czytanie online , dostęp 26 grudnia 2019 ).
- (en) Dominic Wilkinson , Czad Andersen , Colm PF O'Donnell i Antonio G De Paoli , „ High Flow kaniuli nosowej do wspomagania oddychania u wcześniaków ” , Cochrane Database of Systematic Reviews ,22 lutego 2016( DOI 10.1002/14651858.CD006405.pub3 , przeczytane online , dostęp 26 grudnia 2019 r. ).
- (w) Pan Nishimura , „ Tlenowa terapia kaniulami nosowymi o wysokim przepływie u dorosłych: korzyści fizjologiczne, wskazania, korzyści kliniczne i działania niepożądane ” , Opieka oddechowa , tom. 61, n o 4,1 st kwiecień 2016, s. 529-541 ( ISSN 0020-1324 i 1943-3654 , DOI 10.4187 / respcare.04577 , przeczytane online , dostęp 26 grudnia 2019 ).
- (w) Amanda Corley , Claire M Rickard , Leanne M Aitken i Amy Johnston , „ Kaniule nosowe o wysokim przepływie do mediów oddechowych u dorosłych pacjentów intensywnej terapii ” , Cochrane Database of Systematic Reviews ,30 maja 2017 r.( PMID 28555461 , PMCID PMC6481761 , DOI 10.1002/14651858.CD010172.pub2 , przeczytane online , dostęp 26 grudnia 2019 r. ).
- (en) Christian R Osadnik , Vanessa S Tee , Kristin V Carson-Chahhoud i Joanna Picot , „ Nieinwazyjna wentylacja w leczeniu ostrej hiperkapnicznej niewydolności oddechowej spowodowanej zaostrzeniem przewlekłej obturacyjnej choroby płuc ” , Cochrane Baza Przeglądów Systematycznych ,13 lipca 2017 r.( PMID 28702957 , PMCID PMC6483555 , DOI 10.1002/14651858.CD004104.pub4 , przeczytane online , dostęp 26 grudnia 2019 r. ).
- (en) " Międzynarodowe konferencje konsensusu w Intensive Care Medicine: Nieinwazyjna wentylacja dodatnim ciśnieniem w ostrej niewydolności oddechowej: organizowane wspólnie przez American Thoracic Society, European Respiratory Society, European Society of Intensive Care Medicine oraz Société de Réanimation de Langue Française i zatwierdzony przez Radę Dyrektorów ATS, grudzień 2000 ” , American Journal of Respiratory and Critical Care Medicine , tom. 163 n o 1,styczeń 2001, s. 283–291 ( ISSN 1073-449X i 1535-4970 , DOI 10.1164 / ajrccm.163.1.ats1000 , przeczytane online , dostęp 27 grudnia 2019 r. ).
- Giuseppe Bello , Paolo De Santis i Massimo Antonelli , „ Nieinwazyjna wentylacja w kardiogennym obrzęku płuc ”, Annals of Translational Medicine , tom. 6, n O 18wrzesień 2018, s. 355–355 ( PMID 30370282 , PMCID PMC6186545 , DOI 10.21037 / atm.2018.04.39 , czytaj online , dostęp 26 grudnia 2019 ).
- (w) Dean R. Hess , „ Wentylacja nieinwazyjna w przypadku ostrej niewydolności oddechowej ” , Opieka oddechowa , tom. 58, n o 6,1 st czerwiec 2013, s. 950-972 ( ISSN 0020-1324 i 1943-3654 , DOI 10.4187 / respcare.02319 , przeczytane online , dostęp 26 grudnia 2019 ).
- Barbas et al 2013 .
- (w) Aylin Ozsancak Ugurlu i Mehmet Ali Habesoglu , „ Epidemiologia VIN w ostrej niewydolności oddechowej u pacjentów z POChP: Wyniki badań międzynarodowych w porównaniu z „Real World” ” , POChP: Journal of Chronic Obstructive Pulmonary Disease , tom. 14 N O 4,4 lipca 2017 r., s. 429-438 ( ISSN 1541-2555 i 1541-2563 , DOI 10.1080 / 15412555.2017.1336527 , przeczytane online , dostęp 7 stycznia 2020 r. ).
- (en) Josep Masip i Arantxa Mas , „ Wentylacja nieinwazyjna w ostrej niewydolności oddechowej ” , International Journal of Chronic Obstructive Pulmonary Disease ,sierpień 2014, s. 837 ( ISSN 1178-2005 , PMID 25143721 , PMCID PMC4136955 , DOI 10.2147 / COPD.S42664 , odczyt online , dostęp 26 grudnia 2019 r. ).
- Davidson et al 2016 .
- Rochwerg i in . 2017 .
- (w) Nicolas Berbenetz , Yongjun Wang , James Brown i Charlotte Godfrey , „ Wentylacja dodatnim ciśnieniem Nieinwazyjna (CPAP lub dwupoziomowa NPPV) w kardiogennym obrzęku płuc ” , Cochrane Database of Systematic Reviews ,5 kwietnia 2019( PMID 30950507 , PMCID PMC6449889 , DOI 10.1002/14651858.CD005351.pub4 , przeczytane online , dostęp 26 grudnia 2019 r. ).
- (w) Fang Luo , Djillali Annane David Orlikowski i Li He , „ Wentylacja inwazyjna kontra nieinwazyjna w ostrej niewydolności oddechowej w chorobach nerwowo-mięśniowych i zaburzeniach ściany klatki piersiowej ” , Cochrane Database of Systematic Reviews ,4 grudnia 2017 r.( PMID 29199768 , PMCID PMC6486162 , DOI 10.1002/14651858.CD008380.pub2 , odczyt online , dostęp 26 grudnia 2019 r. ).
- (w) Wei Jie Lim , Redhuan Mohammed Akram , Kristin V Carson i Satya Mysore , „ Nieinwazyjna wentylacja dodatnim ciśnieniem w leczeniu niewydolności oddechowej spowodowanej ciężkimi ostrymi zaostrzeniami astmy ” , Baza danych przeglądów systematycznych Cochrane ,12 grudnia 2012( DOI 10.1002 / 14651858.CD004360.pub4 , przeczytany online , dostęp 26 grudnia 2019 r. ).
- (w) Ganesh Raghu , Bram Rochwerg , Yuan Zhang i Carlos Cuello A. Garcia , „ Oficjalne wytyczne praktyki klinicznej ATS/ERS/JRS/ALT: Leczenie idiopatycznego zwłóknienia płuc”. Aktualizacja wytycznych praktyki klinicznej 2011 ” , American Journal of Respiratory and Critical Care Medicine , tom. 192 n O 215 lipca 2015, e3 – e19 ( ISSN 1073-449X i 1535-4970 , DOI 10.1164 / rccm.201506-1063ST , odczyt online , dostęp 16 stycznia 2020 ).
- (w) Debora AS Faria , Edina MK da Silva Álvaro N Atallah i Flávia MR Vital , " dodatnie ciśnienie Nieinwazyjna wentylacja ostrej niewydolności oddechowej po operacji górnej części brzucha " , Baza danych przeglądów systematycznych Cochrane ,5 października 2015 r.( DOI 10.1002 / 14651858.CD009134.pub2 , przeczytane online , dostęp 26 grudnia 2019 r. ).
- (w) Maria FS Torres , Gustavo JM Porfirio Alan PV Carvalho i Rachel Riera , „ Nieinwazyjna wentylacja dodatnim ciśnieniem w celu zapobiegania powikłaniom po resekcji płucnej u pacjentów z rakiem płuc ” , Baza danych przeglądów systematycznych Cochrane ,6 marca 2019( PMID 30840317 , PMCID PMC6402531 , DOI 10.1002/14651858.CD010355.pub3 , przeczytane online , dostęp 26 grudnia 2019 r. ).
- (w) Roberto Bellù , Koert A de Waal i Rinaldo Zanini , " Opioidy dla noworodków otrzymujących wentylację mechaniczną " , Cochrane Database of Systematic Reviews ,23 stycznia 2008( DOI 10.1002 / 14651858.CD004212.pub3 , przeczytany online , dostęp 26 grudnia 2019 r. ).
- (w) Fahad M Al-hameed i Sat Sharma , „ Wyniki pacjentów przyjętych na oddział intensywnej terapii z powodu ostrego zaostrzenia idiopatycznego zwłóknienia płuc ” , Canadian Respiratory Journal , tom. 11 N O 22004, s. 117-122 ( ISSN 1198-2241 , DOI 10.1155 / 2004/379723 , czytaj online , dostęp 16 stycznia 2020 ).
- (w) John P. Kress , Anne S. Pohlman , Michael F. O'Connor i Jesse B. Hall , „ Codzienne przerywanie wlewów uspokajających u krytycznie chorych pacjentów przechodzących wentylację mechaniczną ” , New England Journal of Medicine , tom. 342 n O 20,18 maja 2000 r., s. 1471–1477 ( ISSN 0028-4793 i 1533-4406 , DOI 10.1056/ NEJM200005183422002 , przeczytane online , dostęp 16 stycznia 2020 ).
- Alhazzani, W. Moller, MH Arabi, M. Loeb i in. , Kampania Surviving sepsis: wytyczne dotyczące postępowania z osobami dorosłymi w stanie krytycznym z chorobą koronawirusową 2019 (COVID-19) – nieedytowany zaakceptowany dowód , European Society of Intensive Care Medicine and the Society of Critical Care Medicine,2020( DOI 10.1007/s00134-020-06022-5 , przeczytaj online )
- Thomas Godet, Audrey Johanny i Emmanuel Futier, „ Kiedy i jak wykonać manewr rekrutacyjny wyrostka zębodołowego na sali operacyjnej? » , MAPAR ,2016
- (w) Nora H. Cheung i Lena M. Napolitano , „ Tracheostomia: epidemiologia, wskazania, czas, technika i wyniki ” , Opieka oddechowa , tom. 59, n o 6,1 st czerwiec 2014, s. 895-919 ( ISSN 0020-1324 i 1943-3654 , DOI 10.4187 / respcare.02971 , czytaj online , dostęp 27 grudnia 2019 ).
- JL Trouillet, „ Pneumopatie nabyte przy wentylacji mechanicznej ” , o Francuskim Towarzystwie Anestezjologii-Resuscytacji ,3 marca 2009(dostęp 16 stycznia 2020 r . ) .
- P. Seguin i K. Hervé, „ Profilaktyka zapalenia płuc nabytego podczas wentylacji mechanicznej ” , na sofia.medicalistes.fr ,2012.
- .
- .
- (w) Viviane G. Nasra Lakshmi Ramana , Ryan P. Barbaro i Yigit Güner , " Najważniejsze z pozaustrojowym Resuscytacyjnych Organizacji rejestru: 2006-2017 " , ASAIO Journal , tom. 65, n o 6,sierpień 2019, s. 537-544 ( ISSN 1058-2916 , DOI 10.1097 / MAT.0000000000000863 , odczyt online , dostęp 14 stycznia 2020 r. ).
- Simon Erickson „ pozaustrojowej membrana utleniające w pediatrycznych zespół ostrej niewydolności dróg oddechowych: przecenione lub w pełni wykorzystany? ”, Roczniki Medycyny Translacyjnej , tom. 7, n O 19,październik 2019, s. 512-512 ( PMID 31728365 , PMCID PMC6828785 , DOI 10.21037 / atm.2019.09.27 , odczyt online , dostęp 14 stycznia 2020 ).
- (w) Ryan P. Barbaro , Yuejia Xu , Santiago Borasino i Edward J. Truemper , „ Czy pozaustrojowe natlenianie błon poprawia przeżywalność w przypadku ostrej niewydolności oddechowej u dzieci? ” , American Journal of Respiratory and Critical Care Medicine , tom. 197 N O 9,maj 2018, s. 1177-1186 ( ISSN 1073-449X i 1535-4970 , PMID 29373797 , PMCID PMC6019927 , DOI 10.1164 / rccm.201709-1893OC , odczyt online , dostęp 14 stycznia 2020 ).
- (en) Soo Jin Na , Jae-Seung Jung , Sang-Bum Hong i Woo Hyun Cho , „ Wyniki kliniczne pacjentów otrzymujących przedłużone pozaustrojowe natlenianie błonowe w celu wspomagania oddychania ” , Therapeutic Advances in Respiratory Disease , tom. 13,styczeń 2019, s. 175346661984894 ( ISSN 1753-4666 i 1753-4666 , PMID 31090503 , PMCID PMC6535699 , DOI 10.1177 / 1753466619848941 , odczyt online , dostęp 14 stycznia 2020 r. ).
- (w) Matthew L. Paden , Steven A. Conrad , Peter T. Rycus i Ravi R. Thiagarajan , „ Raport Rejestru Organizacji Pozaustrojowych Podtrzymywania Życia 2012: ” , ASAIO Journal , tom. 59, n o 3,2013, s. 202–210 ( ISSN 1058-2916 , DOI 10.1097 / MAT.0b013e3182904a52 , przeczytane online , dostęp 14 stycznia 2020 ).
- (w) Nikkole Pan Haines , Peter T. Rycus , Joseph B. Zwischenberger i Robert H. Bartlett , „ Raport Rejestru Pozaustrojowych Podtrzymywania Życia 2008: Przypadki Kardiologiczne Noworodków i Dzieci: ” , ASAIO Journal , tom. 55, n o 1,styczeń 2009, s. 111–116 ( ISSN 1058-2916 , DOI 10.1097 / MAT.0b013e318190b6f7 , przeczytane online , dostęp 14 stycznia 2020 ).
- (w) Roberto Lorusso Fabio Barili , Michele Di Mauro i Sandro Gelsomino , „ Szpitalne komplikacje neurologiczne u dorosłych pacjentów poddawanych pozaustrojowemu natlenianiu błon żylno-tętniczych: wyniki z pozaustrojowego rejestru organizacji podtrzymywania życia ” , Critical Care Medicine , tom. 44 N O 10,październik 2016, e964 – e972 ( ISSN 0090-3493 , DOI 10.1097 / CCM.0000000000001865 , odczyt online , dostęp 14 stycznia 2020 ).
- (w) Yue-Nan Ni Jian Luo , He Yu i Dan Liu , „ Czy kaniula nosowa o wysokim przepływie może zmniejszyć szybkość reintubacji u dorosłych pacjentów po ekstubacji? Metaanaliza ” , BMC Pulmonary Medicine , tom. 17, n o 1,grudzień 2017, s. 142 ( ISSN 1471-2466 , PMID 29149868 , PMCID PMC5693546 , DOI 10.1186 / s12890-017-0491-6 , odczyt online , dostęp 26 grudnia 2019 r. ).
- (w) William D Schweickert , Mark C. Pohlman , Anne S Pohlman i Celerina Nigos , „ Wczesna terapia fizyczna i zajęciowa u wentylowanych mechanicznie, krytycznie chorych pacjentów: randomizowana, kontrolowana próba ” , The Lancet , tom. 373 n O 9678,maj 2009, s. 1874-1882 ( DOI 10.1016 / S0140-6736 (09) 60658-9 , przeczytane online , dostęp 13 stycznia 2020 ).
- (i) Gerald S. Zavorsky , Jiguo Cao , Nancy E. Mayo i Rina Gabbay , „ tętnicy w porównaniu kapilarnych gazometrii: a meta-analysis ” , dróg oddechowych i Neurobiology Physiology , Vol. 155 n O 3,Marzec 2007, s. 268-279 ( DOI 10.1016 / j.resp.2006.07.002 , przeczytane online , dostęp 7 stycznia 2020 ).
- (en) Michael W. Quasney , Yolanda M. López-Fernández , Miriam Santschi i R. Scott Watson , „ Wyniki dzieci z pediatrycznym zespołem ostrej niewydolności oddechowej: postępowanie z pediatrycznego ostrego urazu płuc Konferencja konsensusu ” , Medycyna krytycznej opieki pediatrycznej , tom. 16,czerwiec 2015, S118 – S131 ( ISSN 1529-7535 , DOI 10.1097/PCC.0000000000000438 , odczyt online , dostęp 13 stycznia 2020 ).
- (w) Maki Kobayashi Yoko Shibata , Sumitomo Inoue i Akira Igarashi , „ Predyktory śmiertelności z powodu niewydolności oddechowej w populacji ogólnej ” , Raporty Naukowe , tom. 6,16 maja 2016( ISSN 2045-2322 , PMID 27180927 , PMCID 4867438 , DOI 10.1038 / srep26053 , odczyt online , dostęp 21 stycznia 2020 r. ).
- (w) Whitney D. Gannon David J. Lederer , Mauer Biscotti i Azka Javaid , " Rezultaty i śmiertelność przewidywania modelu krytycznie chorych dorosłych z zaburzeniami ostrej niewydolności oddechowej i śródmiąższowego Lung Disease " , Chest , Tom. 153 N O 6,czerwiec 2018, s. 1387–1395 ( PMID 29353024 , PMCID PMC6026289 , DOI 10.1016 / j.chest.2018.01.006 , czytanie online , dostęp 16 stycznia 2020 ).
- (w) Demostenes Bouros , Andrew G. Nicholson , Vlasis Polychronopoulos i Roland M. du Bois , „ Ostre śródmiąższowe zapalenie płuc ” , European Respiratory Journal , tom. 15 N O 2luty 2000, s. 412 ( DOI 10.1034 / j.1399-3003.2000.15b31.x , przeczytany online , dostęp 16 stycznia 2020 ).
- (w) Jason Phua , Joan R. Badia , Neill KJ Adhikari i Jan O. Friedrich , „ Czy śmiertelność z powodu zespołu ostrej niewydolności oddechowej zmniejszyła się z czasem?: przegląd systematyczny ” , American Journal of Respiratory and Critical Care Medicine , tom. 179 n O 3,Luty 2009, s. 220-227 ( ISSN 1073-449X i 1535-4970 , DOI 10.1164 / rccm.200805-722OC , odczyt online , dostęp 13 stycznia 2020 ).
- (en) Margaret S. Herridge , Angela M. Cheung , Catherine M. Tansey i Andrea Matte-Martyn , „ Roczne wyniki u osób przeżyły zespół ostrej niewydolności oddechowej ” , New England Journal of Medicine , lot. 348 N O 8,20 lutego 2003 r., s. 683-693 ( ISSN 0028-4793 i 1533-4406 , DOI 10.1056 / NEJMoa022450 , czytanie online , dostęp 13 stycznia 2020 ).
- .
- (w) Margaret S. Herridge Catherine M. Tansey Andrea matowy i George Tomlinson , " Functional niepełnosprawności po 5 latach zespół ostrej niewydolności oddechowej " , The New England Journal of Medicine , tom. 364 n O 147 kwietnia 2011, s. 1293–1304 ( ISSN 0028-4793 i 1533-4406 , DOI 10.1056/ NEJMoa1011802 , przeczytane online , dostęp 14 stycznia 2020 ).
Zobacz również
Bibliografia
Patofizjologia- (en) Charis Roussos i Antonia Koutsoukou , „ Niewydolność oddechowa ” , European Respiratory Journal , tom. 22, n o suplement 47,16 listopada 2003 r., s. 3s – 14s ( ISSN 0903-1936 i 1399-3003 , DOI 10.1183 / 09031936.03.0038503 , przeczytane online , dostęp 26 grudnia 2019 ).
- (en) Nicolaos K. Markou , Pavlos M. Myrianthefs i George J. Baltopoulos , „ Niewydolność oddechowa: przegląd ” , Kwartalnik Pielęgniarstwa Krytycznego , tom. 27 N O 4,październik 2004, s. 353-379 ( ISSN 0887-9303 , DOI 10.1097/ 00002727-20410000-00006 , przeczytane online , dostęp 16 stycznia 2020 ).
- (w) James Schneider i Todd Sweberg , „ Ostra niewydolność oddechowa ” , Critical Care Clinics , tom. 29 N O 2kwiecień 2013, s. 167–183 ( DOI 10.1016 / j.ccc.2012.12.004 , przeczytany online , dostęp 7 stycznia 2020 ).
- (w) Matthew L. Friedman i Mara E. Nitu , " Ostra niewydolność oddechowa u dzieci " , Roczniki Pediatryczne , tom. 47, n o 7,1 st lipca 2018, e268 – e273 ( ISSN 1938-2359 , DOI 10.3928 / 19382359-20180625-01 , odczyt online , dostęp 26 grudnia 2019 ).
- (en) Carmen Sílvia Valente Barbas , Alexandre Marini Ísola , Augusto Manoel de Carvalho Farias i Alexandre Biasi Cavalcanti , „ Brazylijskie zalecenia dotyczące wentylacji mechanicznej 2013. Część 2 ” , Revista Brasileira de Terapia Intensiva , tom. 26 N O 3,2014( ISSN 0103-507X , PMID 25295817 , PMCID PMC4188459 , DOI 10.5935 / 0103-507X.20140034 , odczyt online , dostęp 16 stycznia 2020 r. ).
- (en) Bram Rochwerg , Laurent Brochard , Mark W. Elliott i Dean Hess , „ Oficjalne wytyczne praktyki klinicznej ERS/ATS: wentylacja nieinwazyjna w ostrej niewydolności oddechowej ” , European Respiratory Journal , tom. 50 N O 2sierpień 2017, s. 1602426 ( ISSN 0903-1936 i 1399-3003 , DOI 10.1183 / 13993003.02426-2016 , czytaj online , konsultacja 4 lutego 2020 r. ).
- (en) Do Craiga Davidsona , Stephena Banhama , Marka Elliotta i Daniela Kennedy'ego , „ Wytyczne BTS/ICS dotyczące postępowania wentylacyjnego w ostrej hiperkapnicznej niewydolności oddechowej u dorosłych ” , Thorax , tom. 71, n o Suppl 2kwiecień 2016, ii1 – ii35 ( ISSN 0040-6376 i 1468-3296 , DOI 10.1136 / thoraxjnl-2015-208209 , czytaj online , dostęp 4 lutego 2020 ).
Powiązane artykuły
Częste przyczyny zaburzeń oddechowych- Pneumopatia
- Niewydolność serca i ostry obrzęk płuc
- Zaostrzenie POChP
- Zespół ostrej niewydolności oddechowej
- Tlenoterapia donosowa o wysokim przepływie
- Wentylacja nieinwazyjna
- Wentylacja inwazyjna: intubacja i tracheostomia
- Pozaustrojowe natlenianie błonowe
- Sztuczny respirator
Linki zewnętrzne
- Zaburzenia oddechowe: informacje dla pacjentów , Claudia Steurer-Stey, Revue Médicale Suisse (2015; tom 11, strony 1965-1966).
- Co zrobić z ostrą niewydolnością oddechową , krajowa kolegium nauczycieli resuscytacji medycznej.
- Ogólny przegląd sztucznej wentylacji , Bhakti K. Patel, Manuel Merck , kwiecień 2018.
- Niewystarczająca wentylacja , Bhakti K. Patel, Manuel Merck , kwiecień 2018.