Argon
| Argon | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Argon stały i płynny. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pozycja w układzie okresowym | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Symbol | Ar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nazwisko | Argon | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liczba atomowa | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupa | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Okres | 3 e okres | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | Zablokuj p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rodzina elementów | gaz szlachetny | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroniczna Konfiguracja | [ Ne ] 3 s 2 3 p 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektrony według poziomu energii | 2, 8, 8 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomowe właściwości pierwiastka | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atomowa | 39,948 ± 0,001 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Promień atomowy (obliczony) | ( 71 po południu ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Promień kowalencyjny | 106 ± 10 po południu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Promień Van der Waalsa | 188 po południu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Stan utlenienia | 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlenek | nieznany | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energie jonizacji | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re : 15,759610 eV | 2 E : 27,62966 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 e : 40,74 eV | 4 E : 59,81 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5 e : 75.02 eV | 6 th : 91009 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7 e : 124,323 eV | 8 e : 143460 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 9 e : 422,45 eV | 10 e : 478,69 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 11 e : 538,96 eV | 12 e : 618,26 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 13 e : 686,10 eV | 14 e : 755,74 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 15 e : 854,77 eV | 16 th : 918,03 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 17 e : 4 120,8857 eV | 18 E : 4 426,2296 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Najbardziej stabilne izotopy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Proste właściwości fizyczne ciała | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Państwo zwykłe | Gaz (niemagnetyczny) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
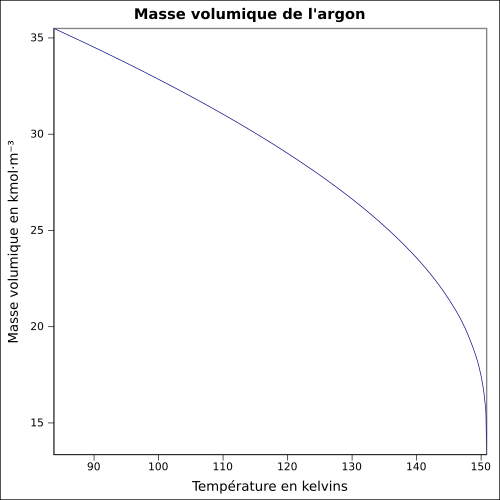
| Masa objętościowa |
1,7837 g · L -1 ( 0 ° C , 1 atm ) równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kryształowy system | sześcienny skupiony na twarzy | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kolor | bezbarwny | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punkt fuzji | −189,36 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura wrzenia | -185,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia termojądrowa | 1188 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energia parowania | 6,43 kJ · mol -1 ( 1 atm , -185,85 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura krytyczna | -122,3 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Potrójny punkt | -189.3442 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Objętość molowa | 22,414 × 10 -3 m 3 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ciśnienie pary |
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Prędkość dźwięku | 319 m · s -1 do 20 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ogromne ciepło |
520 J · kg -1 · K -1
równanie:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Przewodność cieplna | 0,01772 W · m -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Różny | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O ECHA | 100 028 315 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O WE | 231-147-0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Środki ostrożności | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Ostrzeżenie H280 i P403 H280 : Zawiera gaz pod ciśnieniem; ogrzanie grozi wybuchem P403 : Przechowywać w dobrze wentylowanym miejscu. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 DO, A : Temperatura krytyczna sprężonego gazu = -122.4 ° C Ujawnienie przy 1,0% zgodnie z kryteriami klasyfikacji classification |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20 : gaz duszący lub gaz, który nie stanowi dodatkowego zagrożenia Numer UN : 1006 : SPRĘŻONY ARGON Klasa: 2.2 Kod klasyfikacyjny: 1A : Sprężony gaz, duszący; Etykieta: 2.2 : Gazy niepalne, nietoksyczne (odpowiada grupom oznaczonym literą A lub dużą literą O); 
22 : gaz skroplony schłodzony, duszący Numer UN : 1951 : ARGON CIEKŁY SCHŁODZONY Klasa: 2.2 Kod klasyfikacyjny: 3A : Gaz skroplony schłodzony, duszący; Etykieta: 2.2 : Gazy niepalne, nietoksyczne (odpowiada grupom oznaczonym literą A lub dużą literą O);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jednostki SI i STP, chyba że zaznaczono inaczej. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Argon jest pierwiastkiem o liczbie atomowej do 18, a symbol Ar. Należy do grupy 18 układu okresowego pierwiastków i jest częścią rodziny z gazów szlachetnych , zwany również „gazy szlachetne”, który zawiera także hel , tym neon , krypton , ksenon i radon . Argon jest 3 ul , najczęściej występującym składnikiem w atmosferze ziemskiej , z ułamku masowym do 1,288%, co odpowiada frakcji objętościowej 0,934% (lub 9340 ppm ), i jest najbardziej rozpowszechnionym gaz szlachetny na świecie. Skorupy ziemskiej , co odpowiada 1,5 ppm . Argonu w atmosferze ziemskiej jest prawie w całości składa się z argonu, 40 , A radiogeniczny nuklid wynikające z rozkładu na potasu 40 , a argon obserwowano w świata składają się przede wszystkim z argonu 36 , wyprodukowany przez gwiazdowego nukleosyntezy w supernowych .
Nazwa argon pochodzi od starożytnego greckiego ἀργόν, oznaczającego „bezczynny”, „leniwy” [pochodzi od greckiego słowa ἀεργός, utworzonego od ἀ-εργός, co oznacza „bez pracy”, „bezczynny”], w odniesieniu do tego, że pierwiastek jest chemicznie obojętny. Jego konfiguracja elektronowa przedstawia nasyconą warstwę walencyjną u źródła jej stabilności i wirtualną niemożność ustanowienia wiązań kowalencyjnych . Temperatury od 83.805 8 K z jego punktem potrójnym jest jednym z punktów odniesienia z międzynarodową skalą temperatury 1990 (ITS-90).
Argon jest produkowany przemysłowo przez frakcyjną destylację z ciekłego powietrza . Stosowany jest przede wszystkim jako atmosfera obojętna do spawania i różnych procesów przemysłowych w wysokiej temperaturze z udziałem substancji reaktywnych. Atmosferę argonu stosuje się zatem w grafitowych elektrycznych piecach łukowych, aby zapobiec spalaniu tego ostatniego. Wykorzystuje również argon w oświetleniu żarówkami , świetlówkami i lampami gazowymi . Służy do produkcji niebiesko-zielonych laserów gazowych.
Główne właściwości
Argon jest bezbarwny, bezwonny, niepalny i nietoksyczny w stanie gazowym, ciekłym lub stałym. Jego rozpuszczalność w wodzie jest z grubsza porównywalna z tlenem i jest 2,5 razy większa niż azotu . Jest chemicznie obojętny w prawie wszystkich warunkach i nie tworzy żadnych potwierdzonych związków chemicznych w temperaturze pokojowej .
Argon jest jednak zdolny do tworzenia związków chemicznych w pewnych ekstremalnych warunkach braku równowagi. Argonu fluorohydrure Harf ten sposób otrzymano przez fotolizy ultrafiolecie z fluorowodoru HF w matrycy kriogenicznego z cezu jodku CSI Ar argonem stabilna poniżej 27 K ( -246,15 ° C ), została zidentyfikowana za pomocą spektroskopii w podczerwieni . Fluorowodorek argonu jest jedynym znanym związkiem argonu, który jest obojętny i stabilny w stanie podstawowym .
Argon może również tworzyć klatraty w wodzie, gdy jego atomy są uwięzione w trójwymiarowej sieci utworzonej przez lód . Istnieją również jony wieloatomowe zawierające argon, takie jak kation wodorku argonu ArH + oraz ekscypleksy , takie jak Ar 2* i ArF *. Różne związki z wiązaniami Ar C i Ar Jeśli są stabilne, przewidywano za pomocą symulacji numerycznej, ale nie zostały zsyntetyzowane w laboratorium.
Główne izotopy argonu, obecnego w skorupie ziemskiej są argonu 40 ( 40 Ar), 99,6%, argonu 36 ( 36 Ar), 0,34% i w argon 38 ( 38 Ar), 0,06%. Potasu 40 ( 40 K), rozpada się spontanicznie w ilości 11,2% w argon 40 przez wychwytywanie elektronów lub tomografii emisyjnej i w ilości 88,8% w wapnia, 40 ( 40 Ca) o p dezintegracji - z okresem półtrwania (pół -życie) 1,25 miliarda lat. Ten czas trwania oraz stosunek powstających produktów ubocznych umożliwiają określenie wieku skał metodą datowania potasowo-argonowego .
W w atmosferze ziemskiej , argonu 39 jest wytwarzany głównie przez oddziaływanie promieniowania kosmicznego, w atmosferze argonu, 40 przez wychwytywanie neutronów po podwójnym emisji neutronów . W podłożu może być również wytwarzany z potasu 39 poprzez wychwytywanie neutronów, a następnie emisję protonów .
Argonu 37 powstaje podczas testów podziemnych z wapniem 40 przez wychwytywanie neutronów następnie alfa dezintegracji ; ma okres półtrwania 35 dni.
Argon wyróżnia się tym, że jego skład izotopowy znacznie się różni w zależności od regionu Układu Słonecznego . Argon, którego głównym źródłem jest radioaktywny rozpad potasu 40 w skałach, składa się głównie z argonu 40 , podobnie jak na planetach ziemskich zachowujących atmosferę: Wenus , Ziemia i Mars . Z drugiej strony, argon utworzony bezpośrednio przez gwiezdną nukleosyntezę składa się zasadniczo z argonu 36 wytwarzanego w reakcji alfa , jak w przypadku Słońca , którego argon stanowi 84,6% argonu 36 zgodnie z pomiarami wiatru słonecznego . Tak samo jest na gigantycznych planetach , gdzie względna obfitość izotopów 36 Ar: 38 Ar: 40 Ar wynosi 8400:1600:1.
Oprócz atmosfery ziemskiej , której udział objętościowy argonu wynosi 0,934%, czyli 9340 ppm , atmosfera Merkurego zawiera 0,07 ppm , Wenus 70 ppm , a Marsa 19,300 ppm , czyli 1,93%.
Przewaga radiogenicznym argonu 40 w atmosferze ziemskiej jest odpowiedzialna za fakt, że masa atomowa argonu Ziemi, rzędu 39.95 u , 0,85 u większa niż w przypadku potasu , który następuje to w okresowego pierwiastków i którego masa atomowa jest rzędu 39,10 u . Wydawało się to paradoksalne podczas odkrycia argonu w 1894 roku, ponieważ Dymitr Mendelejew ułożył swój układ okresowy pierwiastków w kolejności zwiększającej się masy atomowej, co doprowadziło do konieczności umieszczenia argonu pomiędzy potasem i wapniem , o masie atomowej około 40,08 u i pomylenia z argonu z dokładnością do 0,13 u , podczas gdy różnica mas atomowych między chlorem (35,45 u ) a potasem (39,10 u ) wynosiła 3,65 u . Problem ten rozwiązał Henry Moseley , który w 1913 roku wykazał, że układ okresowy pierwiastków powinien być ułożony w kolejności rosnącej liczby atomowej , a nie zwiększającej się masy atomowej, która układa pierwiastki we właściwej kolejności.
Atmosferycznego obfitość względna argonu w stosunku do innych gazów szlachetnych - 9340 ppm argonu przed 5,24 ppm z helem , 18,18 ppm z neonem , 1,14 ppm z kryptonu i 0,087 ppm do ksenonu - może także być przypisany radiogenicznym argonu 40 : argonu 36 to wprawdzie obfitość tylko 31,5 ppm (0,337% z 9340 ppm ), tego samego rzędu wielkości co neon (18,18 ppm ).
Związki
Argonu atom posiada elektronów nasycony walencyjne powłoki , z pełną s i p podwarstwy . To sprawia, że pierwiastek ten jest chemicznie obojętny i bardzo stabilny, to znaczy, że z wielkim trudem tworzy wiązanie chemiczne z innymi atomami. Aż do 1962 , gazy szlachetne uznano za całkowicie obojętna i nie nadaje się do tworzenia się związków chemicznych ; jednak w tej chwili synteza heksafluoroplatynianu ksenonu XePtF 6 utorował drogę chemii gazów szlachetnych .
Pierwszy związek argonu z pentakarbonylem wolframu o wzorze chemicznym W (CO) 5 Ar, została opublikowana w 1975 roku, ale jej faktyczne istnienie pozostaje kwestionowane. W sierpniu 1962 został zsyntetyzowany w University of Helsinki Fluorowodorek argonu Harf przez fotolizy ultrafiolecie z fluorowodoru HF w matrycy kriogenicznego z cezu jodku CSI Ar argonu związek stabilny poniżej 27 K ( -246,15 ° C ) określonego za pomocą spektroskopii w podczerwieni . To odkrycie doprowadziło do pomysłu, że argon może tworzyć słabo związane związki.
Dication metastabilny ARCf 22+ , izoelektroniczny z fluorkiem karbonylu COF 2i fosgen COCl 2z punktu widzenia elektronów walencyjnych zaobserwowano w 2009 roku wprowadzenie wiązania węgiel- argon. Jon cząsteczkowy 36 ArH + , odpowiadające w argon kationu wodorek 36 (argonium) został wykryty w międzygwiazdowej na poziomie Crab mgławicy ; jest to pierwszy związek gazu szlachetnego wykryty w kosmosie .
Stały wodorek argonu Ar (H 2 ) 2jest związkiem van der Waalsa mającym taką samą strukturę krystaliczną jak faza Lavesa (en) MgZn 2. Tworzy się pod ciśnieniem od 4,3 do 220 GPa , chociaż wyniki uzyskane za pomocą spektroskopii Ramana sugerują, że cząsteczki H 2związku Ar (H 2 ) 2dysocjować powyżej 175 GPa .
Produkcja przemysłowa i aplikacje
Argon jest produkowany przemysłowo przez frakcyjną destylację z ciekłego powietrza w jednostki kriogenicznej z destylacji powietrza (w) , metody rozdzielania z ciekłego azotu , który wrze w temperaturze 77,3 K , argon, który wrze w temperaturze 87,3 K , i ciekłego tlenu , która wrze w temperaturze 90,2 K . Światowa produkcja argonu jest rzędu 700 000 ton rocznie.
Argon ma kilka interesujących właściwości, które uzasadniają jego przemysłowe zastosowanie:
- jest gazem chemicznie obojętnym;
- jest tanią alternatywą, gdy azot nie jest wystarczająco obojętny;
- ma niską przewodność cieplną (jest więc izolatorem termicznym );
- jego właściwości elektroniczne ( jonizacja , widmo emisyjne ) są wykorzystywane w niektórych zastosowaniach oświetleniowych.
Inne gazy szlachetne wykazują podobne właściwości i również mogą być stosowane, ale argon jest zdecydowanie najtańszym ze wszystkich, otrzymywanym jako produkt uboczny ekstrakcji tlenu i azotu z powietrza w kriogenicznej destylacji frakcyjnej.
Zastosowania przemysłowe
Argon jest używany w niektórych wysokotemperaturowych procesach przemysłowych, w których chemicznie obojętne substancje mają tendencję do reagowania. Atmosferę argonu jest używane w piecach elektrycznych z grafitu elektrody w celu zapobieżenia spalaniu tego materiału.
W przypadku niektórych z tych procesów obecność azotu lub tlenu powodowałaby defekty materiału. Argon jest stosowany w niektórych rodzajach spawania łukowego, takich jak spawanie łukowe w osłonie gazów i TIG , a także w obróbce odczynników tytanu i innych pierwiastków . Kryształy krzemu i germanu przeznaczone dla przemysłu półprzewodników są również hodowane w atmosferze argonu, aby zapewnić ich krystaliczną jakość.
Argon jest używany w przemyśle drobiarskim jako metoda obojętnym uduszenie gazu do udusić się drób , albo do uboju masy po wystąpieniu choroby lub środka uboju na przemian Elektronarkoza . Względna gęstość argonu do powietrza powoduje, że podczas gazowania pozostaje on blisko ziemi. Jego niereaktywny charakter sprawia, że jest kompatybilny z produktami spożywczymi, a fakt, że częściowo zastępuje tlen w tkankach, wydłuża okres przydatności do spożycia żywności.
Argon jest czasem używany do gaszenia pożarów poprzez konserwację cennego sprzętu, takiego jak serwery komputerowe , który mógłby zostać uszkodzony przy użyciu wody lub piany.
Zastosowania medyczne
Procedury kriochirurgii (w), takie jak krioablacja (w), wykorzystują ciekły argon do niszczenia tkanek, takich jak komórki rakowe . Możliwe było zastosowanie go w procedurze zwanej koagulacją wspomaganą argonem , która jest formą elektrochirurgii (w) przy użyciu palnika plazmowego , ale która stwarza ryzyko zatoru gazowego, objawiającego się śmiercią co najmniej jednego pacjenta.
Niebieski laser argonowy, stosuje się w chirurgii do szwów na tętnice zniszczyć nowotworu w chirurgii oka , lub elektrokoagulację za pomocą endoskopowych urzędniczej zmian krwawienia z przewodu pokarmowego.
Argon został również przetestowany pod kątem zastąpienia azotu w gazie oddechowym zwanym argoxem w celu przyspieszenia usuwania rozpuszczonego azotu z krwi .
Badania naukowe
Ciekły argon jest używany jako cel do wykrywania neutrin i badań ciemnej materii . Interakcje pomiędzy hipotetycznych WIMPów i jądra z argonu atomów powinno prowadzić do zaobserwowania scyntylacyjnych przez fotopowielania rur . Detektory dwufazowe zawierające argon służą do wykrywania elektronów wytwarzanych w wyniku jonizacji podczas oddziaływań WIMP-jądro argonowe.
Podobnie jak inne skroplone gazy szlachetne, ciekły argon ma wysoki współczynnik scyntylacji (około 51 fotonów / keV ), jest przezroczysty dla własnej scyntylacji i jest stosunkowo łatwy do oczyszczenia. Jest tańszy niż ksenon i ma inny profil czasu scyntylacji, co umożliwia odróżnienie oddziaływań elektronowych od oddziaływań jądrowych. Należy jednak silniejsze radioaktywności p ze względu na zanieczyszczenia w atmosferze argonu 39 , za wyjątkiem tego argonu z piwnicy Ziemia zubożonego w 39 Ar, którego okres półtrwania jest tylko 269 lat i którego czas nie jest odtwarzany przez 40 Ar ( n , 2 n ) 39 Ar interakcja z promieniowaniem kosmicznym w atmosferze argonu .
W innym rejestrze argon 39 został użyty w szczególności do datowania rdzeni wód gruntowych i lodowych na Antarktydzie . K Ar celownik i argon argon celownik są również stosowane w radiometrycznym pochodzącym z osadowego , metamorficzne i ogniowy .
Konserwatywny
Argon o numerze E938 jest używany jako konserwant żywności do usuwania tlenu i wilgoci z atmosfery w opakowaniach oraz do opóźniania jego ważności. Utleniania przez powietrze, do hydrolizy i inne reakcje , które rozkładają się w ten sposób produktu są opóźnione lub całkowicie zablokowany. Odczynniki chemiczne i cząsteczki farmaceutyczne są czasami pakowane w atmosferze argonu. Ten szlachetny gaz jest również używany jako konserwant do lakierów , poliuretanów, a nawet farb .
Argon jest również stosowany w produkcji wina do ochrony wina przed tlenem i zapobiegania jego utlenianiu oraz niepożądanym interakcjom bakteryjnym (zwłaszcza bakteriom octowym , które wytwarzają kwas octowy i zamieniają wino w ocet ). Może być również używany jako gaz pędny do opryskiwaczy .
Sprzęt laboratoryjny
Argon może być używany jako gaz obojętny w przewodzie próżniowym i schowku na rękawiczki ; jest korzystniejszy od azotu , który jest tańszy, ponieważ azot może reagować ze szczególnie reaktywnymi związkami, a także z pewnym sprzętem. Ponadto argon ma tę zaletę, że jest gęstszy niż powietrze, w przeciwieństwie do azotu, co ułatwia jego stosowanie w praktyce.
Argon może być używany jako gaz nośny w chromatografii gazowej i jonizacji elektrorozpylania . Jest gazem z wyboru dla plazmy stosowanej w spektrometrii plazmy sprzężonej indukcyjnie . Argon jest korzystnie stosowany do osadzania napylanego (In) na próbkach, które mają być badane za pomocą skaningowego mikroskopu elektronowego oraz do czyszczenia płytek w mikrofabrykacji .
Oświetlenie
Żarówka jest zwykle wypełniona argonem, w celu zachowania ich włókna z wysokiej temperatury utleniania . Argon jest również używany do promieniowania przez jonizację , jak w lampach plazmowych i kalorymetrach w fizyce cząstek . Wyładowcze wypełnione czystego argonu wytwarzają światło jasno fioletowy ciągnięcie lawendy lebleu, który staje się niebieski dodając małą rtęć .
Argon jest również używany w laserach jonowych (w) niebieskim i zielonym.
Różne zastosowania
Argon służy jako izolator termiczny do szyb zespolonych . Wykorzystywany jest również do napełniania suchych skafandrów do nurkowania ze względu na swoją obojętność chemiczną i niską przewodność cieplną .
Argon jest jednym z gazów, które mogą być wykorzystywane w astronautyce jako paliwo do silników VASIMR . W dziedzinie uzbrojenia lotniczego stosowany jest pod ciśnieniem do chłodzenia, poprzez rozluźnienie, głowic niektórych pocisków powietrze-powietrze , w tym pocisków AIM-9 Sidewinder .
Argon był używany w lekkiej atletyce jako domieszka symulująca niedotlenienie . W związku z tym znalazł się wraz z ksenonem na liście metod i substancji zakazanych przez Światową Agencję Antydopingową w 2014 r., zanim został wycofany w 2020 r.
Historia i etymologia
Słowo argon wywodzi się ze starożytnego greckiego ἀργός / argós („bezczynny”, „leniwy”, „sterylny”), utworzonego przez prywatny grecki przedrostek ἀ i słowo ἔργον / ergon („praca”), ta etymologia przywołuje charakter obojętny elementu '.
Obecność w powietrzu chemicznie obojętnego gazu podejrzewał Henry Cavendish już w 1785 roku, ale jego odkrycie przez Lorda Rayleigha i Sir Williama Ramsaya w University College London zaczekało do 1894 roku . Zrobili to, usuwając tlen , dwutlenek węgla , parę wodną i azot z próbki czystego powietrza , pozostawiając gaz obojętny, który nazwali argonem . Ci dwaj naukowcy oficjalnie powiadomili Royal Society o swoim odkryciu w dniu31 stycznia 1895 r.
Postawił ich na torze fakt, że chemicznie wytwarzany azot był o 0,5% lżejszy od tego, który został wyekstrahowany z powietrza przez usunięcie innych znanych wówczas gazów atmosferycznych. Destylacja frakcyjna skroplonego powietrza pozwoliła im w 1898 roku wyprodukować znaczną ilość argonu i jednocześnie wyizolować dwa inne gazy szlachetne – neon i ksenon .
Argon zaobserwowano również w 1882 roku podczas niezależnych prac HF Newalla i WN Hartleya, którzy zauważyli linie widmowe w widmie emisyjnym powietrza nieodpowiadające żadnemu znanemu pierwiastkowi chemicznemu .
Symbol chemiczny dla argonu w odniesieniu do 1957 roku było, jeśli się Ar.
Niebezpieczeństwa
Podobnie jak hel , argon w niskich stężeniach nie jest niebezpieczny. Jest jednak o 38% gęstszy od powietrza , a wdychanie dużej ilości argonu niesie ze sobą ryzyko uduszenia z powodu niedotlenienia ( niedotlenienia ); może się to zdarzyć na przykład podczas operacji spawania w ograniczonej przestrzeni.
Uwagi i referencje
- (w) Beatriz Cordero Verónica Gómez, Ana E. Platero-Prats, Marc Revés Jorge Echeverría, Eduard Cremades, Flavia i Santiago Barragan Alvarez , „ Kowalentne promienie ponownie ” , Dalton Transactions ,2008, s. 2832 - 2838 ( DOI 10.1039 / b801115j )
- (w) David R. Lide, CRC Handbook of Chemistry and Physics , TF-CRC,2006, 87 th ed. ( ISBN 0849304873 ) , s. 10-202
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 th ed. , 2804 s. , Oprawa twarda ( ISBN 978-1-420-09084-0 )
- (en) Robert H. Perry i Donald W. Green , Perry's Chemical Engineers' Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 pkt. ( ISBN 0-07-049841-5 ) , s. 2-50
- Protokół Międzynarodowy Komitet Miar i Wag , 78 th sesji, 1989, pp. T1-T21 (oraz s. T23-T42, wersja angielska).
- Baza danych Chemical Abstracts zapytana przez SciFinder Web 15 grudnia 2009 r. ( wyniki wyszukiwania )
- Wpis numeru CAS „7440-37-1” w chemicznej bazie danych GESTIS IFA (niemiecki organ odpowiedzialny za bezpieczeństwo i higienę pracy) ( niemiecki , angielski ), dostęp w dniu 30 stycznia 2009 r. (wymagany JavaScript)
- „ Argon ” w bazie produktów chemicznych Reptox z CSST (Quebec organizacji odpowiedzialnej za bezpieczeństwo i higienę pracy), dostęp 25 kwietnia 2009
- (w) Markku Räsänen , „ Argon z powietrza ” , Nature Chemistry , tom. 6, n O 1, Styczeń 2014Artykuł n O 82 ( PMID 24345939 , DOI 10.1038 / nchem.1825 , czytać online )
- (i) Leonid Khriachtchev Mika Pettersson Nino Runeberg Jan Lundell i Markku Räsänen , „ Stabilny związek argonu ” , Naturę , tom. 406 n O 6798, 24 sierpnia 2000, s. 874-876 ( PMID 10972285 , DOI 10.1038/35022551 , Bibcode 2000Natur.406..874K , czytaj online )
- (w) VR Belosludov OS Subbotin DS Krupskii, Prokuda OV, RV i Y. Belosludov Kawazoe , „ Mikroskopowy model związków klatratowych ” , Journal of Physics: Conference Series , tom. 29, n o 1, styczeń 2006, s. 1-7 ( DOI 10.1088/1742-6596/ 29 /1/ 001 , Bibcode 2006JPhCS..29.... 1B , czytaj online )
- (w) Arik Cohen, Jan Lundell i R. Benny Gerber , „ Pierwsze związki z wiązaniami chemicznymi argon-argon i węgiel-krzem ” , Journal of Chemical Physics , tom. 119 n O 13, Październik 2003, s. 6415-6417 ( DOI 10.1063/1.1613631 , kod bib 2003JChPh.119.6415C , przeczytaj online )
- (en) J. Emsley, Nature's Building Blocks , Oxford University Press, 2001, s. 44–45 . ( ISBN 978-0-19-960563-7 )
- Etienne Roth ( dir. ), Bernard Poty ( dir. ), Robert Delmas et al. ( pref. Jean Coulomb ), Metody datowania za pomocą naturalnych zjawisk jądrowych , Paryż, Éditions Masson , coll. "Kolekcja CEA ",1985, 631 s. ( ISBN 978-2-225-80674-2 , informacja BNF n O FRBNF34836710 ) , rozdz. 17 („Krzem 32 i argon 39”)
- (w) The Science Case for 37 Ar jako monitor podziemnych wybuchów jądrowych , strona 1, 2010
- (w) Katharina Lodders , „ Argon Obfitości Słonecznej ” , The Astrophysical Journal , tom. 674, N O 1, 10 lutego 2008, s. 607-611 ( DOI 10.1086/524725 , Bibcode 2008ApJ... 674..607L , arXiv arXiv: 0710.4523 , czytaj online )
- (w) AGW Cameron , „ Pierwiastkowe i izotopowe obfitości lotnych pierwiastków na planetach zewnętrznych ” , „ Space Science Reviews” , tom. 14, n kości 3-4 Marzec 1973, s. 392-400 ( DOI 10.1007/BF00214750 , Bibcode 1973SSRv... 14..392C , czytaj online )
- (w) Marco Fontani , Mariagrazia Costa i Mary Virginia Orna , The Lost Elements: The Periodic Table's Shadow Side , New York, Oxford University Press ,2015( 1 st ed. 2014), 531 , str. ( ISBN 9780199383344 ) , s. 182.
- (w) Neil Bartlett , „ Heksafluoroplatynian ksenonu Xe + [PtF 6 ] - " , Proceedings of the Chemical Society , N O 6,Czerwiec 1962, s. 197-236 ( DOI 10.1039/PS9620000197 , przeczytaj online )
- (w) Nigel A. Young , „ Chemia koordynacyjna grupy głównej w niskiej temperaturze: przegląd macierzy izolowanych kompleksów od grupy 12 do grupy 18 ” , „ Coordination Chemistry Reviews” , tom. 257 n kości 5-6, Marzec 2013, s. 956-1010 ( DOI 10.1016 / j.ccr.2012.10.013 , przeczytaj online )
- (w) Neil Bartlett , „ Gazy szlachetne ” , Wiadomości chemiczne i inżynieryjne , tom. 81 N O 36, 8 września 2003 r., s. 32-34 ( DOI 10.1021/cen-v081n036.p032 , czytaj online )
- (w) Jessica F. Lockyear Kevin Douglas, Stephen D. Price, Małgorzata Karwowska, Karol J. Fijalkowski Wojciech Grochala Marek Remeš Jana Roithová i Detlef Schroeder , „ Generacja ARCf 2 2+ Dykcja ”, The Journal of Physical Chemistry Letters ,tom. 1,N O 1,8 grudnia 2009, s. 358-362 ( DOI 10.1021/jz900274p , przeczytaj online )
- (en) J. Barlow, BM Swinyard, PJ Owen, J. Cernicharo, HL Gomez, RJ Ivison, O. Krause, TL Lim, M. Matsuura, S. Miller, G. Olofsson i AND Polehampton , „ Wykrywanie Molekularny Jon Gazu Szlachetnego, 36 ArH + , w Mgławicy Krab ” , Science , tom. 342 n O 6164, 13 grudnia 2013 r., s. 1343-1345 ( PMID 24337290 , DOI 10.1126/ nauka.1243582 , Bibcode 2013Sci... 342.1343B , czytaj online )
- (w) Annette K. Kleppe, Mónica Amboage i Andrew P. Jephcoat , „ Nowy wysokociśnieniowy związek van der Waalsa Kr (H 2) 4 odkryty w systemie binarnym krypton-wodór ” , „ Scientific Reports” , tom. 4,16 maja 2014 r.Artykuł n o 4989 ( DOI 10.1038 / srep04989 , bibcode 2014NatSR ... 4E4989K , czytać online )
- „ Układ okresowy pierwiastków: Argon - Ar ” , Environmentalchemistry.com (dostęp 12 września 2008 r. )
- (w) Sara J. Shields i ABM Raj , „ Krytyczny przegląd elektrycznych systemów ogłuszania w łaźni wodnej do uboju drobiu i najnowsze osiągnięcia w technologiach alternatywnych ” , Journal of Applied Animal Welfare Science , tom. 13 N O 4, 2012, s. 281-299 ( PMID 20865613 , DOI 10.1080/10888705.2010.507119 , czytaj online )
- DL Fletcher , „ Technologia uboju ”, Sympozjum: Najnowsze postępy w technologii uboju drobiu ,1999( Czytaj online , obejrzano 1 st stycznia 2010 )
- (w) MJ Fraqueza i AS Barreto , „ Efektem jest trwałość mięsa indyczego w opakowaniach ze zmodyfikowaną atmosferą z mieszaniną argonu ” , Poultry Science , tom. 88 N O 9, wrzesień 1999, s. 1991-1998 ( PMID 19687286 , DOI 10.3382/ps.2008-00239 , czytaj online )
- (w) Joseph Z. Su, Andrew K. Kim, George P. Crampton i Zhigang Liu , „ Tłumienie ognia za pomocą gazów obojętnych ” , Journal of Fire Protection Engineering , tom. 11 N O 2 2001, s. 72-87 ( DOI 10.1106/X21V-YQKU-PMKP-XGTP , przeczytaj online )
- (w) „ Śmiertelny zator gazowy spowodowany nadmiernym ciśnieniem podczas laparoskopowego stosowania koagulacji wzmocnionej argonem ” , Urządzenia zdrowotne , tom. 23, n o 6, Czerwiec 1994, s. 257-259 ( czytaj online )
- (w) Jerome Canady , Kimberly Wiley i Biagio Ravo , " Koagulacja plazmą argonową i przyszłe zastosowania sond endoskopowych Dual-Mode " , Reviews in Gastroenterological Disorders , tom. 6, n O 1,2006, s. 1-12 ( ISSN 1533-001X , PMID 16520707 , odczyt online , dostęp 9 października 2017 ).
- (w) Andrew A Pilmanis Ulf I. Balldin, James T. Webb i Kevin M. Krause , „ Dekompresja etapowa do 3,5 psi przy użyciu 100% mieszanek argonowo-tlenowych i tlenowych ” , lotnictwo, przestrzeń kosmiczna i medycyna środowiskowa , lot. 74 N O 12, grudzień 2003, s. 1243-1250 ( PMID 14692466 , czytaj online )
- (w) Dan Gastler Ed Kearns, Andrew Hime, Laura C. Stonehill Stan Seibert, Josh Klein, Hugh W. Lippincott, Daniel N. McKinsey i James A. Nikkel , „ Pomiar sprawności scyntylacyjnej odrzutów jądrowych w ciekłym argonie ” , Przegląd fizyczny C , tom. 85, n o 6, 27 czerwca 2012Artykuł n o 065.811 ( DOI 10,1103 / PhysRevC.85.065811 , bibcode 2012PhRvC..85f5811G , arXiv 1004,0373 , czytać online )
- (w) J.Xu F. Calaprice, C. Galbiati, A. Goretti Guray G., T. Hohman, D. Holtz, An. Ianni, Pan Laubenstein, Loer B., C. Lovec, CJ Martov, D. Montanari, S. Mukhopadhyay, A. Nelson, SD Rountree, RB Vogelaar i A. Wright , „ Studium śladowej zawartości 39 Ar w argonie ze źródeł głęboko pod ziemią ” , Astroparticle Physics , tom. 66, czerwiec 2015, s. 53-60 ( DOI 10.1016 / j.astropartphys.2015.01.002 , Bibcode 2015APh .... 66 ... 53X , arXiv 1204.6011 , czytaj online )
- Paul Depovere, Układ okresowy pierwiastków. Podstawowy cud Wszechświata , De Boeck Supérieur ,2002, s. 98.
- (en) Henry Cavendish , „ XXIII. Eksperymenty na powietrzu. ” , Philosophical Transactions of the Royal Society of London , tom. 75, 1785, s. 372-384 ( DOI 10.1098/rstl.1785.0023 , Bibcode 1785RSPT... 75..372C , czytaj online )
- (w) Robert John Strutt i William Ramsay , „ I. Argon, nowa forma atmosfery ” , Proceedings of the Royal Society of London , tom. 57, 1895, s. 265-287 ( DOI 10.1098/rspl.1894.0149 , JSTOR 115394 , czytaj online )
- (w) John William Strutt i William Ramsay , „ VI. Argon, nowy składnik atmosfery ” , Philosophical Transactions of the Royal Society of London , 1895, s. 187-241 ( DOI 10.1098/rsta.1895.0006 , JSTOR 90645 , Bibcode 1895RSPTA.186..187R , czytaj online )
- (w) Sir William Ramsay, „ The Rare Gases of the Atmosphere ” , https://www.nobelprize.org/ , Nagroda Nobla w dziedzinie chemii , 12 grudnia 1904(dostęp 14 czerwca 2020 r . ) .
- (w) John H. Holloway, chemia gazów szlachetnych , Methuen,1968, s. 6
- (w) John Emsley, Nature's Building Blocks: An AZ Guide to the Elements , Oxford University Press, 2003, s. 36 . ( ISBN 0198503407 )
- (w) Norman E. Holden, „ Historia pochodzenia pierwiastków chemicznych i ich odkrywców ” , 41. Zgromadzenie Ogólne IUPAC w Brisbane, Australia, 29 czerwca – 8 lipca 2001 r. , https://www.nndc.bnl. gov / , Narodowe Centrum Danych Jądrowych , 12 marca 2004 r.(dostęp 14 czerwca 2020 r . ) .
Zobacz również
Powiązane artykuły
Linki zewnętrzne
- (pl) „ Dane techniczne dla argonu ” (dostęp 24 kwietnia 2016 r. ) , ze znanymi danymi dla każdego izotopu na podstronach
- (W) Obrazy argonu w różnych formach
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | h | Hej | |||||||||||||||||||||||||||||||
| 2 | Li | Być | b | VS | NIE | O | F | Urodzić się | |||||||||||||||||||||||||
| 3 | nie dotyczy | Mg | Glin | TAk | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | To | Sc | Ti | V | Cr | Mn | Fe | Współ | Lub | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Tak | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | płyta CD | w | Sn | Sb | ty | i | Xe | |||||||||||||||
| 6 | Cs | Ba | ten | Ten | Pr | NS | Po południu | Sm | Miał | Bóg | Tb | Dy | Ho | Er | Tm | Yb | Czytać | Hf | Twój | W | D | Kość | Ir | Pt | Na | Hg | Tl | Pb | Bi | Po | Na | Rn | |
| 7 | Fr | Ra | Ac | NS | Rocznie | U | Np | Mógł | Jestem | Cm | Bk | cf | Jest | Fm | Md | Nie | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
|
Metale alkaliczne |
Ziemia alkaliczna |
Lantanowce |
Metale przejściowe |
Słabe metale |
metalem loids |
Długoterminowe metale |
geny halo |
Gazy szlachetne |
Przedmioty niesklasyfikowane |
| aktynowce | |||||||||
| Superaktynowce | |||||||||